Hoofdstuk 16 – Experimenten
1. Eiwitten
1.1. Aanslag op het oog
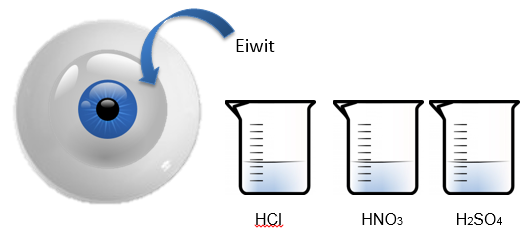
- Info: Wat gebeurt er als we eiwit laten reageren met HCl, HNO3 en H2SO4? We zien dat het gebruik van sterke zuren zorgt voor chemische reacties zoals neerslagvorming (eiwit + HCl). Dit is een irreversibel proces omdat de sterke zuren zorgen voor een hydrolyse van de peptidebindingen tussen de aminozuren.
- Moeilijkheid: eenvoudig
- Chemische stoffen: eiwit van rauw ei 6 mol/l HCl – HNO3 10 mol/l – H2SO4 geconcentreerd
- Thema: biochemie
- Tijd: 15 min
- Begrippen: eiwitten – neerslagreactie
1.2. Alcoholcement

- Info: Wat gebeurt er als we eiwitten behandelen met zuren? Zowel cola als azijn bevatten zuren. Cola bevat fosforzuur en azijn bestaat natuurlijk uit een lage concentratie azijnzuur. Het zuur zorgt voor de denaturatie van de eiwitten die we terugvinden in de Baileys.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Azijn – Cola – Baileys / koffiemelk/ cream
- Thema: biochemie
- Tijd: 15 min
- Begrippen: eiwitten – neerslagreactie – denaturatie
1.3. Baileys en Tonic

- Info: Tonic heeft een pH van rond de 2,5 en Cola rond de 3 en zijn dus in staat om de pH-waarde van de emulsie onder de 4,6 te brengen, waardoor de emulsie opbreekt en gaat schiften
- Moeilijkheid: eenvoudig
- Chemische stoffen: 100 ml Baileys – 100 ml tonic
- Thema: biochemie
- Tijd: 15 min
- Begrippen: eiwitten – neerslagreactie – denaturatie
1.4. Bloed opsporen met luminol
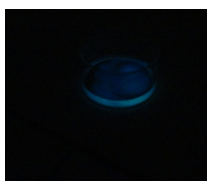
- Info: Luminol onthult vaak niet alleen de aanwezigheid van bloed op het plaats delict,maar ook andere sporen die van belang zijn voor het forensisch onderzoek.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 1 g luminol – 1 g natriumcarbonaat – 7 g natriumperboraat – Bloed of nepbloed (FeCl3) – 3% waterstofperoxide oplossing
- Thema: biochemie
- Tijd: 15 min
- Begrippen: eiwitten – luminescentie
1.5. Bloedijs

- Info: Hoe kunnen we ijs maken met bloed?.Het waterstofperoxide ontleedt zich in water en zuurstof. De vrijgekomen zuurstof heeft een sterk oxiderende kracht. De eiwitten in het bloed houden die zuurstof vast. Hierdoor krijgen we schuim.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Bloed – Waterstofperoxide 30%
- Thema: biochemie
- Tijd: 15 min
- Begrippen: eiwitten – schuimvorming – enzymen
1.6. Eitje bakken met calciumoxide

- Info: Calcium oxide reageert exothermisch met water en vormt Calciumdihydroxide
- Moeilijkheid: eenvoudig
- Chemische stoffen: Ei – Calciumoxide
- Thema: biochemie – neerslagreacties – exo-energetische reactie
- Tijd: 15 min
- Begrippen: eiwitten – denatureren

- Info: Wat gebeurt er wanneer we een haar onderdompelen in een base? Haar is opgebouwd uit het eiwit keratine. Bij het onderdompelen van het haar in het mengsel van NaOH en water treedt er een hydrolyse van de eiwitten op.
- Moeilijkheid: eenvoudig
- Chemische stoffen: NaOH-korrels – Haar
- Thema: biochemie
- Tijd: 15 min
- Begrippen: eiwitten – denatureren – hydrolyse
1.8. Identificatie van eiwitten

- Info: Xanthoproteïnereactie
- Moeilijkheid: eenvoudig
- Chemische stoffen: caseïnepoeder -geconcentreerd salpeterzuur
- Thema: biochemie
- Tijd: 15 min
- Begrippen: eiwitten – identificatie
1.9. Kunstmatige kaviaar

- Info: Algenzuur is een kleurloze met carboxylgroepen polysaccharide welke men in bruinalgen vindt. In koud water zijn ze onoplosbaar, in warmer water eventueel aangezuurd, lossen ze op.
- Moeilijkheid: eenvoudig
- Chemische stoffen: kopersulfaat 5.H2O – natriumalginaat – gedestilleerd water
- Thema: biochemie
- Tijd: 15 min
- Begrippen: eiwitten – denaturatie
1.10. Omkeerbare reactie onder invloed van licht

- Info: Kunnen we een stof laten ontkleuren door er licht op te schijnen ? Thionine is een organische verbinding die in twee vormen kan voorkomen: een kleurloze gereduceerde vorm, en een paarse, geoxideerde vorm. Het kan gebruikt worden als een redoxindicator.Wanneer een reductor, zoals Fe2+-ionen, toegevoegd wordt aan een zure thionine-oplossing, dan wordt deze omgezet in de kleurloze gereduceerde vorm, terwijl Fe2+ geoxideerd wordt naar Fe3+.
- Moeilijkheid: eenvoudig
- Chemische stoffen: FeSO4.7H2O, 2,0 g – H2SO4-oplossing, 1 mol.l-1 – thionine-oplossing 0,001 mol.l-1
- Thema: biochemie – chemische reactie
- Tijd: 15 min
- Begrippen: eiwitten – denaturatie – fotolyse
1.11. Zoutzuurwerking op peptidebindingen in de maag nabootsen

- Info: Hoe worden eiwitten ontleed in de maag? De ene oplossing blijft troebel, die met zoutzuur wordt helder, dit omdat het enzyme alleen werkt in zuur milieu
- Moeilijkheid: eenvoudig
- Chemische stoffen: Pepsinogeen – Magere kwark – Zoutzuur 1 mol/l
- Thema: biochemie – chemische reactie
- Tijd: 15 min
- Begrippen: eiwitten – denaturatie – enzymen
1.12. Aminozuren aantonen met chocolade

- Info: Hoe kunnen we in een product (chocolade) aminozuren aantonen? De chocoladeoplossing kleurt violet, terwijl de proefbuis zonder chocolade kleurloos blijft.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Ninhydrineoplossing – Volle melkchocolade
- Thema: biochemie – chemische reactie
- Tijd: 15 min
- Begrippen: eiwitten – denaturatie – identificatie
1.13. Xanthoproteïnereactie

- Info: Hoe kun je proteïne detecteren?Het salpeterzuur coaguleert het eiwit en denatureert het. Het gedenatureerde, samengeklonterde eiwit is wit van kleur. Bij verhitting worden waterstofatomen in het eiwit vervangen door nitroverbindingen (nitroverbindingen bevatten altijd stikstof ) uit salpeterzuur . Dit proteïne– nitro-complex is geel van kleur.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 4 ml vijf keer verdund ei – 4 ml 20% salpeterzuuroplossing
- Thema: biochemie – chemische reactie
- Tijd: 15 min
- Begrippen: eiwitten – denaturatie – identificatie
1.14. Denaturatie van eiwitten

- Info: Wat gebeurt er in ons lichaam als we alcohol drinken? Ethanol is een celgif. De structuur van het eiwit verandert doordat water wordt afgesplitst (ethanol wil verdunnen). Hierdoor werkt alcohol uitstekend als ontsmettingsmiddel.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 1 ei – 20 druppels ethanol
- Thema: biochemie – chemische reactie
- Tijd: 15 min
- Begrippen: eiwitten – denaturatie
1.15. Hydrolyse van eiwitten

- Info: Hoe kun je eiwitten hydrolyseren? Door hydrolyse worden de peptidebindingen afgebroken tot aminozuren.
- Moeilijkheid: eenvoudig
- Chemische stoffen: gelatine – gec zwavelzuur – kopercarbonaat- universele indicator
- Thema: biochemie – chemische reactie
- Tijd: 15 min
- Begrippen: eiwitten – denaturatie
1.16. Onderzoek van aminozuren

- Info: Hoe kun je bepaalde aminozuren aantonen?
- Moeilijkheid: eenvoudig
- Chemische stoffen: glycine – arginine – kopercarbonaat – sakaghuchi reagens – hopkins-cole
- Thema: biochemie – chemische reactie
- Tijd: 30 min
- Begrippen: eiwitten – identificatie
1.17. Onderzoek van zwitterionvorming en het iso-elektrisch punt
- Info: Hoe kun je het iso-elektrisch punt van tyrosine aantonen? De aminozuursuspensie reageert neutraal. Tyrosine lost zowel op in basisch als in zuur milieu. Tyrosine komt zoals alle ionen zowel in vaste als in opgeloste vorm voor als een zwitterion. Bij toevoeging van een base ontstaat een anion, bij toevoeging van een zuur ontstaat een kation.
- Moeilijkheid: eenvoudig
- Chemische stoffen: thyrosine – universele indicator – zoutzuur 0.1 mol/l – natriumhydroxide 0.1 mol/l
- Thema: biochemie – chemische reactie – neutralisatiereactie
- Tijd: 30 min
- Begrippen: eiwitten – identificatie
1.18. Opbouw van een aminozuur

- Info: Hoe is een aminozuur opgebouwd? Identificatie van de functionele groepen
- Moeilijkheid: eenvoudig
- Chemische stoffen:glycine – universele indicator – zoutzuur 0.1 mol/l – natriumhydroxide 0.1 mol/l – ninhydrine reagens
- Thema: biochemie – chemische reactie – neutralisatiereactie
- Tijd: 30 min
- Begrippen: eiwitten – identificatie
1.19. Bereiding van het aminozuur glycine

- Info: Hoe kun je het aminozuur glycine maken? Uit monochloorazijnzuur en ammoniak is glycine te bereiden. Hierbij ontstaat een kristal.
- Moeilijkheid: eenvoudig
- Chemische stoffen: chloorazijnzuur – ammoniakoplossing
- Thema: biochemie – chemische reactie – neutralisatiereactie
- Tijd: 30 min
- Begrippen: eiwitten – identificatie
1.20. Eiwitten in bloedserum

- Info: Hoe kan je de eiwitten in bloedserum onderscheiden?In water opgeloste eiwitten zijn omgeven door een laag van ionen. Door het uitzouten worden deze onttrokken en gaat het eiwit uitzouten. Op basis van een verschil in concentratie gebeurt eerst het uitzouten van globuline, het albumine is zeer goed oplosbaar in water en zal een volledige uitzouting nodig hebben..
- Moeilijkheid: eenvoudig
- Chemische stoffen: eiwit – verzadigd ammoniumsulfaat – ethaanzuur
- Thema: biochemie – chemische reactie – neutralisatiereactie
- Tijd: 30 min
- Begrippen: eiwitten – identificatie – denaturatie
1.21. Kleurreacties met eiwitten

- Info: Wat zijn de belangrijkste kleurreacties met eiwitten?
- Moeilijkheid: eenvoudig
- Chemische stoffen: eiwit – salpeterzuur – millons reagens
- Thema: biochemie – chemische reactie – neutralisatiereactie
- Tijd: 30 min
- Begrippen: eiwitten – identificatie – denaturatie
1.22. Eigenschappen van eiwitten
- Info: Wat zijn de belangrijkste eigenschappen van eiwitten?
- Moeilijkheid: eenvoudig
- Chemische stoffen: eiwit – ethanol – tannine oplossing – kopersulfaat
- Thema: biochemie – chemische reactie – neutralisatiereactie
- Tijd: 30 min
- Begrippen: eiwitten – identificatie – denaturatie
1.23. Samenstelling van eiwitten

- Info: Hoe zijn eiwitten opgebouwd? Eiwitten worden in alkalimetaalhydroxiden volledig afgebroken waarbij gebonden zwavel en sulfiden ontstaan die met loodionen loodsulfide vormen, een donkerbruine neerslag. Hierbij wordt aangetoond dat eiwitten zwavel bevatten.
- Moeilijkheid: eenvoudig
- Chemische stoffen: eiwit – loodacetaat – natriumhydroxide – zoutzuur
- Thema: biochemie – chemische reactie – neutralisatiereactie
- Tijd: 30 min
- Begrippen: eiwitten – identificatie – denaturatie
1.24.Identificatie via biureetreactie

- Info: Hoe kun je eiwitten aantonen? Alle verbindingen met minstens 2 peptidebindingen vertonen een violetkleuring door de biureetreactie.
- Moeilijkheid: eenvoudig
- Chemische stoffen: eiwit – haines reagens
- Thema: biochemie – chemische reactie – neutralisatiereactie
- Tijd: 30 min
- Begrippen: eiwitten – identificatie – denaturatie
2. Suikers
2.1. Algemeen
2.1.1. Proeven op suikers

- Info: Hoe kun je suikers aantonen? Door gebruik van testkits
- Moeilijkheid: eenvoudig
- Chemische stoffen: suiker -clinistix
- Thema: biochemie – chemische reactie
- Tijd: 10 min
- Begrippen: suikers – identificatie
2.1.2. Onderscheid tussen chocolade en ‘dieetchocolade’

- Info: Hoe kunnen we chocolade onderscheiden van ‘dieetchocolade’? In het eerste deel van de proef gaan we chocolade laten smelten in aceton. Dit doen we omdat aceton vet oplost en wij willen het vet scheiden van de chocolade.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Verschillende soorten chocolade, – aceton
- Thema: biochemie – chemische reactie – neutralisatiereactie
- Tijd: 10 min
- Begrippen: suikers – identificatie
2.1.3. Snoepjes: gelatine of pectine?

- Info: Hoe kunnen we vaststellen of het geleermiddel in een snoepje gelatine of pectine is? Peptidebindingen in gummibeertjes vormen met kopersulfaat een violette complex zout . De kleur kan variëren van blauwviolet naar roodviolet afhankelijk van de hoeveelheid peptidebindingen. De kleurintensiteit is een maat voor de eiwitconcentratie.
- Moeilijkheid: eenvoudig
- Chemische stoffen: gummibeertjes – zure snoepjes – CuSO4-oplossing (0,1 mol/l) – NaOH-oplossing (3 mol/l)
- Thema: biochemie – chemische reactie
- Tijd: 10 min
- Begrippen: suikers – identificatie
2.1.4. Elementen in suikers

- Info: Welke chemische elementen komen voor in suikers?
- Moeilijkheid: eenvoudig
- Chemische stoffen: soorten suikers – magnesium – koper(II)sulfaat – zoutzuur
- Thema: biochemie – chemische reactie
- Tijd: 10 min
- Begrippen: suikers – identificatie
2.1.5. Koolhydraten lossen goed op in water
- Info: Hoe kun je aantonen dat suikers goed oplossen in water? Glucose en sucrose zijn goed oplosbaar in water. Zetmeel vormt een colloïdale oplossing in water. Dit kan goed worden waargenomen als de oplossing met een lichtbron wordt bestraald: tyndall-effect.
- Moeilijkheid: eenvoudig
- Chemische stoffen: soorten suikers – water – benzine
- Thema: biochemie – chemische reactie – eigenschappen van stoffen
- Tijd: 10 min
- Begrippen: suikers -oplosbaarheid
2.1.6. Identificatiereacties bij suikers

- Info: Hoe zijn suikers opgebouwd? Molisch reagens : Bij deze reactie ontstaat aan de interfase een violette ring. Seliwanow reactie : Bij deze reactie wordt ketonenfuncties aangetoond. Hierbij worden fructose- en sucrose-oplossingen na ongeveer 1 min rood. Bij aldosen gebeurt deze kleurvorming pas later. Bial-reactie : De ribose-oplossing wordt blauwgroen. Het gaat over een specifiek onderzoek van pentosen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: soorten suikers – molisch reagens – seliwanow – bialreagens
- Thema: biochemie – chemische reactie – eigenschappen van stoffen
- Tijd: 30 min
- Begrippen: suikers – identificatie
2.1.7. Bereiding en eigenschappen van dextrines

- Info: Hoe kun je dextrine bekomen? Onder invloed van de warmte en het sterk verdunde zuur ontstaat een onvolledige afbraak van zetmeel. Er ontstaat het geelbruine dextrine. Door een behandeling met de lugoloplossing wordt zetmeel blauw, door de afbraak bruinpaars tot bruin. Het resultaat is een tussenproduct tussen zetmeel en glucose.
- Moeilijkheid: eenvoudig
- Chemische stoffen: zetmeel – lugoloplossing – salpeterzuur – ethanol
- Thema: biochemie – chemische reactie
- Tijd: 30 min
- Begrippen: suikers – identificatie
2.1.8. Onderscheid maken tussen cola en cola light
- Info: Hoe maak je het onderscheid tussen cola en cola light? Door ontkleuring van blauw naar rood wordt in cola gewoon het glucose aangetoond. De test op cola light is negatief.
- Moeilijkheid: eenvoudig
- Chemische stoffen: cola – cola light – haines reagens
- Thema: biochemie – chemische reactie
- Tijd: 30 min
- Begrippen: suikers – identificatie
2.2. Cellulose
2.2.1. Nitrocellulose

- Info: Ontbrandt een pingpongballetje als we dit aansteken? Katoenen watten bestaan voor vrijwel 100% uit cellulose, een polymeer van ß D-glucose, bestaande uit lange onvertakte ketens met 2000-3000 glucose-eenheden. Door de reactie met salpeterzuur, hierboven in rood aangegeven als HONO2, ontstaat de nitraat ester van cellulose. De OH-groepen van cellulose verliezen hierbij een proton en salpeterzuur een OH-groep om samen een molecuul water te vormen. Deze reactie is een evenwichtsreactie, maar doordat de zwavelzuur het vrijkomende water bindt is de reactie aflopend naar rechts.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Salpeterzuur 70%: HNO3 – Zwavelzuur 98%: H2SO4 – Natriumwaterstofcarbonaat: NaHCO3 – Watten (100% katoen)
- Thema: biochemie – chemische reactie
- Tijd: 30 min
- Begrippen: suikers – cellulose – verbrandingsreactie
2.2.2. Onoplosbare suiker

- Info: Het collodion zorgt voor een semipermeabel membraan rond de suiker en belet dat de suiker snel oplost in het water. Door de semi-permeabele wand beweegt wel, zij het traag water. In dat water lost suiker op en het suikerwater beweegt traag door het membraan.
- Moeilijkheid: eenvoudig
- Chemische stoffen: klontje suiker – collodionoplossing 4%
- Thema: biochemie – chemische reactie
- Tijd: 30 min
- Begrippen: suikers – cellulose – diffusie
2.2.3. Papier maken

- Info: Hoe kunnen we zelf papier maken? We maken een mengsel van papier en water. Hierdoor wordt het papier zacht en kan je het in kleine deeltjes verdeeld. Wanneer we het papier laten drogen, krijgen we een gerecycleerd velletje papier.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Oud papier – Water
- Thema: biochemie – chemische reactie
- Tijd: 30 min
- Begrippen: suikers – cellulose
2.2.4. Productie van celluloid
- Info: Hoe kunnen we zelf celluloïd maken? Bereiding van cellulosedinitraat en dan hieruit kan de bereiding van celluloïd gebeuren
- Moeilijkheid: eenvoudig
- Chemische stoffen: Campher= C10H16O – Mangaandioxide – Aceton – Ethanol
- Thema: biochemie – chemische reactie
- Tijd: 30 min
- Begrippen: suikers – cellulose
2.2.5. Productie van celluloidfolie

- Info: Hoe kunnen we zelf celluloïdfolie maken? Bereiding van cellulosedinitraat en dan hieruit kan de bereiding van celluloïd gebeuren
- Moeilijkheid: eenvoudig
- Chemische stoffen: Campher – Butaan-1-ol – Aceton – Vaseline
- Thema: biochemie – chemische reactie
- Tijd: 30 min
- Begrippen: suikers – cellulose
2.2.6. Zure hydrolyse van cellulose
- Info: Hoe kun je cellulose hydrolyseren? Door de zure hydrolyse wordt het cellulose afgebroken tot glucose. Door de donkere kleur van de stalen bij de test met chloorzinkjoodoplossing en de seleendioxide oplossing duidt het hydrolyseproduct een positief resultaat voor glucose. Dit is ook aan te tonen met de glucosesticks.
- Moeilijkheid: eenvoudig
- Chemische stoffen: cellulose – geconcentreerd zoutzuur – glucosetest
- Thema: biochemie – chemische reactie
- Tijd: 30 min
- Begrippen: suikers – cellulose
2.3. Enkelvoudige suikers
2.3.1. Aantonen van de optische activiteit met fructose

- Info: Hoe kan je aantonen dat er een optische activiteit plaatsvindt bij een suikeroplossing?
- Moeilijkheid: eenvoudig
- Chemische stoffen: D-fructose
- Thema: biochemie – eigenschappen van stoffen
- Tijd: 30 min
- Begrippen: suikers – enkelvoudige suikers – fructose
2.3.2. Aantoningsreactie van glucose

- Info: Hoe kunnen we glucose aantonen in vloeistoffen? Met behulp van teststrookjes proberen wij de aanwezigheid van glucose in de drie oplossingen te bepalen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Clinistix – Glucose – Coca cola – Cola light – Cola zero
- Thema: biochemie
- Tijd: 20 min
- Begrippen: suikers – enkelvoudige suikers – identificatie
2.3.3. Chemische patronen in een waterige oplossing

- Info: en petrischaal wordt op een overhead gezet met 10 ml zetmeeloplossing 0,5% en 40 ml KI oplossing. Het bereide filtreerpapier wordt op de petrischaal gelegd. Na 1 minuut wordt hij verwijderd. Een wolk verschijnt die geleidelijk van rood naar blauw kleurt. Met een lege pasteur kan door trage bewegingen in de wolk patronen worden gemaakt.
- Moeilijkheid: eenvoudig
- Chemische stoffen: joodoplossing in ethanol 10%, – 0.1 mol/l KI, – zetmeeloplossing 0,5%
- Thema: biochemie
- Tijd: 20 min
- Begrippen: suikers – enkelvoudige suikers – patronen
2.3.4. De klassieke blauwe kolf

- Info: Methyleenblauw is een aromatische verbinding die opgelost in water blauw kleurt. Het is een redoxindicator die een duidelijke kleurverandering ondergaat op een specifieke potentiaal.Glucose wordt in een alkalische oplossing langzaam geoxideerd door zuurstof met vorming van gluconzuur. In aanwezigheid van natriumhydroxide is gluconzuur omgezet naar natriumgluconaat.
- Moeilijkheid: gemiddeld
- Chemische stoffen: 10 g glucose – 12 g vast NaOH – 0.1 massa% methyleenblauwoplossing in ethanol
- Thema: anorganische stoffen – chemisch evenwicht – reactiesnelheid – biochemie
- Tijd: 20 min
- Begrippen: oscillerende reactie – enkelvoudige suikers
2.3.5. Gistkanon

- Info:De gistcellen gaan in deze oplossing zich vermenigvuldigen en eveneens starten met de vergistingsreactie waarbij de suikers omgezet worden naar ethanol en koolstofdioxide.De gevormde koolstofdioxide gaat opstapelen boven de oplossing en door de hoger wordende gasdruk wordt de stop weggeschoten.
- Moeilijkheid: gemiddeld
- Chemische stoffen: sucrose – gist
- Thema: biochemie
- Tijd: 20 min
- Begrippen: gisten – sucrose
2.3.6. Kerstbal maken

- Info:Tijdens het schudden ontstaat aan de binnenzijde van het glas al vrij snel een donkerbruine halfdoorzichtige laag die steeds meer gaat spiegelen en uiteindelijk ondoorzichtig wordt. Binnen een paar minuten is de spiegel gevormd. Na afloop van de reactie bevat de erlenmeyer een grof zandkleurig neerslag.
Opvallend is dat de zilverlaag voornamelijk spiegelt aan de buitenzijde van de erlenmeyer, aan de binnenzijde van het glas is de zilverlaag licht goudbruin. - Moeilijkheid: gemiddeld
- Chemische stoffen: Salpeterzuur 70% – AgNO3 – KOH – Glucose – Ammoniak 35%
- Thema: biochemie – organische stoffen
- Tijd: 20 min
- Begrippen: gisten – glucose – reactie aldehyden
2.3.7. Maak de traagste chemiekameleon

- Info: Onder invloed van NaOH zal het permanganaat met de suiker reageren. Wat overblijft is bruinsteen. Permanganaat is sterk paars en bruinsteen geel/bruin. Omdat de reactie afhankelijk is van temperatuur en concentraties, zal de reactie in deze verhoudingen vrij langzaam verlopen. De kleurveranderingen zijn dan ook mooi te zien.
De laatste verandering, van groen naar geel en geel/bruin, duurt het langst. Die van paars naar donkerpaars gaat vrij snel. - Moeilijkheid: eenvoudig
- Chemische stoffen: KMnO4 – NaOH – suiker
- Thema: organische stoffen – redoxreacties – biochemie
- Tijd: 20 min
- Begrippen: reacties met organische stoffen – oxidatie – enkelvoudige suikers
2.3.8. Misconcept over neutralisatiereacties

- Info: Is het toevoegen van suiker aan citroensap ook een neutralisatiereactie? Suiker neutraliseert zuur niet. Het maskeert de zure smaak.
- Moeilijkheid: eenvoudig
- Chemische stoffen: citroensap – universele indicator – kalkpoeder
- Thema: organische stoffen – biochemie – neutralisatiereactie
- Tijd: 20 min
- Begrippen: enkelvoudige suikers
2.3.9. Blauwe fles met gummibeertjes

- Info: Hoe kunnen we een fles water blauw kleuren zonder gebruik te maken van de kleurstof aanwezig in de gummibeertjes? n het alkalische milieu van glucose reduceert methyleenblauw tot het kleurloze leuko-methyleenblauw. De glucose wordt geoxideerd tot gluconzuur. Door krachtig schudden met de kleurloze oplossing diffundeert zuurstof in de oplossing en reoxideert de leuko-methyleenblauw naar methyleenblauw. De twee reacties gaan zo lang op tot de glucose volledig wordt toegepast of er geen zuurstofmeer aanwezig is.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Gummibeertjes (geen rode) – Natriumhydroxide schilfers – methyleenblauwoplossing
- Thema: organische stoffen – biochemie – redoxreactie
- Tijd: 20 min
- Begrippen: enkelvoudige suikers
2.3.10. Suiker aantonen in kauwgom

- Info: Hoe kunnen we suiker aantonen in kauwgom? We kunnen het verschil in kauwgom aantonen door gist toe te voegen. Gist zet suiker om tot ethanol en koolstofdioxide. Dit is zichtbaar bij de suikerhoudende kauwgom. Koolstofdioxide nemen we waar door de belletjes die ontstaat en het Staalname potje en doordat de ballon licht opblaast.
- Moeilijkheid: eenvoudig
- Chemische stoffen: suikervrije kauwgom – suikerhoudende kauwgom – droge gist – water
- Thema: organische stoffen – biochemie – redoxreactie
- Tijd: 20 min
- Begrippen: enkelvoudige suikers – gistreactie
2.3.11. Glucose in ketchup

- Info: Hoe tonen we glucose aan in Ketchup? Men gaat de eiwitten uit de ketchup verwijderen door het Carrez-Reagens eraan toe te voegen. Door de zinkionen worden de aanwezige eiwitten neergeslagen (uitzouting) Vervolgens heeft men een kleurloze ketchup met een hoog gehalte van glucose. Deze gaat men aantonen door Fehling I en Natriumhydroxide toe te voegen. De Koper-II ionen in de ketchup worden dan gereduceerd tot Koper-I ionen en dit geeft een rode neerslag.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Ketchup – Gedestilleerd water – Fehling I – Natriumhydroxide – Carrez-Reagens I – Carrez-Reagens II
- Thema: organische stoffen – biochemie – redoxreactie
- Tijd: 20 min
- Begrippen: enkelvoudige suikers – identificatiereactie
2.3.12. Functionele groepen in glucosemoleculen

- Info: Welke functionele groepen vind je in een molecule glucose? De glucoseoplossing wordt gereduceerd met een ammoniakale zilvernitraatoplossing. Deze manier wordt gebruikt om aldehydefuncties aan te tonen.De -OH groepen veresteren azijnzuuranhydride. Op de bodem ontstaat veresterd glucose dat door geconcentreerd zwavelzuur hydrolyseert. Door de vrijzetting van ethaanzuurdamp kleurt de indicator rood.De glucoseoplossing reageert neutraal.
- Moeilijkheid: gemiddeld
- Chemische stoffen: glucose – gec zwavelzuur – azijnzuuranhydride – ammoniakale zilvernitraatoplossing
- Thema:biochemie – redoxreactie
- Tijd: 20 min
- Begrippen: enkelvoudige suikers – identificatie
2.3.13. Moleculestructuur van glucosemoleculen

- Info: Hoe zijn glucosemoleculen opgebouwd? In de lugolproef verloopt de reactie met methanol en glucose negatief. Bij aceton en ethanol ontstaat een gele neerslag door jodoform. Hierdoor wordt aangeduid dat er geen CH3-CHOH- en CH3COCH2– groep aanwezig is in glucose.Met het Schiffs reagens ontstaat bij de glucose-oplossing geen roodkleuring. Met ethanol wel. Dit duidt er op dat glucosemoleculen niet in een ketenstructuur voorkomen.
- Moeilijkheid: gemiddeld
- Chemische stoffen: glucose – schiffs reagens – ethanol – ethanal – methanol
- Thema:biochemie – redoxreactie
- Tijd: 20 min
- Begrippen: enkelvoudige suikers – identificatie
2.3.14. Reducerende werking van glucose
- Info: Hoe kun je de reducerende werking van glucose aantonen? Reactie met Haines reagens: Er ontstaat het rode koper(I)oxide? Dit reagens bevat een koper(II)-glycerine complex .
- Moeilijkheid: gemiddeld
- Chemische stoffen: glucose – haines reagens – fehlings reagens
- Thema:biochemie – redoxreactie
- Tijd: 20 min
- Begrippen: enkelvoudige suikers – identificatie
2.3.15. Onderzoek van glucose en fructose: onderscheid
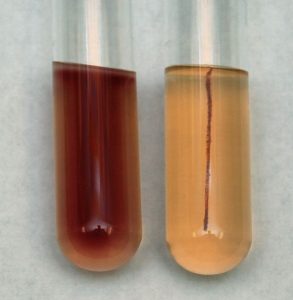
- Info: Hoe kun je fructose van glucose onderscheiden? Bij de GOD-test gebeurt de identificatie van glucose. Met fructose hebben de sticks geen verkleuring. Bij glucose ontstaat een blauwgroene kleuring. Deze kleuring ontstaat door een enzymatische reactie. Bij seleendioxide:Een fructose oplossing wordt hierbij van geelrood naar donkerrood. Een glucose-oplossing wordt doorzichtig en kleurt lichtgeel.
- Moeilijkheid: gemiddeld
- Chemische stoffen: glucose – fructose – seleendioxide – natriumcarbonaat
- Thema:biochemie – redoxreactie
- Tijd: 20 min
- Begrippen: enkelvoudige suikers – identificatie
2.4. Sucrose
2.4.1. Chemische kameleon
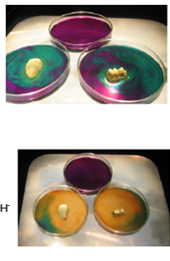
- Info: Onder invloed van NaOH zal het permanganaat met de suiker reageren. Wat overblijft is bruinsteen. Permanganaat is sterk paars en bruinsteen geel/bruin. Omdat de reactie afhankelijk is van temperatuur en concentraties, zal de reactie in deze verhoudingen vrij langzaam verlopen. De kleurveranderingen zijn dan ook mooi te zien. De laatste verandering, van groen naar geel en geel/bruin, duurt het langst. Die van paars naar donkerpaars gaat vrij snel.
- Moeilijkheid: eenvoudig
- Chemische stoffen: KMnO4 – saccharose – NaOH
- Thema: organische stoffen – redoxreacties – biochemie
- Tijd: 20 min
- Begrippen: reacties met organische stoffen – oxidatie – sucrose
2.4.2. Sucrose als reductor in chemische kleurverandering

- Info: Hoe kunnen we kleuren van stoffen veranderen met behulp van sacharose? Suiker is de reductor en zorgt ervoor dat het kaliumpermanganaat kan reduceren. De sucrose reageert met het paarse permanganaation
- Moeilijkheid: eenvoudig
- Chemische stoffen: KMnO4 – saccharose – NaOH
- Thema: redoxreacties – biochemie
- Tijd: 20 min
- Begrippen: reacties met organische stoffen – sucrose
2.4.3. Dichtheidsverschil cola en cola light

- Info: Hoe kunnen we het verschil tussen cola en cola light visueel aantonen? Het coca cola blikje zinkt en het blikje met coca cola light blijft drijven. Dit komt door de kleinere dichtheid van coca cola light, vanwege het lagere suikergehalte.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Blikje coca cola – Blikje coca cola light
- Thema:biochemie
- Tijd: 20 min
- Begrippen: massadichtheid – sucrose
2.4.4. Grootste zwarte slang uit suiker door middel van dehydratatie?

- Info: Hoe kan je de hoogste faraoslang maken met maximaal 20 gram vaste stof? Zoek de juiste verhouding van reagentia
- Moeilijkheid: eenvoudig
- Chemische stoffen: Natriumwaterstofcarbonaat – kristalsuiker – ethanol
- Thema:biochemie – chemische reactie
- Tijd: 20 min
- Begrippen: sucrose
2.4.5. Ontleding van suiker

- Info: Wat gebeurt er als je suiker verhit? Na warmtetoevoer ontleedt suiker in koolstof en water
- Moeilijkheid: eenvoudig
- Chemische stoffen:kristalsuiker
- Thema:biochemie – chemische reactie
- Tijd: 15 min
- Begrippen: sucrose – thermolyse
2.4.6. De suikerspin
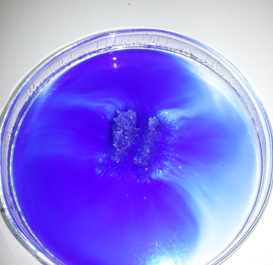
- Info: Wat gebeurt er met inkt op een suikerklontje als we dit in water leggen? De inkt wordt opgenomen in het suikerklontje. Als we deze dan in water leggen, zal het suikerklontje oplossen waardoor de inkt in draden ook zichtbaar zal uitlopen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: inkt – suikerklontje
- Thema:biochemie – chemische reactie
- Tijd: 15 min
- Begrippen: sucrose – diffusie
2.4.7. Thermolyse en verbranding van suiker

- Info: Hoe kunnen we suiker verbranden in plaats van te ontleden via thermolyse? Een suikerklontje zal niet zomaar branden. Leg je er sigarettenas op dan zal je zien dat het klontje zal blijven branden.Door de mengverhouding van het suikerklontje met het as kan het suikerklontje gaan branden tijdens dit verbrandingsproces zal de suiker afnemen als brandbare stof en de sigarettenas/CuO dienen als de katalysator en houdt het vuurtje brandend.
- Moeilijkheid: eenvoudig
- Chemische stoffen:koperoxide – suiker
- Thema:biochemie – chemische reactie
- Tijd: 25 min
- Begrippen: sucrose – verbrandingsreactie – thermolyse
2.4.8. Vonken uit suiker

- Info: Wat gebeurt er als we met een hamer op een suikerklontje slaan? Het verschijnsel dat plaatsvindt noemt men triboluminescentie.Op het moment dat je het suikerklontje fijnknijpt, raakt de elektrische lading in asymmetrische suikerkristallen ongelijk verdeeld. Des te meer suiker je breekt, des te meer de positieve en negatieve deeltjes gescheiden worden. Als het ladingsverschil tussen de brokken suiker groot genoeg wordt, springen negatief geladen elektronen over naar de suiker met de positieve lading.
- Moeilijkheid: eenvoudig
- Chemische stoffen: suikerklontje – hamer
- Thema:biochemie – chemische reactie – energetische uitwisseling
- Tijd: 15 min
- Begrippen: sucrose – triboluminescentie
2.4.9. Cola vs Cola Light

- Info: Wat merk je op bij het uitdampen en verbranden van Cola en Cola Light? Cola net als Cola Light bestaat uit een groot deel uit water. Het water verdampt. Het colastaaltje ruikt na een tijdje naar vanille, kaneel en daarna naar Karamelsuiker. Na een langere tijd komt er sterkere geur.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Cola – Cola Light
- Thema:biochemie – chemische reactie – energetische uitwisseling
- Tijd: 15 min
- Begrippen: sucrose – caramel
2.4.10. Vuurwerk met suiker

- Info: Hoe kunnen we aan de hand van suiker vuurwerk maken/nabootsen? Het zwavelzuur onttrekt water aan de suiker (hydraterende werking) . Dit is een erg exotherm proces. De hitte is voldoende om de verbrandingsreactie van suiker met kaliumchloraat – een sterke oxidator – in gang te zetten
- Moeilijkheid: eenvoudig
- Chemische stoffen: Kaliumchloraat (KClO3) – Sacharose (C12H22O11) – Zwavelzuur (H2SO4)
- Thema:biochemie – chemische reactie – exo- energetische uitwisseling
- Tijd: 15 min
- Begrippen: sucrose
2.4.11. Brandend suiker

- Info: Hoe kunnen we suiker blijvend laten branden? Het eerste suikerklontje brandt niet, omdat de lucifer niet genoeg energie geeft om de reactie te starten. Wanneer je het suikerklontje met as inwrijft, brandt het wel. Dit komt doordat de as meehelpt bij het verbranden van de suiker. Er is nu minder warmte nodig om de verbranding te starten.
- Moeilijkheid: eenvoudig
- Chemische stoffen: suikerklontje – sigarettenas
- Thema:biochemie – chemische reactie – exo- energetische uitwisseling
- Tijd: 15 min
- Begrippen: sucrose – katalysator
2.4.12. Chemisch stoplicht

- Info:Hoe kunnen we aan de hand van chemische reacties een oplossing de kleuren van een stoplicht krijgen? De indicator hier is indigokarmijn dat door de glucose omkeerbaar. Het indigokarmijn wordt gereduceerd van zijn basische groene vorm naar een gele, met als tussenstap een rode. Zuurstof uit de lucht oxideert de kleurstof weer terug van geel via rood naar groen
- Moeilijkheid: gemiddeld
- Chemische stoffen: 2 g druivensuiker of glucose (C6H12O6) – 75 ml natriumhydroxide 1 mol/l (NaOH) – 2 ml indigokarmijnoplossing 1%
- Thema:biochemie – chemische reactie – reactiesnelheid
- Tijd: 25 min
- Begrippen: sucrose – oscillerende reactie – klokreactie
2.4.13. Chemische kameleon alternatief

- Info: Onder invloed van NaOH zal het permanganaat met de suiker reageren. Wat overblijft is bruinsteen. Permanganaat is sterk paars en bruinsteen geel/bruin.
Omdat de reactie afhankelijk is van temperatuur en concentraties, zal de reactie in deze verhoudingen vrij langzaam verlopen. De kleurveranderingen zijn dan ook mooi te zien. - Moeilijkheid: gemiddeld
- Chemische stoffen: KMnO4 – saccharose – NaOH
- Thema:biochemie – redoxreactie
- Tijd: 25 min
- Begrippen: sucrose – meerdere oxidatiegetallen van mangaan
2.4.14. Maken van kunsthoning

- Info:Hoe kunnen we met chemische stoffen honing maken? Honing is een mengsel van glucose en fructose. Dit mengsel wordt gevormd door een hydrolyse van suiker met melkzuur (of tafelazijn) als katalysator. Het gevormd mengsel is een equimoleculair mengsel van glucose en fructose, ook invertsuiker genoemd.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Suiker – Melkzuur ( vervangbaar door azijnzuur) – water
- Thema:biochemie – redoxreactie
- Tijd: 25 min
- Begrippen: sucrose – invertsuiker
2.4.15. Verschil tussen groene en gele banaan

- Info:Wat is het verschil tussen een groene, gele en bruine banaan? We kunnen een onderscheid maken met behulp van de indicator iso-betadine. Wanneer er zetmeel aanwezig is zal de indicator van kleur veranderen namelijk van geel naar zwart. Bij de gele en bruine banaan is het aanwezig zetmeel omgezet door enzymen in suiker. Een banaan is rijp om te eten als ze geel is omdat ze dan zoeter en ook malser is dan een groene banaan die droog en hard is.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Groene, gele en bruine banaan – Iso-betadine
- Thema:biochemie – redoxreactie
- Tijd: 25 min
- Begrippen: sucrose – katalysator
2.4.16. Regenboog van suikerwater

- Info:Hoe kunnen we met behulp van suiker en water een regenboog maken? Door oplossingen van suiker te maken met een verschillende hoeveelheid van suiker creëren we oplossingen met verschillende dichtheden. Wanneer deze lagen rustig op elkaar aangebracht worden beginnende met de oplossing met de hoogste densiteit, blijven de verschillende lagen behouden.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Suiker – Water – Vloeibare kleurstoffen
- Thema:biochemie
- Tijd: 25 min
- Begrippen: sucrose – massadichtheid
2.4.17. Hydrolyse van sucrose en maltose
- Info:Hoe kun je de hydrolyse van sucrose en maltose uitvoeren? Een fructose oplossing wordt hierbij van geelrood naar donkerrood. Een glucose-oplossing wordt doorzichtig en kleurt lichtgeel.Door hydrolyse wordt uit sucrose fructose en glucose gevormd. Uit maltose ontstaat enkel glucose.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Suikers – Water – natriumhydroxide – seleendioxide
- Thema:biochemie
- Tijd: 25 min
- Begrippen: sucrose – hydrolyse – identificatie
2.5. Zetmeel
2.5.1. Dansende materie

- Info:Welke invloed heeft druk op de verandering van aggregatietoestand? Het mengsel van maïzena en water bestaat uit kleine vaste deeltjes die in suspensie zijn in water. Het mengsel verandert zeer snel van aggregatietoestand wanneer er veranderingen in druk optreden door bijvoorbeeld drukken, knijpen of vibreren.
- Moeilijkheid: gemiddeld
- Chemische stoffen: zetmeel/Maïzena – water
- Thema:biochemie
- Tijd: 25 min
- Begrippen: zetmeel – niet-newtoniaanse vloeistof
2.5.2. Flubberende zetmeel

- Info:Welke invloed heeft druk op de verandering van aggregatietoestand? Bij een langzame beweging werkt het water als een smeermiddel tussen de maïzenakorrels. Bij een snelle beweging druk je al het water weg, waardoor bewegen stroef gaat. Je merkt het ook bij het roeren: langzaam roeren lukt wel en snel roeren niet!
- Moeilijkheid: gemiddeld
- Chemische stoffen: 75 gram maïzena – Water
- Thema:biochemie
- Tijd: 25 min
- Begrippen: zetmeel – niet-newtoniaanse vloeistof
2.5.3. Eetbare folie uit zetmeel

- Info:Folie maken met zetmeel
- Moeilijkheid: gemiddeld
- Chemische stoffen: (rijst)zetmeel (3g) – glycerine oplossing (85%) – zoutzuur 0,1mol/l – NaOH 0,1mol/l
- Thema:biochemie – kunststoffen
- Tijd: 25 min
- Begrippen: zetmeel – bioplastics
2.5.4. Identificatie van biokunststof

- Info:Identifcatie van bioplastics door identificatie
- Moeilijkheid: gemiddeld
- Chemische stoffen: polystyreen verpakkingschips – stukje brood – lugol
- Thema:biochemie – kunststoffen
- Tijd: 25 min
- Begrippen: zetmeel – bioplastics
2.5.5. Kunststof uit rijstzetmeel

- Info:Voor de productie van zetmeelplastics wordt natief zetmeel gemengd met weekmakers (water en glycerol)
- Moeilijkheid: eenvoudig
- Chemische stoffen: maïszetmeel of rijststijfsel – glycerol – voedingskleurstof – huishoudazijn
- Thema:biochemie – kunststoffen
- Tijd: 25 min
- Begrippen: zetmeel – bioplastics
2.5.6. Magische hand
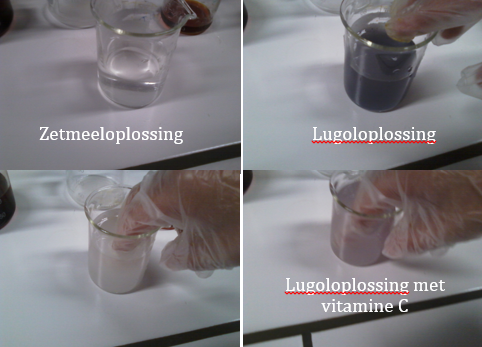
- Info:Hoe kunnen we met onze hand oplossingen van kleur doen veranderen?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Zetmeeloplossing van 1% – Vitamine C of ascorbinezuur – Lugol-oplossing
- Thema:biochemie – chemische reacties
- Tijd: 25 min
- Begrippen: zetmeel – identificatiereactie
2.5.7. Zetmeellijm

- Info:De zetmeelmoleculen en het water vormen samen een colloïdale oplossing. De lijm plakt heel goed, zolang je er maar voor zorgt dat de lijm droog blijft en de zetmeel moleculen niet opnieuw kunnen oplossen. Behangplaksel wordt van zetmeel gemaakt, daarom kun je behang er goed afhalen met stoom.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 1 aardappel – papier, kunststof – water
- Thema:biochemie
- Tijd: 20 min
- Begrippen: zetmeel – intermoleculaire krachten
2.5.8. Zwart wit geeft kleurloos

- Info:Hoe kan bij het samenvoegen van een witte en een zwarte oplossing, een kleurloze oplossing worden gevormd? Verschillende redoxreactie treden op met telkens een kleurverandering
- Moeilijkheid: gemiddeld
- Chemische stoffen: 10 ml joodtinctuur – 90 ml azijn – ascorbinezuur opgelost in 30 ml water – zetmeeloplossing – 15 ml hypochloriet in 45 ml water (=javel) – 150 ml water – een halve theelepel magnesiumsulfaat – huishoudammoniak 1 mol/l
- Thema: chemische reacties – redoxreacties – complexreactie – biochemie
- Tijd:35 min
- Begrippen: stofveranderingen – kleurveranderingen
2.5.9. Zetmeeltest

- Info: Hoe kunnen we de aanwezigheid van zetmeel in aardappelen aantonen? Identificatie met een dijoodoplossing
- Moeilijkheid: gemiddeld
- Chemische stoffen: 1 rauwe aardappel – dijoodoplossing
- Thema: chemische reacties – biochemie
- Tijd:35 min
- Begrippen: identificatie
2.5.10. Zetmeel in Smarties en M&M’s

- Info: Hoe kun je aantonen dat zetmeel aanwezig is in Smarties of M&M’s? Jodiumoplossing is een indicator die bruin/paars kleurt als deze in contact komt met zetmeel.
- Moeilijkheid: gemiddeld
- Chemische stoffen: M&M’s – Smarties – Jodiumoplossing
- Thema: chemische reacties – biochemie
- Tijd:15 min
- Begrippen: identificatie
2.5.11. Bioplastic uit zetmeel

- Info: Hoe kan je uit zetmeel plastic maken? Zetmeel is een voorbeeld van een polymeer van natuurlijke oorsprong. Deze polymeren worden direct geëxtraheerd en gewonnen uit diverse graangewassen (bijvoorbeeld tarwe en maïs), knolgewassen (bijvoorbeeld aardappels) en wortels.
- Moeilijkheid: gemiddeld
- Chemische stoffen: aardappelzetmeel – glycerol – azijn – demiwater
- Thema: kunststoffen – biochemie
- Tijd:30 min
- Begrippen: bioplastics
2.5.12. Blauw op drie wijzen

- Info: Hoe kunnen we een indicatordoekje op drie manieren van kleur doen veranderen? Dit van rood naar blauw en weer naar rood? De stof in oplossing is dijood, bij aanwezigheid van zetmeel ontstaat jood-zetmeelamylosecomplex met een blauwe kleur. Het dijood reageert vervolgens weg, waardoor het niet meer met zetmeel kan reageren en de blauwe kleur verdwijnt.Het doekje is rood door het congorood, dit is een zuur-base indicator bij een pH hoger dan 5.2 is de kleurstof rood, bij een lagere pH kleurt het blauw.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Ethanol – Zetmeel – H2SO4
- Thema: neutralisatie – chemische reactie – biochemie
- Tijd:30 min
- Begrippen: indicatorreactie
2.5.13. Druivensuiker uit zetmeel

- Info: Hoe kan je aantonen dat druivensuiker te bekomen is uit zetmeel? Door middel van de fehlingsreagens kan men aantonen dat zetmeel in zuur milieu (HCl) hydrolyseert tot glucose (druivensuiker). Het gevormde glucose kan aangetoond worden via het Fehlings reagens.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Zoutzuur 10% – Natriumcarbonaat – Fehlings A en B – Universeel indicatorpapier – Zetmeel
- Thema: chemische reactie – biochemie
- Tijd:30 min
- Begrippen: indicatorreactie – hydrolyse
2.5.14. Elektrische slijm

- Info: Hoe kunnen we elektrische slijm maken op basis van zonnebloemolie en bloem? De ballon wordt door het wrijven statisch geladen. Het bloem, dat bestaat uit zetmeel, is ook elektrisch geladen.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Bloem – Zonnebloemolie
- Thema: chemische reactie – biochemie
- Tijd:20 min
- Begrippen: elektrostatica
2.5.15. Maken van een harde vloeistof

- Info: Hoe kan je een” harde “vloeistof maken? Je kan een colloïdaal mengsel maken door zetmeel en water samen te voegen in een zelfde hoeveelheid.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Zetmeel (maïzena) – water
- Thema: biochemie
- Tijd:20 min
- Begrippen: niet-newtoniaanse vloeistof
2.5.16. Schrijven met zetmeel

- Info: Hoe kun je een boodschap schrijven met zetmeel?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Zetmeel (maïzena) – KI oplossing
- Thema: biochemie – redoxreactie
- Tijd:20 min
- Begrippen: zetmeel – elektrolyse
2.5.17. Schrijven met zetmeel alternatief
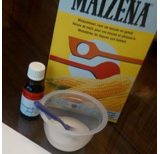
- Info: Hoe kan je een boodschap die geschreven is met zetmeel zichtbaar maken? De blauwzwarte kleur ontstaat op het equivalentiepunt bij de reactie tussen zetmeel en I2. I2 kunnen we gebruiken als indicator om zetmeel aan te tonen. Na het equivalentiepunt wordt de oplossing terug kleurloos.
- Moeilijkheid: eenvoudig
- Chemische stoffen: I2 – KI – 1 g (aardappel)zetmeel – Na2S2O3.5H2O
- Thema: biochemie – redoxreactie
- Tijd:20 min
- Begrippen: zetmeel
2.5.18. Zetmeel aantonen in een blad
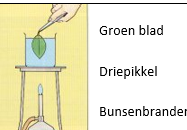
- Info: Is er zetmeel aanwezig in een blad? Hoe kan je de aanwezigheid van zetmeel in een blad aantonen? In een blad is er zetmeel aanwezig.Zodra licht op de bladgroenkorrels valt, vindt de lichtreactie plaats. Hierbij ontstaat zuurstof en wordt ATP gevormd. Er is water bij nodig. Een fractie van een seconde later gebeurt de zogeheten donkerreactie (hier is geen licht meer bij nodig): de energie uit de ATP wordt gebruikt om het energierijke glucose te maken.
- Moeilijkheid: eenvoudig
- Chemische stoffen: ontkleurde spiritus/ ethanol 96% – dijoodoplossing (Betadine)
- Thema: biochemie
- Tijd:20 min
- Begrippen: zetmeel – fotosynthese
2.5.19. Lopen op het water

- Info: Hoe kunnen we op water lopen? Wanneer we maïzena met water mengen, krijgen we een suspensie. De vaste deeltjes maïzena en het vloeibare water zijn door elkaar gemengd. Het is dus geen oplossing. Het gevormde mengsel is een niet-Newtoniaanse vloeistof:Wanneer er druk wordt uitgevoerd op het mengsel, worden de maïzena-deeltjes tegen elkaar aan geduwd. Hierdoor kan het water niet goed tussen de deeltjes door stromen. Indien er geen druk wordt uitgevoerd kan het water gewoon tussen de maïzena-deeltjes door stromen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Maïzena – Water
- Thema: biochemie
- Tijd:20 min
- Begrippen: zetmeel – niet-Newtoniaanse vloeistof
2.5.20. Vals geld ontdekken

- Info: Wat kunnen we waarnemen en welke reactie treedt er op wanneer we echt en nep geld testen met lugol? Zetmeel (C6H10O5)n vormt samen met lugol (KI en I2) een complex. Dit complex heeft de waargenomen zwart grijze kleur. Op het neppe bankbiljet blijft er een zwarte markering achter.
- Moeilijkheid: eenvoudig
- Chemische stoffen: echt bankbiljet – nep bankbiljet ( of een gewoon blad papier) – Lugol indicator
- Thema: biochemie
- Tijd:20 min
- Begrippen: zetmeel – identificatiereactie
2.5.21. Dilawattes

- Info: Hoe kunnen we op water lopen? Wanneer we maïzena met water mengen, krijgen we een suspensie. De vaste deeltjes maïzena en het vloeibare water zijn door elkaar gemengd. Het is dus geen oplossing. Het gevormde mengsel is een niet-Newtoniaanse vloeistof:Wanneer er druk wordt uitgevoerd op het mengsel, worden de maïzena-deeltjes tegen elkaar aan geduwd. Hierdoor kan het water niet goed tussen de deeltjes door stromen. Indien er geen druk wordt uitgevoerd kan het water gewoon tussen de maïzena-deeltjes door stromen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Maïzena – Water
- Thema: biochemie
- Tijd:20 min
- Begrippen: zetmeel – niet-Newtoniaanse vloeistof
2.5.22. Water aantonen met zetmeel, dijood en aceton

- Info: Hoe kan je water aantonen zonder kobaltdichloride papiertjes? Door het onttrekken van water wordt de reactive eveneens naar links getrokken. Hierdoor ontstaat terug de bruine kleur van het dijood. Water toevoer leidt tot het vormen van het complex.Water kan ook aangetoond worden met een zetmeel dijood papiertje. Als er water opkomt kleurt het paars blauw. Als er aceton bij komt kleurt het terug bruin. Dit stelt dus dat aceton water onttrekt aan het papiertje.
- Moeilijkheid: eenvoudig
- Chemische stoffen: aceton – zetmeeloplossing – dijoodoplossing
- Thema: biochemie
- Tijd:20 min
- Begrippen: zetmeel – identificatie
2.5.23.Jood-Bloem

- Info: Wat gebeurt er als we lugol en zetmeel in dezelfde afgesloten ruimte brengen? In de afgesloten ruimte zal het voorwerp/de plaats waar zetmeel aanwezig is blauw worden. Doordat in lugol het dijood een goede vluchtigheid heeft stijgt deze. Deze komt dan geleidelijk in aanraking met het zetmeel dat op de tissue zit. Als deze 2 stoffen in aanraking komen met elkaar verkleurt het lugol blauw. Ze vormen een blauw zetmeel-jodiumcomplex.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Zetmeel – Lugoloplossing
- Thema: biochemie
- Tijd:20 min
- Begrippen: zetmeel – identificatie
2.5.24. Egyptische nacht

- Info:Door isobetadine toe te voegen voeg je dijood (indicator voor zetmeel) toe aan de maatbeker. De vitamine C oplossing reduceert dijood in jodide-ionen.Bij het toevoegen van de zetmeeloplossing zal de inhoud van de maatbeker dus niet meteen donkerblauw kleuren. Dat gebeurt pas wanneer waterstofperoxide reageert met de gereduceerde jodide-ionen ter vorming van water en dijood (trage reactie). Hierbij komt zuurstof (onder de vorm van water) vrij en zal stillaan stijgen naar het oppervlak.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Isobetadine – Huishoudazijn – Waterstofperoxide 30% – Zetmeeloplossing 1% – Vitamine C oplossing 5%
- Thema: biochemie – reactiesnelheid
- Tijd:20 min
- Begrippen: zetmeel – klokreactie
2.5.25. Originele stempel

- Info:Hoe kunnen we een aardappel als stempel gebruiken als er geen inkt aanwezig is? Het zetmeel van de aardappel kan reageren met het dijodide aanwezig in de Iso-Betadine ter vorming van blauwe zetmeelcomplexen met ingesloten jodide-ionen die vervolgens als inkt kan gebruikt worden.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Aardappel – Iso-betadine
- Thema: biochemie
- Tijd: 10 min
- Begrippen: zetmeel – identificatie
2.5.26. Maak behanglijm met zetmeel

- Info:Hoe kun je behangplaksel maken van zetmeel? De lange, spiraalvormige zetmeelmoleculen worden in heet water afgebroken, maar netwerken snel met elkaar of met de sucrosemoleculen . Door de vele verknoopte bindingen vormt zich een stroperige massa – pasta.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 30 g sucrose – 40 g zetmeel – 100 ml water
- Thema: biochemie
- Tijd: 10 min
- Begrippen: zetmeel – intermoleculaire krachten
2.5.27. Bewijs van zetmeel in wit brood

- Info:Hoe kun je de zetmeel van het meel in witbrood bewijzen?
- De jodium- kaliumjodideoplossing valt onder andere uiteen in I – ionen. Deze worden opgeslagen in de zetmeelmoleculen. Het resulterende jodium- zetmeelcomplex heeft een diepblauwe kleur.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 2 boterhammen witbrood – 2 druppels lugol
- Thema: biochemie
- Tijd: 10 min
- Begrippen: zetmeel – identificatie
2.5.28. Meelexplosie

- Info: Wat als meel (of een ander poedervormig organisch materiaal) wordt uiteengeblazen en aangestoken? Door in de metalen bus te blazen, wordt het brandbare organische materiaal opgedwarreld. Dit resulteert in een enorme toename in oppervlakte. Grote hoeveelheden lucht bereiken elk poederdeeltje. Die poederdeeltjes die in de buurt van de kaarsvlam worden opgeblazen, branden plotseling. De vlam verspreidt zich door de rest van het opgeblazen materiaal.De jodium- kaliumjodideoplossing valt onder andere uiteen in I – ionen. Deze worden opgeslagen in de zetmeelmoleculen. Het resulterende jodium- zetmeelcomplex heeft een diepblauwe kleur.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 5 g meel – 5 g koffiepoeder – 5 g cacaopoeder – 5 g druivensuiker – 1 kaars
- Thema: biochemie
- Tijd: 20 min
- Begrippen: zetmeel – verbrandingsreactie
2.5.29. Winnen van zetmeel

- Info: Hoe kun je zetmeel bekomen uit aardappelen? De aardappelen schillen en in kleine stukjes snijden. Breng deze in water in een erlenmeyer. Sluit met de stof en schut goed. Giet het mengsel door een linnen doek. Druk de aardappelmoes wat samen. Zet het filtraat apart en laat de neerslag wat bezinken. Decanteer de bovenstaande vloeistof af en laat het laatste deel water uitdampen door drogen aan de lucht.
- Moeilijkheid: eenvoudig
- Chemische stoffen: aardappelen
- Thema: biochemie
- Tijd: 20 min
- Begrippen: zetmeel – verbrandingsreactie
2.5.30. Zetmeel aantonen

- Info: Hoe kun je zetmeel aantonen? Eerst ontstaat er een blauw-violette tot blauw-zwarte kleur. Deze kleur lijft niet bestaan door verwarming. Bij terug afkoelen wordt de kleur terug gevormd.
- Moeilijkheid: eenvoudig
- Chemische stoffen: zetmeel – lugoloplossing
- Thema: biochemie
- Tijd: 20 min
- Begrippen: zetmeel – identificatiereactie
2.5.31. Samenstelling van zetmeel

- Info: Uit welke bestanddelen is zetmeel opgebouwd? Het zetmeel bevat een in water oplosbaar deel het amylose en een onoplosbaar deel amylopectine. Het amylosedeel wordt blauw en het amylopectine wordt paars met een lugoloplossing.
- Moeilijkheid: eenvoudig
- Chemische stoffen: zetmeel – lugoloplossing
- Thema: biochemie
- Tijd: 20 min
- Begrippen: zetmeel – identificatiereactie
2.5.32. Hydrolyse van zetmeel
- Info: Hoe kun je zetmeel hydrolyseren? De zetmeeloplossing wordt blauw, paarsblauw, bruin en uiteindelijk geel. Na de neutralisatie worden de glucosesticks groen. Het onderzoek met seleendioxide is negatief. Door hydrolyse is zetmeel bijgevolg omgezet tot glucose.
- Moeilijkheid: eenvoudig
- Chemische stoffen: zetmeel – lugoloplossing – zoutzuuroplossing – natriumhydroxide oplossing – seleendioxide
- Thema: biochemie
- Tijd: 20 min
- Begrippen: zetmeel -hydrolyse
2.6. Glycogeen
2.6.1. Isoleren van glycogeen

- Info: Hoe kun je glycogeen bekomen? Door een extractie uit te voeren van glycogeen uit lever
- Moeilijkheid: eenvoudig
- Chemische stoffen: lever – ethanol – kaliumhydroxide- ethanol
- Thema: biochemie
- Tijd: 20 min
- Begrippen: glycogeen – isolatie
2.6.2. Onderzoek en hydrolyse van glycogeen

- Info: Hoe is glycogeen opgebouwd?Glycogeen heeft een gelijkaardige structuur als amylopectine. Het bezit kleinere vertakkingen. Hierdoor gebeurt er verkleuring met de lugoloplossing tot roodbruin en niet tot roodpaars zoals bij amylopectine. Met het benedictreagens wordt geen positieve test verkregen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: lugol – clinistix – glycogeenoplossing – bendedict reagens
- Thema: biochemie
- Tijd: 20 min
- Begrippen: glycogeen – hydrolyse
3. Vetten
3.1. Identificatie en eigenschappen van vetten
- Info: Hoe is vet aan te tonen? Doe een druppel olie en een druppel water op papier. Hou vervolgens het blad naar het licht
en bekijk waar de stalen werden aangebracht. - Moeilijkheid: eenvoudig
- Chemische stoffen: olie – papier – water
- Thema: biochemie
- Tijd: 10 min
- Begrippen: vetten – identificatie
3.2. Ijsklontje in olie

- Info: Hoe is vet aan te tonen? Doe een druppel olie en een druppel water op papier. Hou vervolgens het blad naar het licht
en bekijk waar de stalen werden aangebracht. - Moeilijkheid: eenvoudig
- Chemische stoffen: ijsklontje – glas slaolie
- Thema: biochemie
- Tijd: 10 min
- Begrippen: vetten – massadichtheid
3.3. Lipgloss

- Info: Kunnen we lipgloss maken met producten uit de keuken? Het belangrijkste ingrediënt voor lipgloss is honing. Honing is een vochtinbrenger. Het zorgt ervoor dat er meer vocht uit je lichaam naar je lippen gaat. Ook zorgt honing ervoor dat je lippen glanzen en beschermd zijn tegen de zon. En honing smaakt natuurlijk lekker! De amandelolie ligt als een laagje op je lippen en zorgt ervoor dat er geen vocht uit je lippen verdampt. Zo kun je geen droge lippen meer krijgen. De amandelolie en de honing maken samen met de vaseline je lippen glad en glanzend. De frambozen zorgen voor een lekkere smaak en een beetje kleur op je lippen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Amandelolie (te koop bij de drogist) – 10 frambozen – Honing – Gezuiverde vaseline (te koop bij de drogist)
- Thema: biochemie
- Tijd: 10 min
- Begrippen: vetten – polair/apolair
3.4. Onzichtbaar glas

- Info: Op welke manier kunnen we glas onzichtbaar maken? De brekingsindex van de olie sluit heel nauw aan bij de brekingsindex van de roerstaaf. Wanneer we de juiste invalshoek vinden lijkt het glas onzichtbaar in de laag olie maar zichtbaar in de laag water.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Zonnebloemolie/Arachideolie – Water
- Thema: biochemie – eigenschappen van stoffen
- Tijd: 10 min
- Begrippen: vetten – brekingsindex
3.5. Polyester uit citroenzuur en ricinusolie

- Info: Kunnen we met behulp van ricinusolie en citroenzuur polyester maken? Het is mogelijk om uit citroenzuur en ricinusolie polyester te maken
- Moeilijkheid: eenvoudig
- Chemische stoffen: Ricinusolie – citroenzuur
- Thema: biochemie – kunststoffen
- Tijd: 30 min
- Begrippen: vetten – polycondensatiereactie

- Info: Als de oliezuurlaag precies 1 molecuul dik is, kun je op grond van je metingen de grootte van een oliezuur molecuul berekenen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: benzine of petroleumether – oliezuur – peper
- Thema: biochemie
- Tijd: 30 min
- Begrippen: vetten – grootte van een molecule
3.7. Zelf zeep maken

- Info: Wanneer men natriumhydroxide samen doet met vetten ontstaat er een ester met afsplitsing van watermoleculen. Deze reactie noemt men een verzepingsreactie.
- Moeilijkheid: eenvoudig
- Chemische stoffen: natriumhydroxide ( 9 g) – arachideolie
- Thema: biochemie
- Tijd: 30 min
- Begrippen: vetten – bereiding zeep – verzeping

- Info: Hoe werkt een emulgator in chocolade?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Kookolie – water – paprikapoeder – lecithine
- Thema: biochemie – soorten mengsels
- Tijd: 30 min
- Begrippen: vetten – emulgator
3.10. Maken van biodiesel

- Info: De bereiding van diesel is een zgn transesterificatiereactie, een bewerking waarbij de alkoxygroep van een ester wordt vervangen door die van een alcohol. De reactie is schematisch weergegeven in nevenstaande figuur. Men voegt loog aan het mengsel om een zgn methoxide of ethoxide te maken (CH3O–Na+). Het methoxide of ethoxide reageert vervolgens met de estergroep van het triglycderide. De overmaat aan methanol/ethanol die in het mengsel aanwezig is zorgt ervoor dat de reactie richting biodiesel verloopt.
- Moeilijkheid: eenvoudig
- Chemische stoffen: zonnebloemolie – methanol – natronloog
- Thema: biochemie -organische stoffen
- Tijd: 30 min
- Begrippen: vetten – mengsels
3.11. Olie op water,water op olie

- Info: Zal het water boven blijven? De oplossingen hebben een verschillende dichtheid. De lichtere vloeistoffen bewegen naar boven en de zware naar beneden en daarom beweegt in dit geval de olie naar boven en het water naar beneden
- Moeilijkheid: eenvoudig
- Chemische stoffen: olie – water
- Thema: biochemie -organische stoffen
- Tijd: 30 min
- Begrippen: vetten – massadichtheid
3.12. Zeep maken

- Info: Wanneer men natriumhydroxide samen doet met vetten ontstaat er een ester met afsplitsing van watermoleculen. Deze reactie noemt men een verzepingsreactie.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 8 ml soda – 10 g plantaardige olie – 100 ml water – 20 g NaCl
- Thema: biochemie
- Tijd: 30 min
- Begrippen: vetten – bereiding zeep – verzeping
4. Voeding
4.1. Aardappelen
4.1.1. Aardappelkanon

- Info: Hoever kun je een aardappel schieten met een zelfgemaakt aardappelkanon? In de meeste spuitbussen is butaan het drijfgas. De reactie die optreedt is dus de verbranding van butaan.De afstand die we kunnen bereiken met het aardappelkanon is voornamelijk afhankelijk van de hoeveelheid gas dat we gebruiken, ook spelen de hoek waaronder we schieten en in mindere mate de aard van het gas een rol.
- Moeilijkheid: gemiddeld
- Chemische stoffen: koperdraad – (laad)stok – aardappels – alkaan
- Thema: organische stoffen – organische reacties – redoxreactie – biochemie
- Tijd: 30 min
- Begrippen:alkanen – verbrandingsreactie
4.1.2. Biologische plastic

- Info: Hoe maak je een biologisch afbreekbare plastic van aardappelen? Wanneer het water met daarin de zetmeelkorrels wordt verwarmt, nemen de amylose moleculen meer water op. Hierdoor zwellen de zetmeelkorrels en breken de onderling gevormde waterstofbruggen, naarmate de suspensie opzwelt en stroperiger wordt nemen ook de amylpectine moleculen water op.
- Moeilijkheid: gemiddeld
- Chemische stoffen:8 à 9 grote aardappelen
- Thema: biochemie – kunststoffen
- Tijd: 30 min
- Begrippen: bioplastics
4.1.3. Elektrolyse in aardappelen

- Info: Wat gebeurt er als we een aardappel onder spanning plaatsen? Aan de koperdraad in de aardappel waarmee de positieve pool verbonden is, is er een duidelijke turquoise kleur te herkennen. Dit duidt op aanwezigheid van koperionen. Cu wordt tot Cu2+ ionen gereduceerd. Deze vormen samen met de anionen van uit de aardappel een blauw koperzout.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Magnesiumstaaf – Aardappel – Afwasmiddeloplossing – Indicatorpapier – fenolftaleïne-oplossing 0,05%
- Thema: biochemie – redoxreacties
- Tijd: 30 min
- Begrippen: elektrolyse
4.1.4. Rietje door aardappel

- Info: Hoe kan je een rietje door een aardappel steken, zonder het te breken? Als je je duim op het uiteinde van het rietje zet of het rietje dicht knijpt, hou je de lucht binnenin tegen. De luchtmoleculen zijn als het ware gevangen waardoor het rietje sterker wordt. Doordat het rietje op deze manier sterker wordt, zal het niet vervormen. Indien dit niet wordt gedaan, wordt de lucht simpelweg eruit geduwd.
- Moeilijkheid: gemiddeld
- Chemische stoffen: enkele aardappelen – enkele rietjes
- Thema: biochemie
- Tijd: 30 min
- Begrippen: luchtdruk – fysica
4.1.5. Extractie van vet uit chips

- Info: Hoe kunnen we vet van chips scheiden? Hoe kunnen we het vetgehalte in chips bepalen? Door middel van extractie kunnen we het vet van de chips scheiden. Hiervoor maken we gebruik van het Soxhletapparaat.
- Moeilijkheid: gemiddeld
- Chemische stoffen: paprikachips – diethylether
- Thema: scheidingstechnieken – biochemie
- Tijd: 60 min
- Begrippen: extractie
4.1.6. Aardappelbatterij

- Info: Hoe kunnen we met aardappelen elektrische energie vormen? In de aardappel-batterij wordt chemische energie omgezet naar elektrische energie door een spontane overdracht van elektronen.
In dit geval reageert het zink van de nagel met het koper van de koperdraad. - Moeilijkheid: eenvoudig
- Chemische stoffen: 12 reepjes zink / magensium – 12 reepjes koper – 24 paperclips – 12 aardappelen – dun koperdraad
- Thema: chemische reacties – energetische aspecten – redoxreactie – biochemie
- Tijd: 20 min
- Begrippen: exo-energetische reacties – galvanische cel
4.1.7. Aardappelbatterij versie2
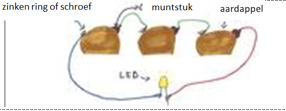
- Info: Hoe kunnen we met aardappelen elektrische energie vormen? In de aardappel-batterij wordt chemische energie omgezet naar elektrische energie door een spontane overdracht van elektronen.
In dit geval reageert het zink van de nagel met het koper van de koperdraad. - Moeilijkheid: eenvoudig
- Chemische stoffen: 3 aardappels – 3 muntstukken – 3 schroeven of ringen van zink – 4 kabels – 1 LED-lampje (zonder serieweerstand)
- Thema: chemische reacties – energetische aspecten – redoxreactie – biochemie
- Tijd: 20 min
- Begrippen: exo-energetische reacties – galvanische cel
4.1.8. Zetmeelfolie

- Info: Zetmeel is een voorbeeld van een polymeer van natuurlijke oorsprong. Deze polymeren worden direct geëxtraheerd en gewonnen uit diverse graangewassen (bijvoorbeeld tarwe en maïs), knolgewassen (bijvoorbeeld aardappels) en wortels.Uit microscopisch onderzoek is af te leiden dat de kern van de zetmeelkorrel bestaat uit onvertakte polymeren, die amylose worden genoemd. Amylose zijn ketens van glucosemoleculen.De vertakte polymeren in het zetmeel worden amylopectine genoemd, deze amylopectine wordt verbonden.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Glycerol – HCl-oplossing (0.1 mol/l) – NaOH-oplossing (0.1 mol/l)
- Thema:kunststoffen – biochemie
- Tijd: 20 min
- Begrippen:bioplastics
4.1.9. Zetmeeltest

- Info: Hoe kunnen we de aanwezigheid van zetmeel in aardappelen aantonen? Identificatie met een dijoodoplossing
- Moeilijkheid: gemiddeld
- Chemische stoffen: 1 rauwe aardappel – dijoodoplossing
- Thema: chemische reacties – biochemie
- Tijd:35 min
- Begrippen: identificatie
4.1.10. Elektrolyse in een aardappel

- Info:Hoe kunnen we zowel de aardappel gebruiken om een batterij als een elektrolyse cel te maken?
- Moeilijkheid: gemiddeld
- Chemische stoffen: magnesiumstaaf – aardappel – afwasmiddeloplossing (1/4de verdund) – indicatorpapier – FFT-oplossing
- Thema: redoxreacties – biochemie
- Tijd: 20 min
- Begrippen: elektrolyse
4.1.11. Katalase in een aardappel
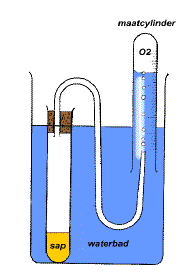
- Info: Hoe kunnen we het enzym katalase in een aardappel aantonen? In de aardappelen zit het enzym katalase. De katalase werkt als enzym/katalysator voor de ontleding van waterstofperoxide in water en zuurstof. Zonder dit enzym kan waterstofperoxide zich niet zomaar splitsen.
- Moeilijkheid: gemiddeld
- Chemische stoffen: aardappel – waterstofperoxide 5%
- Thema: biochemie
- Tijd: 20 min
- Begrippen: enzymen
4.1.12. Onzichtbare inkt met aardappel

- Info: Hoe kunnen we op papier een boodschap schrijven zonder inkt te gebruiken? Door middel van het zetmeel in een aardappel boven een warmtebron te houden zodat de koolstof in het zetmeel omgezet kan worden tot roet wordt de tekst zichtbaar.
Waar er aardappelsap was, verschijnt na het opwarmen een lichtbruine kleur. - Moeilijkheid: gemiddeld
- Chemische stoffen: 1 aardappel
- Thema: biochemie
- Tijd: 20 min
- Begrippen: identificatie zetmeel
4.1.13. Aardappelen in een vlam

- Info: Wat zien we als we een aardappel of chips in een vlam houden?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Aardappel – Chips
- Thema: biochemie
- Tijd: 20 min
- Begrippen: verbrandingsreactie
4.1.14. Originele stempel

- Info:Hoe kunnen we een aardappel als stempel gebruiken als er geen inkt aanwezig is? Het zetmeel van de aardappel kan reageren met het dijodide aanwezig in de Iso-Betadine ter vorming van blauwe zetmeelcomplexen met ingesloten jodide-ionen die vervolgens als inkt kan gebruikt worden.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Aardappel – Iso-betadine
- Thema: biochemie
- Tijd: 10 min
- Begrippen: zetmeel – identificatie
4.2. Algemeen
4.2.1. Kettingreactie met voedingsmiddelen

- Info:Een kettingreactie is een keten van reacties waarbij een stof onstaat in de eerste reactie reageert in de volgende reactie. Tijdens deze kettingreactie vinden vijf verschillende reacties plaats met voedingsmiddelen
- Moeilijkheid: gemiddeld
- Chemische stoffen: Rodekoolsap (voor het maken van rodekoolsap kook je de groente 10 minuten in een beetje water) – Maïzena (zetmeel van maïs) – Water – Ammonia (VOORZICHTIG! Irriteert ogen en neus) – Schoonmaakazijn – Zuiveringszout (verkrijgbaar bij de drogist) – Betadine (jodium) – Vitamine C-bruistablet
- Thema: chemische reacties – complexreactie – redoxreactie – biochemie
- Tijd:20 min
- Begrippen: stofveranderingen – kleurreacties
4.3. Dranken
4.3.1. Alcoholhoudende dranken
4.3.1.1. Aantonen van methanol in dranken

- Info: In de KMnO4 oplossing wordt methanol geoxideerd tot formaldehyde. Formaldehyde reageert met de Schiff’s base tot een paarse kleur. Deze methanol is terug te vinden in brandewijnen, niet in graanjenever.Een overmaat KMnO4 wordt toegevoegd om methanol te oxideren. De oxaalzuuroplossing reduceert deze overmaat nadien.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Schiff’s reagens:Fuchsine-oplossing (Schiff’s reagens):0,1 g fuchsine opgelost in 300 ml water, verzadigen met SO2 (Na2SO3, HCl) tot de oplossing ontkleurt. Een mespunt salicylzuur maakt de oplossing langer houdbaar – SO2 bron: 1 g Natriumsulfiet toevoegen en oplossen.Nadien 5 ml geconcentreerd HCl toevoegen. – Methanol – Ethanol – KMnO4 – H3PO4 – Oxaalzuur – Zwavelzuur
- Thema: organische stoffen – alcohol – redoxreactie – biochemie
- Tijd: 20 min
- Begrippen: methanol -oxidans
4.3.1.2. Afbuiging van tequila

- Info: Wat gebeurt er als een opgewreven staaf in de buurt komt van tequila? Als de pvc buis wordt opgewreven krijgt deze een lading. In stoffen die aangetrokken worden door de buis zijn ook ladingen aanwezig. Stoffen die ladingen dragen zijn polaire stoffen.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Tequila
- Thema: bouw van atomen – biochemie
- Tijd: 10 min
- Begrippen: atoommodel van Thomson
4.3.1.3. Alcoholcement

- Info: Wat gebeurt er als we eiwitten behandelen met zuren? Zowel cola als azijn bevatten zuren. Cola bevat fosforzuur en azijn bestaat natuurlijk uit een lage concentratie azijnzuur. Het zuur zorgt voor de denaturatie van de eiwitten die we terugvinden in de Baileys.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Azijn – Cola – Baileys / koffiemelk/ cream
- Thema: biochemie
- Tijd: 15 min
- Begrippen: eiwitten – neerslagreactie – denaturatie
4.3.1.4. Alcoholgehalte bepalen van jenever

- Info: Bij welk alcoholpercentage kun je likeur laten ontbranden? Wanneer we in het donker werken, zien we dat zelfs bij alcoholpercentages van 30% à 40% het wattenstaafje vuur (vonken) vat. Dit betekent dat we likeuren vanaf 30% kunnen laten ontbranden.We testen dit met een kleine hoeveelheid rum.
- Moeilijkheid: gemiddeld
- Chemische stoffen: 98% alcoholoplossing (in de apotheek te verkrijgen) – rum
- Thema: chemisch rekenen – biochemie
- Tijd: 20 min
- Begrippen: concentratie -verbranding
4.3.1.5. Bepalen van alcoholgehalte in alcopops

- Info: Hoeveel alcohol zit er in een alcopop? De alcopop bevat inderdaad iets van een 10 procent alcohol. De destillatie is vrij eenvoudig uit te voeren
- Moeilijkheid: gemiddeld
- Chemische stoffen:Alcoholpop
- Thema: chemisch rekenen – biochemie
- Tijd: 20 min
- Begrippen: concentratie -verbranding
4.3.1.6. Chemisch bier

- Info: Hoe kunnen we bier (Duvel) op een chemische wijze nabootsen? Voer redoxreactie uit met vorming van djood
- Moeilijkheid:moeilijk
- Chemische stoffen: KIO3 (kaliumjodaat) – CH3CH2OH (ethanol) – H2SO4 (zwavelzuur) – Na2SO3 (dinatriumsulfiet) – kleurloos detergent
- Thema: enkelvoudige stoffen – reactiesnelheid – redoxreacties – biochemie
- Tijd:30 min
- Begrippen: enkelvoudige stoffen – reactiesnelheid
4.3.1.7. Destillatie van wijn met alambic

- Info: Maak volgende opstelling van tekening (zie foto hierboven) .Breng in de kolf het zeewater en warm traag op.Indien het water bijna verdwenen is uit de kolf wordt gestopt met de verhitting.
- Moeilijkheid: eenvoudig
- Chemische stoffen: zout – water -alambic
- Thema: scheidingstechnieken – biochemie
- Tijd:15 min
- Begrippen: destillatie – verschil in kookpunt
4.3.1.8. Destillatie met gewoon glaswerk van wijn
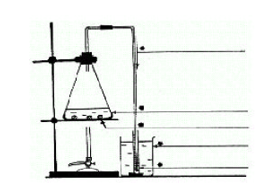
- Info: Destillatie van wijn zonder dat gebruik wordt gemaakt van een liebigkoeler
- Moeilijkheid: eenvoudig
- Chemische stoffen: 50 ml wijn
- Thema: scheidingstechnieken – biochemie
- Tijd:15 min
- Begrippen: destillatie – verschil in kookpunt
4.3.1.9. Destillatie van wijn met de Vigreuxkolom

- Info: Destillatie van wijn waarbij gebruik wordt gemaakt van een vigreuxkolom
- Moeilijkheid: gemiddeld
- Chemische stoffen: 50 ml wijn – kookkolf – vigreuxkolom
- Thema: scheidingstechnieken – biochemie
- Tijd:15 min
- Begrippen: destillatie – verschil in kookpunt
4.3.1.10. Destillatie met minilabor van wijn

- Info: Destillatie van wijn waarbij gebruik wordt gemaakt van minilabormateriaal
- Moeilijkheid: gemiddeld
- Chemische stoffen: 50 ml wijn – minilabor
- Thema: scheidingstechnieken – biochemie
- Tijd:15 min
- Begrippen: destillatie – verschil in kookpunt
4.3.1.11. Destillatie van wijn met geslepen glaswerk
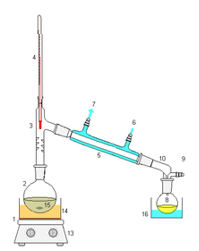
- Info: Destillatie van wijn waarbij gebruik wordt gemaakt van geslepen glaswerk. Meet met de piknometer de dichtheid en bepaal hieruit het volume alcohol.
- Moeilijkheid: gemiddeld
- Chemische stoffen: aardolie
- Thema: scheidingstechnieken – biochemie
- Tijd:15 min
- Begrippen: destillatie – verschil in kookpunt
4.3.1.12. Ontkleuren van wijn door adsorptie

- Info: Door toevoeging van de actieve kool aan de wijn wordt deze zeer donker. Giet men het heterogeen mengsel over de filter, blijft een zwart residu achter en is het filtraat lichter van kleur. De rode kleur is uit het filtraat verdwenen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: actieve kool eventueel zelf gemaakt – wijn
- Thema: scheidingstechnieken – biochemie
- Tijd: 10 min
- Begrippen: adsorptie – norit
4.3.1.13. Rode wijn als indicator

- Info: Hoe kunnen we huishoudmiddeltjes als zuurbase-indicator gebruiken? De indicatorstof in de wijn zijn de anthocyanen. Dit zijn kleurstoffen die in plantencellen voorkomen, zoals die van druiven. Men heeft al meer dan 500 soorten anthocyanen kunnen isoleren uit planten. Deze zijn allemaal gelijkaardig opgebouwd.
- Moeilijkheid: eenvoudig
- Chemische stoffen: actieve kool eventueel zelf gemaakt – wijn
- Thema: neutralisatiereactie- biochemie
- Tijd: 10 min
- Begrippen: titraties
4.3.1.14. Zuurgehalte bepalen in wijn door titratie

- Info: Hoe kun je experimenteel het totale zuurgehalte bepalen in wijn? Bij deze proef gaan we de base NaOH toevoegen aan een zure oplossing van wijn. Nadat we enkele ml NaOH hebben toegevoegd zien we een lichte kleurverandering van rood naar groen. Deze kleuromslag gebeurt door de anthocyanen in de wijn.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Wijn – Natriumhydroxide 0,1 mol/l
- Thema: neutralisatiereactie- biochemie
- Tijd: 30 min
- Begrippen: titraties
4.3.1.15. Wijnsoorten maken

- Info: Hoe kun je verschillende wijnsoorten maken?
- Moeilijkheid: gemiddeld
- Chemische stoffen: Natriumhydroxide oplossing (1mol/L) – Zwavelzuur (40%) – Ijzer(III)chloride – Ammoniumthiocyanaat – Fenolftaleine-oplossing – Citroenzuur – Heptaan – Kaliumhexacyanoferraat (II) K4[Fe(CN)6] – Natriumwaterstofcarbonaat
- Thema: neutralisatiereactie- redoxreacties – biochemie – chemisch evenwicht
- Tijd: 30 min
- Begrippen:complexreacties
4.3.1.16. Water kleuren met wijn

- Info: Indien we een glas wijn en een glas water hebben, hoe kunnen we dan dit water kleuren met de wijn, zonder de glazen aan te raken? De wet van communicerende vaten stelt dat wanneer twee vaten met elkaar verbonden zijn, deze na verloop van tijd gelijk zullen zijn in niveau.In dit geval wordt de wijn overgedragen door het touw. Dit is namelijk opgebouwd uit cellulose, wat gemakkelijk water opneemt.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Rode wijn – Water
- Thema: neutralisatiereactie- redoxreacties – biochemie – chemisch evenwicht
- Tijd: 30 min
- Begrippen: capillariteit
4.3.1.17. Baileys en tonic

- Info: Tonic heeft een pH van rond de 2,5 en Cola rond de 3 en zijn dus in staat om de pH-waarde van de emulsie onder de 4,6 te brengen, waardoor de emulsie opbreekt en gaat schiften
- Moeilijkheid: eenvoudig
- Chemische stoffen: 100 ml Baileys – 100 ml tonic
- Thema: biochemie
- Tijd: 15 min
- Begrippen: eiwitten – neerslagreactie – denaturatie
4.3.1.18. Brandende doek met wodka

- Info: Hoe kan je een (zak)doek in brand steken zonder dat het verbrandt? In wodka is ethanol aanwezig die een verbrandingsreactie ondergaat. In de verbrandingsreactie gaat de ethanol met O2. De zakdoek brandt niet op omdat er in wodka een hoog gehalte aan water aanwezig is dat lang genoeg de warmte kan opvangen van de verbrandingsreactie. Hierdoor vliegt de zakdoek niet in brand.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Wodka, 50% alcoholpercentage of meer
- Thema: biochemie
- Tijd: 15 min
- Begrippen: verbrandingsreactie – alcoholen
4.3.1.19. Coldpack maken met wodka

- Info: Hoe kan je met alledaagse producten een coldpack maken? Alcohol heeft een smeltpunt van -114°C. Dit smeltpunt is lagen dan het smeltpunt van water, dit is 0°C. Het wodka-watermengsel heeft een lager smeltpunt dan water waardoor men een coldpack kan ontwikkelen die nog vloeibaar is en dus eenvoudiger is te plaatsen op het lichaam. Het smelttraject van vodka start rond -27°C. Bij een gewone diepvries is dus een gel te maken met vodka die nog vloeibaar blijft.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Wodka, 50% alcoholpercentage of meer
- Thema: biochemie
- Tijd: 15 min
- Begrippen: oploswarmte
4.3.1.20. Pulserend glas

- Info: Hoe kunnen we een schuimwijn maken die blijft schuimen? In het experiment blijft het vrijgekomen zuurstof in oplossing. Als de oplossing in een verzadigde toestand het zuurstofgas bezit, schuimt het plotseling en komt een grote hoeveelheid vrij. Het verzadigingspunt wordt nu niet meer bereikt. Indien een nieuwe oververzadiging wordt bereikt komt terug gas vrij.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Koper(II)chloride – Zoutzuur (2mol/l) – Waterstofperoxide (10%)
- Thema: anorganische stoffen – energetische aspecten – chemisch evenwicht – biochemie
- Tijd: 20 min
- Begrippen: peroxiden – katalysator – oscillerende reactie
4.3.1.21. Vuur in een fles

- Info: Hoe kunnen we veilig vuur in een kunststoffen fles maken? Door de verbranding in de fles van ethanoldampen kan je voor een korte tijd een vlam in een fles bewaren.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Sterk alcoholische drank +40%
- Thema: biochemie
- Tijd: 20 min
- Begrippen:verbrandingsreactie
4.3.1.22. Troebel komt en gaat met ouzo

- Info: Hoe kan je een emulsie omzetten naar een oplossing? Alcohol is minder polair dan water waardoor de anijs opgelost kan worden in de drank. Daardoor is de oplossing alcohol (veel alcohol )-anijs zeer helder. Door toevoeging van een overmaat aan water (die een grotere polariteit heeft) kan het anijs niet meer oplossen en hierdoor wordt het uitzicht troebel.
- Moeilijkheid: eenvoudig
- Chemische stoffen: ouzo/raki/anijs, – afwasmiddel/detergent
- Thema: biochemie
- Tijd: 20 min
- Begrippen: emulsie – micellen
4.3.1.23. Zoek de samenstelling van chemisch bier

- Info: Hoe kunnen we bier (Duvel) op een chemische wijze nabootsen? Voer redoxreactie uit met vorming van djood
- Moeilijkheid:moeilijk
- Chemische stoffen: KIO3 (kaliumjodaat) – CH3CH2OH (ethanol) – H2SO4 (zwavelzuur) – Na2SO3 (dinatriumsulfiet) – kleurloos detergent
- Thema: enkelvoudige stoffen – reactiesnelheid – redoxreacties – biochemie
- Tijd:30 min
- Begrippen: enkelvoudige stoffen – reactiesnelheid
4.3.1.24. Verbranding van verschillende concentraties vodka

- Info: Vanaf welke concentratie is wodka niet meer brandbaar? Als de concentratie daalt tot onder 50% alcohol (bij kamertemperatuur) dan zal de vloeistof niet meer ontbranden omdat alle warmte die vrijkomt meteen wordt geabsorbeerd door het water en de reactie stopt.
- Moeilijkheid: eenvoudig
- Chemische stoffen: wodka 60%, – water
- Thema: enkelvoudige stoffen – reactiesnelheid – redoxreacties – biochemie
- Tijd: 20 min
- Begrippen: verbrandingsreactie
4.3.1.25. Bloedcocktail

- Info: Hoe kunnen we ijs maken met bloed?.Het waterstofperoxide ontleedt zich in water en zuurstof. De vrijgekomen zuurstof heeft een sterk oxiderende kracht. De eiwitten in het bloed houden die zuurstof vast. Hierdoor krijgen we schuim.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Bloed – Waterstofperoxide 30%
- Thema: biochemie
- Tijd: 15 min
- Begrippen: eiwitten – schuimvorming – enzymen
4.3.1.26. Groenten ontkleuren met vodka

- Info: Hoe kan je groenten ontkleuren met Wodka? De bladgroenkorrels lossen op in de alcohol en worden uit het blad verwijderd door extractie.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Wodka (minstens 50%), – groente met bladgroenkorrels
- Thema: biochemie
- Tijd: 15 min
- Begrippen: ontkleuring
4.3.1.27. Verandering water in wijn

- Info: Hoe kan je groenten ontkleuren met Wodka? De bladgroenkorrels lossen op in de alcohol en worden uit het blad verwijderd door extractie.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Na2CO3 – Water – Fenolftaleïne 0,05% – zoutzuur
- Thema: biochemie – neutralisatiereactie
- Tijd: 25 min
- Begrippen: pH-indicator
4.3.1.28. Wijn maken

- Info: Hoe kun je zelf wijn maken? De enzymen uit de gist zetten de suiker om in ethanol . Bij een alcoholpercentage van ongeveer 15% gaan de gisten dood.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 1 l perensap – 20 ml wijngist – 200 g sucrose
- Thema: biochemie – neutralisatiereactie
- Tijd: 25 min
- Begrippen: vergisting
4.3.2. Algemeen
4.3.2.1. Blik geeft stroom

- Info: Hoe kan een blikje energie geven? Door een galvanische cel te bouwen waarbij er een reactie optreedt met het aluminium van dit blikje.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 2mol/l NaCl – 2mol/l KNO3 oplossing – blikje bier
- Thema: chemische reacties – energetische aspecten – redoxreactie – biochemie
- Tijd: 20 min
- Begrippen: exo-energetische reacties – galvanische cel
4.3.2.2. Maak met eenzelfde oplossing de meeste dranken

- Info: Maak een oplossing van 500ml 1M H2SO4 met 0.5 g watervrije ijzertrichloride. De oplossing is praktisch kleurloos. Neem nu verschillende glazen voor porto, sherry, wijn, melk, water, champagne, cola, curacao
- Moeilijkheid: gemiddeld
- Chemische stoffen: 500 ml 1 mol/L H2SO4 met 0,5g watervrije ijzertrichloride – ammoniomthiocyanaat – ijzetrichloride – loodnitraat – NaHCO3 – K4Fe(CN)6 3H2O
- Thema: chemische reacties – compexreacties – redoxreacties
- Tijd:30 min
- Begrippen: stofveranderingen – neerslagen
4.3.3. Azijn
4.3.3.1. Bepaling van gehalte azijnzuur in tafelazijn met een nunclonschaaltje

- Info: Hoeveel azijnzuur zit er in tafelazijn? Titratie in een nunclonplaatje
- Moeilijkheid: gemiddeld
- Chemische stoffen: 5 ml tafelazijn – 5 ml 0,10 mol/l NaOH – Fenolftaleïne 1%
- Thema:neutralisatiereactie – biochemie
- Tijd:30 min
- Begrippen: titratie
4.3.3.2. Bereiding van wijnazijn uit wijn

- Info: Hoe kan je wijnazijn bereiden uit wijn? Doordat de wijn aan lucht kan, komt er een bacterie op. Deze azijnzuurbacterie zorgt er voor dat de alcohol wordt geabsorbeerd en oxideert de alcohol tot azijnzuur. Hierdoor ontstaat wijnazijn. De azijnzuurbacterie sterft wanneer er een teveel aan azijnzuur is.
- Moeilijkheid: gemiddeld
- Chemische stoffen: 100 ml witte wijn
- Thema: biochemie
- Tijd:30 min
- Begrippen: groei micro-organismen
4.3.3.3. Het azijnzuurgehalte bepalen

- Info: Hoeveel is het azijnzuurgehalte van tafelazijn? Titratie
- Moeilijkheid: gemiddeld
- Chemische stoffen: Water – NaOH 0,10 mol/l – azijn
- Thema: biochemie – neutralisatie
- Tijd:30 min
- Begrippen: titratie
4.3.4. Frisdranken
4.3.4.1. Adsorptie en filtratie van cola met minilabor

- Info: Na adsorptie van kleurstof uit cola de filtratie in minilabor
- Moeilijkheid: eenvoudig
- Chemische stoffen: ontgaste colawater 5ml – actieve kool 0,5g
- Thema: scheidingstechnieken – biochemie
- Tijd: 10 min
- Begrippen: filtratie – residu – filtraat
4.3.4.2. Lichtgevende tonic

- Info: Geeft tonic licht onder een UV-lamp en hoe komt dit? Tonic bevat kinine, een zeer bittere stof. Kinine fluoresceert. Wanneer het met UV-licht wordt beschenen, zal het zelf blauw licht beginnen uitschijnen.
- Moeilijkheid: eenvoudig
- Chemische stoffen:schweppes tonic
- Thema: chemische reacties – energetische aspecten – biochemie
- Tijd: 5 min
- Begrippen: exo-energetische reacties – lichtvorming – luminescentie
4.3.4.3. Spuit de hoogste colafontein

- Info: Maak de hoogste colafontein met 1,5L cola-Light, Coca Cola, Cola Light Lemon of Cola Zero en 5 mentossnoepjes naar keuze. Wanneer je een mentossnoepje in cola gooit verstoor je door het toevoegen van de suikers het evenwicht tussen koolzuur en kooldioxide (de prik) in de cola. Het instabiele koolzuur valt daardoor versneld uit elkaar in water en nog meer kooldioxide-belletjes. De snel ontsnappende extra belletjes maken daarna de fontein.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 1 Fles Cola naar keuze – 5 mentos naar keuze
- Thema: biochemie
- Tijd: 5 min
- Begrippen: exo-energetische reacties
4.3.4.4. Roest en cola

- Info: Wat gebeurt er als we cola aanbrengen op roest? Onmiddellijk na de toevoeging van de nagels in de cola, is de cola aan het bruisen. De verroeste nagel zorgt voor een hevigere reactie dan de opgeschuurde nagel, er komt een gas vrij.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Staalwol – Cola – NaCl-oplossing – Gedestilleerd water – Ontkleurde cola
- Thema: biochemie – redoxreactie
- Tijd: 15 min
- Begrippen: roesten
4.3.4.5. Aanduiden koolzuurgas in cola

- Info: Hoe tonen we aan dat er koolzuurgas in cola zit? De vrijgezette gassen lossen op in de bariumhydroxide oplossing en vormen een neerslag. Deze neerslag toont CO2 aan.
- Moeilijkheid: eenvoudig
- Chemische stoffen: bariumhydroxideoplossing – cola
- Thema: biochemie – neerslagreactie
- Tijd: 15 min
- Begrippen: neerslagreactie – identificatie
4.3.4.6. Oplosbaarheid van CO2 in cola

- Info: Gaat de CO2 van cola beter behouden blijven in een warmwaterbad of in een koudwaterbad?
- Moeilijkheid: eenvoudig
- Chemische stoffen: cola
- Thema: biochemie – oplosbaarheid
- Tijd: 15 min
- Begrippen: oplosbaarheid van gassen – identificatie
4.3.4.7. Colafontein

- Info: Welke invloed heeft mentos op cola? Wanneer je een mentossnoepje in cola gooit verstoor je door het toevoegen van de suikers het evenwicht tussen koolzuur en kooldioxide (de prik) in de cola. Het instabiele koolzuur valt daardoor versneld uit elkaar in water en nog meer kooldioxide-belletjes. De snel ontsnappende extra belletjes maken daarna de fontein.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 1 Fles Cola naar keuze – 5 mentos naar keuze
- Thema: biochemie
- Tijd: 5 min
- Begrippen: exo-energetische reacties
4.3.4.8. Colavulkaan

- Info: Wat gebeurt er als we bakpoeder en Coca Cola samenvoegen? Het voedseladditief E338, fosforzuur, gaat reageren met het bakpoeder, waardoor CO2 ontstaat. Zo kom het dat het mengsel gaat stijgen uit de maatbeker en zal overspoelen. De vulkaanvorm zorgt dat de proef er spectaculairder uitziet.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 1Grote lepel bakpoeder – 75 ml Coca Cola
- Thema: biochemie – gasvormingsreactie
- Tijd: 15 min
- Begrippen: gasvorming
4.3.4.9. Titratie van fosforzuur

- Info: Hoeveel fosforzuur zit er in cola? Via de reactie met natriumhydroxide en de indicatorwordt 1 zuurfunctie geneutraliseerd.
- Moeilijkheid: eenvoudig
- Chemische stoffen: tft oplossing (thymolftaleïne 0,05% in ethanol) – Natriumhydroxide 0,1 mol/l – Neutraalrood (0,1% in water) – Methyleenblauw (0,1% in water) – Cola
- Thema: biochemie – neutralisatiereactie
- Tijd: 15 min
- Begrippen: titratie
4.3.4.10. Colabatterij

- Info: Hoe kunnen we een batterij maken met cola die sterk genoeg is voor een LED-lampje te laten branden? Door een galvanische cel te maken en cola dient als zoutbrug.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Cola – 3 Koperelektrode – 3 Zinkelektrode of magnesiumelektrode
- Thema: chemische reacties – energetische aspecten – redoxreactie – biochemie
- Tijd: 20 min
- Begrippen: exo-energetische reacties – galvanische cel
4.3.4.11. Cola ontkleuren + pH

- Info: Hoe ontkleuren we Cola? Cola wordt met de actieve kool in verhouding 10 op 1 ongeveer 5 minuten opgewarmd in een warmwaterbad.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Actieve kool – Coca-Cola
- Thema: biochemie – scheidingstechnieken
- Tijd: 20 min
- Begrippen: adsorptie – filtratie
4.3.4.12. De pH van cola

- Info: Welke pH heeft cola? Doordat cola fosforzuur bevat is het een sterk zuur met een pH-waarde van 3.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Cola – Ontkleurde cola
- Thema: biochemie – neutralisatiereactie
- Tijd: 20 min
- Begrippen: adsorptie – filtratie – pH
4.3.4.13. Cola vs Cola Light

- Info: Wat merk je op bij het uitdampen en verbranden van Cola en Cola Light? Cola net als Cola Light bestaat uit een groot deel uit water. Het water verdampt. Het colastaaltje ruikt na een tijdje naar vanille, kaneel en daarna naar Karamelsuiker. Na een langere tijd komt er sterkere geur.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Cola – Cola Light
- Thema: biochemie
- Tijd: 20 min
- Begrippen: massadichtheid
4.3.4.14. Dichtheidsverschil tussen Cola en Cola Light

- Info: Hoe kunnen we het verschil tussen cola en cola light visueel aantonen? Het coca cola blikje zinkt en het blikje met coca cola light blijft drijven. Dit komt door de kleinere dichtheid van coca cola light, vanwege het lagere suikergehalte.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Cola – Cola Light
- Thema: biochemie
- Tijd: 20 min
- Begrippen: massadichtheid
4.3.4.15. Taurine in een energiedrankje

- Info: Hoe kunnen we de aanwezigheid van taurine aantonen in een energydrank? Ninhydrine is een stof die zal reageren met de aanwezige aminozuur, in dit geval de taurine. Het is ook goed oplosbaar in alcoholen zoals propaan-2-ol. Doordat er in energydrink taurine zit, zal deze dan reageren en verkrijgen we een verkleuring, dat normaal blauw-violet zal zijn.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Propaan-2-ol – Ninhydrin – Natriumhydroxide 2 mol/l – Energydrank – Water – Waterstofchloride 2 mol/l
- Thema: biochemie
- Tijd: 20 min
- Begrippen: identificatie taurine
4.3.4.16. Suikergehalte semi-kwantitatief aantonen

- Info: Wat is het verschil in suikergehalte tussen een normale frisdrank en zijn light versie? Doordat we de frisdrank boven het vuur houden, zal het vloeistof feitelijk verdampen. Al het vloeistof zal verdwijnen en dan zal het suiker wat achterblijft karamelliseren en uiteindelijk zwart worden. We merken dat er in de zero versie van het frisdrank veel minder neerslag achterblijft, wat op wijst dat het weldegelijk weinig suiker bevat. Dit is feitelijk wel geen suiker maar aspartaam.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Propaan-2-ol – Ninhydrin – Natriumhydroxide 2 mol/l – Energydrank – Water – Waterstofchloride 2 mol/l
- Thema: biochemie – kwantitatieve aspecten
- Tijd: 20 min
- Begrippen: identificatie – dosering
4.3.4.17. Vitamine C in fruitsap

- Info: Hoe kunnen we de gehalte vitamine C in fruitsap bepalen? Doseren via een redoxtitratie
- Moeilijkheid: eenvoudig
- Chemische stoffen: Fruitsap – I2-oplossing – Na2S2O3-oplossing – Zetmeelindicator – Water
- Thema: biochemie – redoxreacties
- Tijd: 20 min
- Begrippen: ititratie – dosering
4.3.4.18. Lichtgevende tonic

- Info: Geeft tonic licht onder een UV-lamp en hoe komt dit? Tonic bevat kinine, een zeer bittere stof. Kinine fluoresceert. Wanneer het met UV-licht wordt beschenen, zal het zelf blauw licht beginnen uitschijnen.
- Moeilijkheid: eenvoudig
- Chemische stoffen:schweppes tonic
- Thema: chemische reacties – energetische aspecten – biochemie
- Tijd: 15 min
- Begrippen: exo-energetische reacties – lichtvorming – luminescentie
4.3.4.19. Paarse limonade, doorzichtige limonade

- Info: Hoe verkrijgen we een mengsel met twee verschillende kleurlagen? Doordat we het alkaan met kaliumpermanganaat samenvoegen verkrijgen we een heterogeen mengsel waar het alkaan boven drijft door zijn lagere massadichtheid dan die van kaliumpermanganaat-oplossing. Bovendien zijn deze stoffen slecht oplosbaar in elkaar.
- Moeilijkheid: eenvoudig
- Chemische stoffen: n-hexaan – Kaliumpermanganaat (0,002 mol/l) – Dijood – Water
- Thema: organische stoffen – biochemie
- Tijd: 15 min
- Begrippen: polariteit
4.3.4.20. Limonade namaken

- Info: Hoe kunnen we limonade namaken? De tannine met water gaf een limonade achtige kleur, wanneer de tannine in aanmerking kwam met het IJzer(III)chloride begon deze zwart te kleuren door het gevormde complex.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Tannine 3,5 g – IJzer(III)chloride 0,1 mol/l – Zwavelzuur 3 mol/l – Water
- Thema: organische stoffen – biochemie
- Tijd: 15 min
- Begrippen: complexreactie
4.3.4.21. Reactie tussen melk en cola

- Info: Wat gaat er gebeuren wanneer men een mengsel van cola en volle melk maken? Als de melk en de cola worden gemengd, dan reageren de eiwitten uit de melk en het fosforzuur uit de cola met elkaar.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Cola – Volle melk
- Thema: neerslagreactie – biochemie
- Tijd: 15 min
- Begrippen: coagulatie
4.3.4.22. Doorzichtige cola

- Info: Hoe kunnen we cola, een ondoorzichtige drank, doorzichtig maken met behulp van een chemische reactie? De kleurstof in cola is kleurstof e150d, oftewel karamelkleurstof. De ‘d’ slaat op de toevoeging van ammoniakzouten en sulfieten, dus de complete naam is sulfiet-ammoniakkaramel. Het natriumhypochloriet (NaClO) in het bleekwater zorgt voor een ontkleuring van deze kleurstof door een chemische reactie waarbij de kleurstof wordt omgezet in zijn kleurloze leuco-vorm.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Cola – Bleekwater
- Thema: chemische greactie – biochemie
- Tijd: 15 min
- Begrippen: kleurverandering
4.3.4.23. Onderscheid maken tussen cola en cola light

- Info: Hoe maak je het onderscheid tussen cola en cola light? Door ontkleuring van blauw naar rood wordt in cola gewoon het glucose aangetoond. De test op cola light is negatief.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Cola – Haines reagens – cola light
- Thema: chemische greactie – biochemie
- Tijd: 15 min
- Begrippen: kleurverandering
4.3.5. Fruitsappen
4.3.5.1.De fruitsapklok

- Info: Door de chemische reacties die optreden in de fruitsap ontstaat elektrische energie. Dit is een voorbeeld van een exo-energetische reactie met vorming van elektrische energie.
- Moeilijkheid: gemiddeld
- Chemische stoffen: fruitsap – 20 tot 30 cm magnesiumlint, aan één uiteinde opgerold rond b.v. een ijslollystokje; – 20 tot 30 cm koperdraad, aan één uiteinde opgerold;
- Thema: chemische reacties – energetische aspecten – redoxreactie – biochemie
- Tijd: 20 min
- Begrippen: exo-energetische reacties – galvanische cel
4.3.5.2. Microschaaltitratie van vitamine C in fruitsappen

- Info: Hoe kunnen we gehalte vitamine C bepalen? Jodaat vormt met jodide in een zure oplossing jood.Ascorbinezuur is in oplossing makkelijk te oxideren tot dehydro-ascorbinezuur. Als oxidator kan een joodoplossing gebruikt worden:
- Moeilijkheid: gemiddeld
- Chemische stoffen: vitamine C tabletten – zwavelzuur 2 mol/l – KI oplossing 2 mol/l – KIO3 oplossing 0.03 mol/l – zetmeeloplossing
- Thema: redoxreactie – biochemie
- Tijd: 40 min
- Begrippen: titratie
4.3.5.3. Mierenzuur als conserveermiddel

- Info: Hoe kan mierenzuur een conserveermiddel zijn? De niet behandelde stalen worden troebel. Met mierenzuur zijn de gemaakte mengsels niet troebel.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Mierenzuur/ Methaanzuur – Fruitsap – Stukken worst of ham – Gras
- Thema: organische stoffen – biochemie
- Tijd: 25 min
- Begrippen: carbonzuren – oxidatie
4.3.5.4. Tomatensap met broom

- Info: Het belangrijkste pigment in tomaten is het lycopen. In de structuur zijn geconjugeerde electronensystemen aanwezig die blauwe kleur absorberen en daardoor een rode kleur hebben. Door additie met broom verkleint de lengte van het geconjugeerd systeem waardoor de geabsorbeerde golflengte verkort. Deze gaat uiteindelijk naar kleurloos.
- Moeilijkheid: eenvoudig
- Chemische stoffen: tomatensap – broomwater (verzadigd)
- Thema: organische stoffen – redoxreacties
- Tijd: 20 min
- Begrippen: reacties met organische stoffen – oxidatie
4.3.6. Koffie en thee
4.3.6.1. Extractie van cafeïne uit koffie

- Info: Hoe verkrijg je cafeïne uit koffie? Door de paarse kleur kunnen we aanduiden dat er cafeïne in koffie zit. De cafeïne lost op in het oplosmiddel (dichloormethaan) en de rest niet.
- Moeilijkheid: gemiddeld
- Chemische stoffen: cafeïne houdende stof (koffie) – natriumcarbonaat – dichloormethaan – magnesiumsulfaat – geconc HCl – Kaliumchloraat – NH4OH 2 mol/l
- Thema: scheidingstechnieken – biochemie
- Tijd:15 min
- Begrippen: extractie
4.3.6.2. Extraheren van koffie uit koffiepoeder

- Info: Een aantal geur-, smaak- en kleurstoffen lossen op in het water, wat dient als extractiemiddel. Na filtratie is de donkere kleur van het water goed zichtbaar. Des te warmer het water, des te meer en des te makkelijker de geur-, kleurstoffen oplossen.
- Moeilijkheid: gemiddeld
- Chemische stoffen: koffiepoeder – heet water (kookplaat/waterkoker)
- Thema: scheidingstechnieken – biochemie
- Tijd: 10 min
- Begrippen: extractie
4.6.3.3. Vliegend theezakje

- Info: Wat gebeurt er als we een theezakje aansteken? Het papier verbrandt en er ontstaat koolstof.
Het papier verbrandt en wordt op het einde zo licht en zo warm dat het opstijgt. - Moeilijkheid: eenvoudig
- Chemische stoffen: Theezakje – Aansteker
- Thema: redoxreacties – biochemie
- Tijd: 10 min
- Begrippen: verbrandingsreactie
4.3.6.4. Maak de mooiste “ instant cappuccino”

- Info: Hoe kunnen we het ontleden van zuurstofwater versnellen? Exotherme reactie waarbij het detergent zorgt voor het schuim. De kaliumpermanganaat kristallen blijven op het schuim drijven en zorgen voor het bovenste laagje van de cappuccino.
- Moeilijkheid: gemiddeld
- Chemische stoffen: KMnO4, H2O2 30 % (5 ml) , vloeibaar detergent
- Thema: anorganische stoffen – energetische aspecten – redoxreactie – biochemie
- Tijd: 10 min
- Begrippen: peroxiden – exo-energetische reacties –katalysator
4.3.6.4. Huid met zwarte thee

- Info: Hoe kunnen we een huid maken met zwarte thee? Na toevoegen van de oplossingen ontstaat een geribbelde huid.Dit ontstaat door reactie van thee met warm water en de ontstane polyfenolen met calciumionen. Door de aanwezigheid van zuurstof en bicarbonaationen ontstaan onoplosbare verbindingen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 1 builtje zwarte thee – Calciumdichloride (CaCl2) – Natriumwaterstofcarbonaat (NaHCO3)
- Thema: biochemie – neerslagreacties
- Tijd: 10 min
- Begrippen: complexen
4.3.6.5. Indicator thee
- Info: Welke natuurlijke producten kunnen we gebruiken als indicator? In thee zit een chemische stof thearubigine die samen met het zuur of de base een reactie gaan vormen.Thee kan dus gebruikt worden om zuren en base aan te tonen. In een zuur milieu wordt thee geel en in een basisch milieu gaat thee een donkere kleur krijgen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Koffie – Verdunde natronloog/ Natriumhydroxide (1 mol/l) – Verdund zoutzuur (1mol/l)
- Thema: biochemie – neutralisatiereacties
- Tijd: 10 min
- Begrippen: pH-indicator
4.3.6.6. Chlorofyl in thee
- Info: Hoe kunnen we licht maken met thee? Chlorofyl lost op in ethanol. Door UV-licht wordt het energie opgewekt en deze energie wordt uitgestraald als zichtbaar licht. In zwarte thee wordt het chlorofyl door fermentatieprocessen losgemaakt, daarna is ook hier een fluorescerende werking zichtbaar.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Zwarte thee – Groene thee – Ethanol
- Thema: biochemie – energetische aspecten
- Tijd: 10 min
- Begrippen: luminescentie
4.3.6.7. Het vliegend theezakje

- Info: Wat gebeurt er als we een theezakje aansteken? Het papier verbrandt en er ontstaat koolstof.
Het papier verbrandt en wordt op het einde zo licht en zo warm dat het opstijgt. - Moeilijkheid: eenvoudig
- Chemische stoffen: Theezakje – Aansteker
- Thema: redoxreacties – biochemie
- Tijd: 10 min
- Begrippen: verbrandingsreactie
4.3.6.8. Schrijven met thee, koffie en cacao

- Info: Hoe kan je een tekst schrijven met thee, koffie of cacao? Door toevoegen van ijzersulfaat ontstaat een zwarte oplossing die wordt aangedikt met de arabische gom. Hierdoor kan je schrijven. De geschreven tekst wordt donkerder na verloop van tijd.
- Moeilijkheid: eenvoudig
- Chemische stoffen: thee – ijzer(II)sulfaat – arabische gom
- Thema: redoxreacties – biochemie
- Tijd: 10 min
- Begrippen: identificatiereacties – neerslag
4.3.6.9. De bittere smaak van groene thee

- Info: Waarom smaakt groene thee bitter? Door de aanwezigheid van polyfenolen, die neer te slaan zijn met calciumionen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 4 buidels groene thee – Calciumchloride – gedestilleerd water
- Thema: redoxreacties – biochemie
- Tijd: 10 min
- Begrippen: identificatiereacties – neerslag
4.3.6.10. Geheime boodschap

- Info: Kan je een geheime boodschap maken met thee? De thee gaat een reactie vormen met het zuur waardoor er een donkere kleur gevormd wordt. Deze kleur zorgt ervoor dat je tekst terug zichtbaar is.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Heel sterke zwarte thee – Citroen
- Thema: neutralisatiereacties – biochemie
- Tijd: 10 min
- Begrippen: identificatiereacties – indicator
4.3.6.11. Extractie van Chlorofyl

- Info: Wat is het verschil in de extractie van chlorofyl uit groene en zwarte thee?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Gedestilleerd water – groene thee – zwarte thee – ether
- Thema: scheidingstechnieken- biochemie
- Tijd: 20 min
- Begrippen: extractie
4.3.6.12. Kombucha

- Info: Hoe maak je een bioplastic met zwarte thee? Je maakt een bioplastic van thee door dat je een systeem creëert waarbij gist en bacteriën in symbiose met elkaar werken.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Warm water – Zwarte thee – Appel ciderazijn – Suiker
- Thema: kunststoffen- biochemie
- Tijd: 60 min
- Begrippen: bioplastics
4.3.7. Melk
4.3.7.1. Kunststof uit melk

- Info: In melk zit een stof dat caseïne heet. Normaal gesproken is die caseïne opgelost in de melk. Maar als je zure azijn toevoegt, verandert de caseïne een beetje. Het stofje lost dan niet meer op in de melk. Daardoor komen er plastic lijkende brokjes in de melk.
- Moeilijkheid: eenvoudig
- Chemische stoffen: huishoudazijn (100 ml) – volle melk (200 ml)
- Thema: kunststoffen- biochemie
- Tijd: 60 min
- Begrippen: bioplastics
4.3.7.2. Kwalitatief onderzoek van melk

- Info: Hoe kunnen we de samenstelling van melk kwalitatief nagaan? Na scheiden in componenten gebeuren verschillende identificatiereacties
- Moeilijkheid: gemiddeld
- Chemische stoffen: volle melk – verdund azijnzur -verdund natriumhydroxide 0.5 M -kopersulfaatoplossing 1% -diethylether -ethanol 96% -indikatorpapier -natriumsulfaat -Fehling-oplossingen -SudanIII-oplossing 0.1% in methanol
-natriumdithionietoplossing 1% -ammoniumoxalaatoplossing 5% -ammoniummolybdaatoplossing 10% - Thema: chemisch rekenen – scheidingstechnieken – biochemie
- Tijd: 120 min
- Begrippen: concentratie – identificatiereacties – scheidingsschema
4.3.7.3. Lichtverstrooiing en lichtgeleiding in melk

- Info: Melk is een emulsie van vet druppels in water die gestabiliseerd wordt door eiwit moleculen die zich gedragen als emulsifiers en daardoor supermoleculen vormen. Deze druppels verstrooien het licht op dezelfde manier als de moleculen en deeltjes die in de lucht om ons heen aanwezig zijn het licht verstrooien.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Melk
- Thema: biochemie
- Tijd: 20 min
- Begrippen: lichtverstrooiing
4.3.7.4. Lijm uit melk

- Info:Hoe kunnen we met melk lijm maken? Wanneer melk zuur wordt vlokt het eiwit caseïne uit. Caseïne wordt gewonnen door afgeroomde melk met water te verdunnen en er vervolgens azijnzuur aan toe te voegen zodat de caseïne neerslaat.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Melk – azijnzuur 2 mol/l
- Thema: biochemie – kunststoffen
- Tijd: 20 min
- Begrippen: intermoleculaire krachten
4.3.7.5. Lijmen

- Info:Hoe kunnen we met melk lijm maken? Twee te hechten voorwerpen worden aangetrokken door de lijmmoleculen door middel van intermoleculaire interacties.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Melk – azijnzuur 2 mol/l
- Thema: biochemie – kunststoffen
- Tijd: 20 min
- Begrippen: intermoleculaire krachten
4.3.7.6. Melk en huishoudazijn samenvoegen

- Info: Als je de melk zuurder maakt door er azijn aan toe te voegen, kan de caseïne niet opgelost blijven. Hierdoor verdwijnt de emulgerende werking rond de vetten zodanig dat ook de vetten gaan uitvlokken. De melk gaat schiften in water en losse caseïne. Als je de caseïne laat opdrogen wordt het heel hard. Daarom kun je er leuk beeldjes mee maken.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Melk – azijnzuur 2 mol/l
- Thema: biochemie – kunststoffen
- Tijd: 20 min
- Begrippen: intermoleculaire krachten
4.3.7.7. Plakken met melk

- Info: Hoe kunnen we lijm maken op basis van melkpoeder en andere huishoudproducten? Het melkpoeder reageert met het zuur van azijn. Er ontstaan allemaal kleine klontjes. Dat zijn eiwitklontjes. Eiwit is niet alleen het wit van een ei, maar ook een ander woord voor proteïne. Proteïnes zitten in veel voedingsmiddelen, zoals melk. Door het bakpoeder bij de klontjes te doen, worden de eiwitklontjes zacht. Zo wordt je lijm goed smeerbaar.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Melkpoeder (voor in de koffie) – Water – Azijn – Bakpoeder
- Thema: biochemie
- Tijd: 20 min
- Begrippen: intermoleculaire krachten
4.3.7.8. Schilderij met indicatoren in melk
- Info: Hoe kan je een uniek schilderij maken met melk, kleurstoffen en afwasmiddel? Melk bevat veel vetten, deze vetten zorgen ervoor dat alles op zijn plaats blijft. Doordat je een zeep toevoegt, zullen de zwakke chemische bindingen die de eiwitten in de oplossing houden veranderen. Hierdoor gaan alle kleurstofdeeltjes in alle richtingen en krijg je vervolgens een kleurenfestijn op je bord.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Melk – Enkele indicatoren met verschillende kleuren – afwasmiddel
- Thema: biochemie – neutralisatiereacties
- Tijd: 20 min
- Begrippen: indicatoren
4.3.7.9. Zuurgehalte van melkproducten

- Info: Hoeveel zuur bevat melk? Je bepaalt de concentratie door een titratie met een sterke base
- Moeilijkheid: eenvoudig
- Chemische stoffen: Melk – NaOH 0,1 mol/l – 2% fft; – 5% kobaltdichlorideoplossing
- Thema: biochemie – neutralisatiereacties
- Tijd: 20 min
- Begrippen: titratie
4.3.7.10. Zonnemelk

- Info: Hoe beschermt zonnemelk je tegen de UV-straling van de zon? Melk is een emulsie van vet druppels in water die gestabiliseerd wordt door eiwit moleculen die zich gedragen als emulsifiers en daardoor supermoleculen vormen. Deze druppels verstrooien het licht op dezelfde manier als de moleculen en deeltjes die in de lucht om ons heen aanwezig zijn het licht verstrooien
- Moeilijkheid: eenvoudig
- Chemische stoffen: Volle melk – Water
- Thema: biochemie – bouw van materie
- Tijd: 20 min
- Begrippen: lichtverstrooiing – colloïdale oplossing
4.3.7.11. Melkkunst

- Info: Hoe kan je een beeldje maken met melk en azijn? n melk zit een als belangrijkste eiwit het caseïne . In melk is die caseïne de emulgator voor de o/w emulsie. De emulgator laat toe dat de vetdeeltjes verdeelt blijven in de waterfase. Door het homogeniseren van de melk in de melkerij blijft de emulsie stabiel. Maar als je zure azijn toevoegt, verandert de caseïne een klein beetje. De eiwitstructuur wordt deels afgebroken waardoor de emulgerende werking vermindert. De vetdeeltjes komen vrij en coaguleren ter vorming van een wrongel (vet en caseïne). Door de suspensie te filtreren en het achtergebleven water uit te persen is een klonter te bekomen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 0,5l volle melk – 3 eetlepels azijn
- Thema: biochemie – kunststoffen
- Tijd: 20 min
- Begrippen: bioplastics
4.3.7.12. Samenstelling van melk

- Info: Hoe kunnen we de samenstelling van melk kwalitatief nagaan? Na scheiden in componenten gebeuren verschillende identificatiereacties
- Moeilijkheid: gemiddeld
- Chemische stoffen: volle melk – verdund azijnzur -verdund natriumhydroxide 0.5 M -kopersulfaatoplossing 1% -diethylether -ethanol 96% -indikatorpapier -natriumsulfaat -Fehling-oplossingen -SudanIII-oplossing 0.1% in methanol
-natriumdithionietoplossing 1% -ammoniumoxalaatoplossing 5% -ammoniummolybdaatoplossing 10% - Thema: chemisch rekenen – scheidingstechnieken – biochemie
- Tijd: 120 min
- Begrippen: concentratie – identificatiereacties – scheidingsschema
4.3.7.13. Calcium in melk

- Info: Hoe kan je de aanwezigheid van calcium in melk bewijzen aan de hand van ammoniumoxalaat? De calciumionen zitten in de wei van volle melk. We kunnen ze aantonen aan de hand van een neerslagreactie met een ammoniumoxalaatoplossing
- Moeilijkheid: eenvoudig
- Chemische stoffen: Volle melk (wei) – Ammoniumoxalaatoplossing 10%
- Thema: neerslagreactie – biochemie
- Tijd: 20 min
- Begrippen: identificatiereacties – neerslagvorming
4.3.7.14. Vitamine B2 in melk

- Info: Hoe kan je de aanwezigheid van vitamine B2 in melk bewijzen met een UV-lamp? De vitamine B2 fluoresceert onder de invloed van de UV-lamp
- Moeilijkheid: eenvoudig
- Chemische stoffen: Volle melk (wei)
- Thema: biochemie – chemische reacties
- Tijd: 20 min
- Begrippen: luminescentie
4.3.7.15. Verse of oude melk

- Info: Hoe weet je of de melk vers of oud is? Alizarine werkt als indicator voor zuren en basen. In een basisch milieu kleurt het blauw-violet, in een zuur milieu geel. Verse melk is met andere woorden eerder neutraal terwijl oude melk zuurder is.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Verse volle melk – Oude volle melk (ongeveer 1 week oud) – Ethanol 99% – Alizarine
- Thema: biochemie – chemische reacties – neutralisatiereactie
- Tijd: 20 min
- Begrippen: pH-indicator
4.3.7.16. Schrijven met melk

- Info: Hoe schrijf je een geheim bericht met melk? Opgedroogde melk heeft een lagere ontbrandingstemperatuur dan papier. Dat betekent dat papier meer warmte nodig heeft om te reageren met zuurstof dan opgedroogde melk .
- Moeilijkheid: eenvoudig
- Chemische stoffen: Strijkijzer – Melk
- Thema: biochemie
- Tijd: 20 min
- Begrippen: verbrandingsreactie
4.3.7.17. Geheime boodschap

- Info: Hoe schrijf je een geheim bericht met melk? Wanneer het vel papier met onzichtbare inkt wordt verhit, vindt de afbraak van citroenzuur, melk en keukensoda plaats. Als gevolg van deze chemische reacties komen de producten van hun afbraak vrij, die het papier bruin kleuren, waardoor de geheime boodschap zichtbaar wordt.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Melk – Citroensap – Bakpoeder oplossing
- Thema: biochemie
- Tijd: 120 min
- Begrippen: verbrandingsreactie
4.3.7.18. Melk en kleurstof

- Info: Hoe kunnen we het verschil in volle en magere melk aantonen? Zeep bestaat uit een hydrofiele en hydrofobe kant. De hydrofobe kant trekt vetten aan. Bij de volle melk reageert deze hydrofobe kant met het vet in de melk waardoor de melk aangetrokken wordt en de kleurstof afgestoten. Bij de magere melk zit er meer vet in de kleurstof dan in de melk waardoor de kleurstof aangetrokken wordt en de melk afgestoten.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Melk – Voedingskleurstof – Afwasmiddel
- Thema: biochemie – neutralisatiereactie
- Tijd: 120 min
- Begrippen: pH indicator
4.3.7.19. Schrijven met melk

- Info: Hoe kan een geheime boodschap geschreven met melk ontcijferd worden? Door de bovenstaande werkwijze toe te passen kan er worden geschreven worden met melk. Hierbij zal door het verwarmen de Maillardreactie ontstaan waardoor de lactose en lysine (beiden bestanddelen van melk) gaan reageren waarbij het water verdampt en er een amide gevormd wordt wat voor de bruine kleur zorgt.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Melk
- Thema: biochemie
- Tijd: 20 min
- Begrippen:verbrandingsreactie
4.3.8. Water
4.3.8.1. Titratie van bicarbonaat in leidingwater

- Info: Hoeveel bicarbonaat zit er in leidingwater?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Methyleenblauw – Neutraalrood – Kraanwater – HCl-oplossing 0,1 mol/l
- Thema: biochemie – neutralisatiereactie
- Tijd: 20 min
- Begrippen:titratie
4.3.8.2. Invloed van temperatuur bij het oplossen van stoffen

- Info: Hoe heeft de temperatuur een invloed bij een oplossen van een stof? Door zout in water te doen gaat deze ook zijn intermoleculaire krachten verliezen. Deze zoekt een evenwicht tussen de intermoleculaire krachten van het oplosmiddel (water). Net zoals bij het smelten van een vaste stof, zal ook bij het oplossen van een vaste stof de temperatuur een invloed hebben.
- Moeilijkheid: eenvoudig
- Chemische stoffen: keukenzout
- Thema: biochemie – oplosbaarheid
- Tijd: 20 min
- Begrippen: invloed van temperatuur
4.3.8.3. Onweer onder water

- Info: Zodra de Kaliumpermanganaat in aanraking komt met de onderste laag zwavelzuur wordt onder andere het groene Mangaanheptoxide gevormd.Dit Mangaanheptoxide gaat op het grensvlak tussen de Ethanol en het Zwavelzuur ook een reactie aan (redoxreactie).
- Moeilijkheid: gemiddeld
- Chemische stoffen:Geconcentreerd zwavelzuur – Ethanol 96% – Vast kaliumpermanganaat
- Thema: chemische reacties – energetische aspecten – redoxreactie – biochemie
- Tijd: 15 min
- Begrippen: exo-energetische reacties – lichtvorming – verbrandingsreactie
4.3.8.4. Van water naar bier

- Info: Hoe kan kunstmatig vanuit water via een melkproduct naar bier gaan? Ketenreacties met kleurverandering
- Moeilijkheid: gemiddeld
- Chemische stoffen: 20% natriumcarbonaat-oplossing – verzadigde natriumwaterstofcarbonaat-oplossing – gedestilleerd water – mengsel van 1,5g p-nitrofenol en 0,75g fft in 30 ml 95% ethanol – verzadigde bariumchloride-oplossing – 8 mol/l zoutzuur – broomthymolblauw – dijood (c = 0,05 mol/l) – detergent
- Thema: chemische reacties – redoxreactie – biochemie
- Tijd: 35 min
- Begrippen: complexreacties – kleurverandering
4.3.8.5. Vulkaan onder water

- Info: Hoe kan je een vulkaan reconstrueren met water en olie? Olie heeft een kleinere massadichtheid ten opzichte van water. Hierdoor drijft olie op water. Dit experiment gaat echter verder dan dat. Doordat watermoleculen en oliemoleculen onderricht zijn aan de Vanderwaalskrachten, is er sprake van oppervlaktespanning.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Gedemineraliseerd water – Sudanrood – Olie – afwasmiddel
- Thema: biochemie
- Tijd: 35 min
- Begrippen: oplosbaarheid
4.3.8.6. Water kleuren met rode wijn

- Info: Indien we een glas wijn en een glas water hebben, hoe kunnen we dan dit water kleuren met de wijn, zonder de glazen aan te raken? De wet van communicerende vaten stelt dat wanneer twee vaten met elkaar verbonden zijn, deze na verloop van tijd gelijk zullen zijn in niveau.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Gedemineraliseerd water – wijn
- Thema: biochemie – eigenschappen van stoffen
- Tijd: 15 min
- Begrippen: capillariteit
4.3.8.7. Water naar een glas met een rietje

- Info: Hoe krijg je de vloeistof van een flesje met een rietje in een glas, zonder het flesje op te heffen? Door in de fles te blazen, creëren we een overdruk in de fles. De enige weg waarlangs de druk afgelaten kan worden, is die via het rietje. Hierdoor duw je als het ware het water erdoorheen, waarna het in het glas terechtkomt. Dit kan je blijven doen, totdat de onderkant van het rietje het wateroppervlak bereikt heeft, aangezien je dan gewoon de lucht rechtstreeks terug via het rietje naar buiten blaast.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Gedemineraliseerd water
- Thema: biochemie – eigenschappen van stoffen
- Tijd: 15 min
- Begrippen: onderdruk
4.3.8.8. Verandering water in wijn

- Info: Hoe kan je water in wijn laten veranderen? Door Na2CO3 op te lossen in water en FFT ontstaat er een roze kleur. Dit komt omdat FFT een zuur-base-indicator is, die roze kleurt in een basisch milieu.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Na2CO3 – Water – Fenolftaleïne 0,05% – Zoutzuur 1 mol/l
- Thema: biochemie – neutralisatiereactie
- Tijd: 15 min
- Begrippen:pH-indicatoren
4.4. Ei
4.4.1. Aanslag op het oog

- Info: Wat gebeurt er als we eiwit laten reageren met HCl, HNO3 en H2SO4? We zien dat het gebruik van sterke zuren zorgt voor chemische reacties zoals neerslagvorming (eiwit + HCl). Dit is een irreversibel proces omdat de sterke zuren zorgen voor een hydrolyse van de peptidebindingen tussen de aminozuren.
- Moeilijkheid: eenvoudig
- Chemische stoffen: eiwit van rauw ei 6 mol/l HCl – HNO3 10 mol/l – H2SO4 geconcentreerd
- Thema: biochemie
- Tijd: 15 min
- Begrippen: eiwitten – neerslagreactie
4.4.2. Dansende rozijnen

- Info: Hoe kunnen we rozijnen laten dansen? Eerst bruist het mengsel hevig en zien we een hevige gasvorming. Na enkele ogenblikken stijgen de rozijnen en dalen ze weer. Zolang als er gas aanwezig is, blijven de rozijnen deze beweging maken.
- Moeilijkheid: eenvoudig
- Chemische stoffen: rozijnen – halve eetlepel soda – ¼ bekertje azijn
- Thema: chemische reacties – anorganische stoffen – stofeigenschappen – biochemie
- Tijd: 20 min
- Begrippen: zouten – vorming van koolstofdioxide – massadichtheid
4.4.3. Eitje bakken met calciumoxide

- Info: Calcium oxide reageert exothermisch met water en vormt Calciumhydroxide
- Moeilijkheid: eenvoudig
- Chemische stoffen: Ei – Calciumoxide
- Thema: chemische reacties – energetische aspecten – biochemie
- Tijd: 25 min
- Begrippen: Oploswarmte – warmte – exo-energetische reactie
4.4.4. Eitje wordt springbal

- Info: Hoe kunnen we een eitje laten botsen? De schaal van een ei is gemaakt van calciumcarbonaat. Dit lost op in het zuur. Hierdoor ontstaan belletjes
- Moeilijkheid: eenvoudig
- Chemische stoffen: 1 rauw ei – 300 ml tafelazijn
- Thema: chemische reacties – biochemie
- Tijd: 25 min
- Begrippen: vorming van koolzuurgas
4.4.5. Groengebakken ei

- Info: De pigmenten in de rode kool zijn anthocyanen. De anthocyanen veranderen van kleur door de pH-waarde. De rode kool is rood in zure omstandigheden en verandert naar blauw-groen in basisch mileu. Het ei-wit is alkalisch (pH 9) en wordt zo groen. De pH verandert niet als het eitje wordt gebakken en de kleur blijft stabiel.
- Moeilijkheid: eenvoudig
- Chemische stoffen: ei – rode kool
- Thema: neutralisatiereacties – biochemie
- Tijd: 25 min
- Begrippen:pH- indicatoren
4.4.6. Knalgas in een ei

- Info: Hoe kunnen we knalgas vormen in een ei? Het ei heeft zich gevuld met het knalgas doordat dit lichter is dan lucht en het stijgt. Wanneer we dan een lucifer in de buurt houden van het ei, ontploft het ei. Door de reactie van HCl met magnesium ontstaat er H2-gas, ook wel knalgas genoemd.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Uitgeblazen ei – Tape – HCl
- Thema: enkelvoudige stoffen – redoxreactie – chemische reactie – biochemie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – exo-energetische reactie – synthesereactie
4.4.7. Koolstof uit eierschalen

- Info: Op welke manier kunnen we koolstof bereiden uit eierschalen? Eierschalen bevatten calciumcarbonaat. Dit gaat met magnesium koolstof vormen. Het wit licht dat tijdens de verbranding ontstaat, is afkomstig van het magnesium en de oranje vonkjes zijn afkomstig van het calciumcarbonaat in de eierschalen.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Droge eierschalen – Magnesiumpoeder – Zoutzuur 1mol/l
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – verdringingsreactie metalen
4.4.8. Magische eieren

- Info: Eieren in een keukenzoutoplossing zinkt, eieren in een zoutzuuroplossing komt drijven. De reden van het bewegen is de vorming van CO2 van het CaCO3 van de eierschaal wat in contact komt met de HCl. Wanneer het ei aan het oppervlak komt wordt de gevormde CO2 langs de lucht geëvacueerd.
- Moeilijkheid: eenvoudig
- Chemische stoffen: twee eieren van 65-70g – NaCl – 6mol/l HCl
- Thema:stofeigenschappen – biochemie
- Tijd: 5 min
- Begrippen: dichtheidsverschillen – vorming van koolzuurgas door reactie zoutzuur en calciumcarbonaat
4.4.9. Oplichtend hoenderei
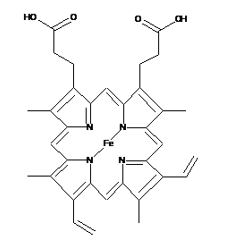
- Info: In de schaal zit ooporphyrin (Protoporphyrine IX). Hierin zit zoals in hemoglobine het haem. In tegenstelling tot hemoglobine bevindt zich centraal het Fe3+. Hierdoor is deze in staat rood op te lichten bij 366nm.
- Moeilijkheid: gemiddeld
- Chemische stoffen: gedroogde bruine hoendereierenschalen – zoutzuur 10% – ethylacetaat
- Thema: chemische reacties – energetische aspecten – redoxreactie – biochemie
- Tijd: 20 min
- Begrippen: exo-energetische reacties – lichtvorming – luminescentie
4.4.10. Osmose door een ei-membraan

- Info: De eieren hebben een harde schaal van calciumcarbonaat en hieronder een membraan dat doorlaatbaar is voor water. Wanneer het ei gebracht wordt in de tafelazijn, wordt de schaal opgelost
- Moeilijkheid: gemiddeld
- Chemische stoffen: 3 rauwe eieren – 500ml tafelazijn – 1,2 l water – 400ml 20% suikersiroop ( los 85 g tafelzuiker op in 350ml water) – 10mg methyleenblauw indicator
- Thema:stofeigenschappen – biochemie
- Tijd: 20 min
- Begrippen: osmose
4.4.11. Chocolade en eieren verwarmen

- Info: Hoe kunnen we het verschil tussen een chemisch en fysisch verschijnsel aantonen met behulp van chocolade en eiwit?
- Moeilijkheid: gemiddeld
- Chemische stoffen: Chocolade – Eiwit van ei
- Thema:stofeigenschappen – biochemie
- Tijd: 20 min
- Begrippen: fysische en chemische reacties
4.4.12. Ei in de fles

- Info: Hoe krijg je een gepeld, hardgekookt eitje in een fles/kolf?
- Moeilijkheid: eenvoudig
- Chemische stoffen: ei
- Thema:stofeigenschappen – biochemie
- Tijd: 20 min
- Begrippen: onderdruk
4.5. Fruit en groenten
4.5.1. Adsorptie met minilabor van aardbeiensauspoeder

- Info: Hoe ontkleuren we aardbeiensaus? Door adsorptie met actieve kool kan de rode kleur van het sap verwijderd worden.
- Moeilijkheid: eenvoudig
- Chemische stoffen: aardbeiensauspoederpoeder 1g – HCl 70% 1ml – ethanol 5ml – actieve kool 10g
- Thema: scheidingstechnieken – biochemie
- Tijd: 10 min
- Begrippen: adsorptie – norit
4.5.2. Extractie van DNA uit ajuin

- Info: Hoe DNA uit een ajuin isoleren?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Een vierde ajuin – Protease enzyme – keukenzout – 5ml koude ethanol
- Thema: scheidingstechnieken – biochemie
- Tijd: 40 min
- Begrippen: extractie
4.5.3. Geheime boodschap met ajuin
- Info: Hoe je een boodschap versturen met een ajuin? Schrijf een boodschap en gebruik een UV-lamp voor het lezen van de boodschap
- Moeilijkheid: eenvoudig
- Chemische stoffen: ajuin – UV-lamp
- Thema:biochemie
- Tijd: 10 min
- Begrippen: luminescentie
4.5.4. Ontkleuren van tomaten

- Info: Door reactie van HCl en KMnO4 vormt Cl2. In een waterige oplossing levert het Cl2 HOCl en HCl. Tijdens de ontkleuringsreactie ontbindt HClO in HCl en O2. Dit O2 ontkleurt de tomatensap.
- Moeilijkheid: eenvoudig
- Chemische stoffen: KMnO4 – 6 mol/l HCl – tomatensap
- Thema:biochemie – redoxreacties
- Tijd: 10 min
- Begrippen: oxidatie
4.5.5. Opname van koolstofdioxide door waterpest

- Info: De planten in de flessen blootgesteld aan het licht waren in staat te doen aan fotosynthese waarbij het CO2 in het water werd verbruikt.
- Moeilijkheid: eenvoudig
- Chemische stoffen: waterpest – Natriumhydroxide (0.1 mol /l)
- Thema:biochemie – redoxreacties
- Tijd: 30 min
- Begrippen: fotosynthese
4.5.6. Oxaalzuurgehalte in rabarber

- Info:In principe kan de hoeveeheid oxaalzuur in planten worden bepaald door titratie met kaliumpermanganaat. Planten bevatten naast oxaalzuur nog anderz zuren zoals appelzuur en melkzuur en reductoren zoals Fe(II)-ionen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: rabarber (80g per bepaling) – HCl 1M – ammoniak 25% – CaCl2 oplossing 15 massa% – zwavelzuur 20massa% -KMnO4 0.02M – Universeelindicatorpapier
- Thema: organische stoffen – redoxreactie – biochemie
- Tijd: 25 min
- Begrippen: carbonzuren – oxidatie
4.5.7. Papierchromatografie op spinazie
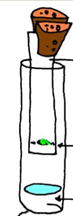
- Info: De kleur van spinazie wordt bepaald door verschillende vormen van chlorofyl, die via chromatografie te scheiden zijn.Chlorofyl a, dan chlorofyl b, dan xantofyl en bovenaan caroteen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: petroleumether – verse spinazie of andijvie, fijngesneden – aceton
- Thema: scheidingstechnieken – biochemie
- Tijd:10 min
- Begrippen: chromatografie – papierchromatografie
4.5.8. Rijp fruit in een ommezien

- Info: Kunnen we d.m.v. een beschimmelde citroen onrijp fruit sneller laten rijpen? De groene schimmel op de citroen geeft een gas af: ethyleen.De schimmel geeft zo veel gas af dat een enkele beschimmelde citroen genoeg is om honderden stukken fruit te doen rijpen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: een citroen laten beschimmelen – papieren zak – onrijpe peren, appelen of perziken
- Thema: organische stoffen – organische reactie – biochemie
- Tijd: 15min
- Begrippen:alkenen – katalysator – oxidatie
4.5.9. Scheiding via TLC van aardbeienpudding
- Info: De verschillende kleurstoffen in aardbeienpudding scheiden van elkaar door TLC-chromatografie
- Moeilijkheid: eenvoudig
- Chemische stoffen: oplossing met kleur van puddingpoeder – Loopmiddel: 2,5% natriumcitraat/5% ammoniak/methanol: 20/5/3
- Thema: scheidingstechnieken – biochemie
- Tijd:10 min
- Begrippen: chromatografie – papier chromatografie – TLC
4.5.10. Stoomdestillatie op lavendel

- Info: Destillatie van geurstoffen uit lavendel. De destillatie verloopt via stoom en in een minilaboropstelling.
- Moeilijkheid: gemiddeld
- Chemische stoffen: 1 g lavendel
- Thema: scheidingstechnieken – biochemie
- Tijd:15 min
- Begrippen: destillatie – stoomdestillatie
4.5.11. Zuren als antioxidans

- Info: Kunnen we het verkleuren van een gesneden appel tegen gaan door het gebruik van zuren? Wanneer we de appel in stukken snijden, reageert een enzym (tyrosinase) in het vruchtvlees met zuurstof waardoor polyfenolen in melanine veranderen (bruine kleur).
- Moeilijkheid: eenvoudig
- Chemische stoffen: Citroenzuuroplossing 10% – HCl oplossing 0,1 mol/l – Ascorbinezuuroplossing 0,1% – Appel
- Thema: redoxreactie – biochemie
- Tijd:15 min
- Begrippen: enzymen – oxidatie
4.5.12. Aroma’s maken

- Info: Hoe kunnen we aroma’s maken op een chemische manier dat hetzelfde ruikt als bepaalde fruitsoorten? Na het toevoegen van zwavelzuur ontstaat er een hevige reactie met mogelijk opspatten van de vloeistof. Door het toevoegen van water kan je beter de 2 vloeistoffases zien.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 2ml: 3-methyl-1-butanol(isoamylalcohol, isopentylalcohol, isopentanol) – 2ml: azijnzuur anhydride – Druppel geconc. Zwavelzuur
- Thema:organische stoffen- biochemie
- Tijd:15 min
- Begrippen: esters
4.5.13. Bruinkleuring van appels

- Info: Wat zorgt er voor dat appels een bruine kleur krijgen en kunnen we dit proces remmen? De verschillende polyfenolen in een appel zijn:chlorogeenzuur (vruchtvlees), catechol, catechine (schil), koffiezuur, 3,4-dihydroxyfenylalanine (DOPA), 3,4-dihydroxybenzeenzuur, p-cresol, 4-methylcatechol, leucocyanidine, p-cumarinezuur, flavonolglycosiden .Deze reageren met zuurstof tot vorming van een quinone dat een typische bruine kleur heeft.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Appels, – ascorbinezuur(vitamine C) ,
- Thema: redoxreacties- biochemie
- Tijd:15 min
- Begrippen: enzymen – oxidatie
4.5.14. Fruitsapklok

- Info: Door de chemische reacties die optreden in de fruitsap ontstaat elektrische energie. Dit is een voorbeeld van een exo-energetische reactie met vorming van elektrische energie.
- Moeilijkheid: gemiddeld
- Chemische stoffen: fruitsap – 20 tot 30 cm magnesiumlint, aan één uiteinde opgerold rond b.v. een ijslollystokje; – 20 tot 30 cm koperdraad, aan één uiteinde opgerold;
- Thema: chemische reacties – energetische aspecten – redoxreactie – biochemie
- Tijd: 20 min
- Begrippen: exo-energetische reacties – galvanische cel
4.5.15. Dansende rozijnen

- Info: Hoe kunnen we rozijnen laten dansen? Eerst bruist het mengsel hevig en zien we een hevige gasvorming. Na enkele ogenblikken stijgen de rozijnen en dalen ze weer. Zolang als er gas aanwezig is, blijven de rozijnen deze beweging maken.
- Moeilijkheid: eenvoudig
- Chemische stoffen: rozijnen – halve eetlepel soda – ¼ bekertje azijn
- Thema: chemische reacties – anorganische stoffen – stofeigenschappen – biochemie
- Tijd: 20 min
- Begrippen: zouten – vorming van koolstofdioxide – massadichtheid
4.5.16. SO2 in gedroogd fruit

- Info: Hoe kan SO2 aangetoond worden in gedroogd fruit?Bij de gedroogde rozijnen en abrikoos wordt het loodacetaat-papier bruin en er is een geur van rotte eieren. Dit is een aanwijzing voor de aanwezigheid voor SO2.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Zn, – HCl 1 mol/l, H2O, l – loodacetaat-papier, – gedroogde abrikoos, gedroogde peer, gedroogde pruim,
- Thema: Anorganische stoffen – reactie stofklassen – biochemie
- Tijd: 25 min
- Begrippen: oxiden – identificatiereactie
4.5.17. pH afhankelijkheid kleurstoffen

- Info: Verandert de kleur van kersensap bij een verschillende pH? Als er een zuur wordt toegevoegd aan het kersensap wordt dit lichter, wordt er een base toegevoegd wordt het kersensap groen. Het kersensap krijgt dus een andere kleur bij een verschillende pH en kan als indicator gebruikt worden. De stof die zorgt voor de kleurverandering is anthocyaan.
- Moeilijkheid: eenvoudig
- Chemische stoffen: kersensap, – water, – zoutzuur 2mol/l, – natriumhydroxide 2 mol/l
- Thema: neutralisatiereactie – biochemie
- Tijd: 25 min
- Begrippen: pH indicatoren
4.5.18. Chemische regenboog in tomatensap

- Info: Het belangrijkste pigment in tomaten is het lycopeen. In de structuur zijn geconjugeerde electronensystemen aanwezig die blauwe kleur absorberen en daardoor een rode kleur hebben. Door additie met broom verkleint de lengte van het geconjugeerd systeem waardoor de geabsorbeerde golflengte verkort. Deze gaat uiteindelijk naar kleurloos.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Tomatensap – Broomwater (verzadigd)
- Thema: organische stoffen – organische reacties – biochemie
- Tijd: 20 min
- Begrippen:alkanen – radicalaire substitutie
4.5.19. Bepaling van het gehalte citroenzuur in een bloedrode sinaasappel

- Info: Hoeveel citroenzuur zit er in een bloedrode sinaasappel? De indicator die zich van naturen in bloedrode sinaasappels zit is anthocyaan. In zuur milieu kleurt deze rood; in basisch milieu kleurt deze blauw/groen.
De kleuromslag gebeurt bij de neutralisatie van de derde zuurfunctie met een pKz van 6,4. - Moeilijkheid: eenvoudig
- Chemische stoffen: NaOH 0,1 mol/l, – bloedrode sinaasappelsap,
- Thema: neutralisatiereactie – biochemie
- Tijd: 40 min
- Begrippen: titratie
4.5.20. Geraspte appel

- Info: Waarom verandert een geraspte appel van kleur? Een appel bestaat uit cellen. In die cellen zitten water en kleurstoffen die de appel zijn kenmerkende kleur geeft. In de cellen zit ook polyfenol. Wanneer de appel geraspt wordt, kan er lucht bij de stoffen komen. Als de zuurstof in aanraking komt met polyfenol, dan reageren ze tot o-quinon. Deze oxidatie wordt versneld door het enzym polyfenoloxidase. Het o-quinon reageert op zijn beurt met eiwitten waardoor de bruine kleur ontstaat.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Appel
- Thema: redoxreactie – biochemie
- Tijd: 10 min
- Begrippen: enzymen – oxidatie
4.5.21. Appelmummie

- Info: Hoe kunnen we oxidatie van een appel tegengaan? De hygroscopische werking van de zouten zorg ervoor dat al het vocht uit de appel gezogen wordt. De appel verdroogt volledig, dit voorkomt dat bacteriën zich kunnen ontwikkelen en houdt het rottingsproces tegen. Andere processen waar we dit principe tegen komen is bij het mummificeren van mensen (Egyptenaren,….), maar ook het drogen van vlees, en de zeer lang bewaarbare astronautenvoeding steunen op hetzelfde principe.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Appel – NaCl – NaHCO3 – Na2CO3
- Thema: redoxreactie – biochemie
- Tijd: 20 min
- Begrippen: enzymen – oxidatie
4.5.22. Droge vinger

- Info: Hoe komt het dat onze vingertop droog blijft als we onze vinger in het volgende glas water steken? De laag kruiden blijft op het water liggen. Als je met je vinger op de kruiden drukt, deuk je de waterlaag een beetje in, maar je komt niet met je vinger in het water. Dit komt doordat de bovenste laag van het water heel sterk is, dit wordt oppervlaktespanning genoemd. Water bestaat uit een heleboel watermoleculen, deze trekken elkaar heel sterk aan.
- Moeilijkheid: eenvoudig
- Chemische stoffen:Kruiden die drijven (Provençaalse kruiden, peper …) – Water – (lycopodiumpoeder)
- Thema: eigenschappen van stoffen – biochemie
- Tijd: 15 min
- Begrippen: polair en apolair
4.5.23. Zuurgehalte bepalen van appelen

- Info: Hoe kan je het zuurgehalte bepalen van appelen? Titratie met een sterke base
- Moeilijkheid: eenvoudig
- Chemische stoffen: 0.1 mol/l NaOH – pH elektrode of fenolftaleïne 0.05% oplossing in ethanol. – appelen
- Thema: neutralisatiereactie – biochemie
- Tijd: 40 min
- Begrippen: titratie
4.5.24. Aantonen fotosynthese van waterpest

- Info: Hoe kunnen we fotosynthese met waterpest aantonen? Planten doen aan fotosynthese omdat ze energie nodig hebben. Ze nemen hierbij koolstofdioxide en water op en onder invloed van licht zetten ze deze stoffen om in zuurstofgas en andere organische stoffen. Dit proces noemen we fotosynthese.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Waterpest – Natriumwaterstofcarbonaat (5 g/l)
- Thema: redoxreactie – biochemie
- Tijd: 40 min
- Begrippen: fotosynthese
4.5.25. Blauwe bessen als zuur-base indicator

- Info: Hoe kunnen we blauwe bessen als zuur-base indicator gebruiken? Het blauwe bessensap verkleurt in de verschillende oplossingen. In een zuur milieu, citroensap of azijn, geeft het een roze kleur. In een alkalisch milieu, NaHCO3-oplossing, kleurt het sap blauw.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Blauwe bessensap – Natriumwaterstofcarbonaatoplossing 10 g/ 100 ml oplossing – natriumhydroxide
- Thema:neutralisatiereactie – biochemie
- Tijd: 40 min
- Begrippen: titratie
4.5.26. Chromatografie van bladpigmenten

- Info: Hoeveel kunnen we de bladpigmenten in spinazie scheiden? Een groen blad heeft verschillende bladpigmenten. Elk pigment heeft maar een bepaalde hoogte tot waar de loopvloeistof het kan meenemen en dit afhankelijk van de stationaire fase. Dit zorgt er voor dat je een scheiding krijgt in de pigmenten.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Spinazie blaadjes – Aceton – Diëthylether
- Thema: scheidingstechnieken – biochemie
- Tijd:15 min
- Begrippen: chromatografie – papier chromatografie
4.5.27. De sinaasappel + ballon

- Info: Hoe kun je een ballon laten knallen met een sinaasappelschil? De ballon zal kapot springen als de sinaasappelschil er tegenaan komt. Dit komt doordat de schil van een sinaasappel limoneen bevat. Limoneen is een koolwaterstofverbinding die als olie voorkomt.
- Moeilijkheid: eenvoudig
- Chemische stoffen: sinaasappel
- Thema: organische stoffen – biochemie
- Tijd:15 min
- Begrippen: alkenen
4.5.28. Isoleren van DNA van een banaan

- Info: Hoe kunnen we DNA uit een banaan afzonderen? Het detergent, dat natriumdodecylsulfaat bevat, zorgt voor het vernietigen van de kernen en celmembranen (= lyse). De oorzaak van het vernietigen is de oppervlakte-actieve stof in het detergent. Deze stap is belangrijk omdat het DNA vrijkomt.
- Moeilijkheid: eenvoudig
- Chemische stoffen: banaan – ethanol
- Thema: organische stoffen – biochemie
- Tijd:40 min
- Begrippen: DNA
4.6. Citroen
4.6.1. Schuim maken met citroensap (raket).

- Info: Wat gebeurt er als we bakpoeder aan citroensap toevoegen? Bij toevoegen van bakpoeder aan citroensap/zuur wordt er schuim gevormd. Dit komt omdat er ook een gas gevormd wordt, namelijk CO2. Dit is afkomstig van het gevormde H2CO3 dat onstabiel is en spontaan splitst in H2O en CO2.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Citroensap (of citroenzuur) – bakpoeder
- Thema: anorganische stoffen – biochemie
- Tijd: 15min
- Begrippen: vorming van koolzuurgas
4.6.2. Identificatie citroenzuur

- Info: Hoe kunnen we citroenzuur aanduiden door identificatie van de functionele groepen? Het ceriumreagens wordt kleurloos als we citroenzuur toevoegen en troebel als we citroensap gebruiken. Het BTB wordt geel als we citroenzuur en citroensap gebruiken.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Cerium(IV)ammoniumnitraat – salpeterzuur 2mol/l – water – citroenzuur – broomthymolblauw – natriumloog – ethanol.
- Thema: organische stoffen – biochemie
- Tijd: 25 min
- Begrippen: carbonzuren – identificatiereactie
4.6.3. Citroenblauwdruk
- Info: Hoe kunnen we een blauwdruk maken met citroensap? Door ammoniumijzer(III)citraat te gebruiken (kan gemaakt worden met citroenzuur) als reductor, kan je Fe3+ reduceren naar Fe2+. De Fe3+ ionen zijn afkomstig van het gedissocieerde kaliumhexacynoferraat. Samen met Fe2+ kan het mengsel (groen) onder invloed van UV-licht een oplosbare vorm van Pruisisch blauw gemaakt worden.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Ijzer ammoniumcitraat, kaliumhexacyanoferraat
- Thema: chemische reacties – energetische aspecten – biochemie
- Tijd: 20 min
- Begrippen: endo-energetische reacties – fotolyse
4.6.4. Titratie met ascorbinezuur

- Info: Hoe kan je ascorbinezuur in een citroen doseren met een titratie? In de erlenmeyer wordt bij titreren dijood gevormd. Dijood is een indicator voor zetmeel. Bij aanwezigheid kleurt deze zwart. Ascorbinezuur is een zwak zuur maar toch een zuur. Deze geeft dus zijn H-atomen van zijn hydroxylgroepen af (aan de cyclische binding door negatief mesomeer effect) zodat de di-jood naar iodide-ionen kunnen vormen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: zetmeeloplossing 1% – ascorbinezuur – zwavelzuur 2mol/l – kaliumjodaat 0,03 mol/l – kaliumjodide 2 mol/l – gedestilleerd water
- Thema: redoxreactie – biochemie
- Tijd: 40 min
- Begrippen: titratie
4.6.5. Polyester uit citroenzuur
- Info:Hoe kan je een natuurlijk afbreekbaar polyester maken met citroenzuur? Door polycondensatie kan je met een organische stof (citroenzuur) een polyester maken.
- Moeilijkheid: eenvoudig
- Chemische stoffen: citroenzuur – glycerine
- Thema: kunststoffen – biochemie
- Tijd: 20 min
- Begrippen:polycondensatie – polyester
4.6.6. Reducerende werking ascorbinezuur (vitamine C).

- Info: Hoe kunnen we met een redoxreactie ascorbinezuur aantonen? Het ascorbinezuur zit in citroenen. Het heeft een reducerend vermogen en reduceert daarom het mangaan in het kaliumpermanganaat. Door de verandering van OT en uitwisseling van elektronen verandert de oplossing van kleur.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Ascorbinezuuroplossing 0,1% – kaliumpermanganaatoplossing 1% – zwavelzuur 1mol/l
- Thema: redoxreacties – biochemie
- Tijd: 20 min
- Begrippen: oxidatie
4.6.7. Citroenzuur en natriumcarbonaat.

- Info: Hoe kunnen we met een neutralisatiereactie citroenzuur aantonen? Door toevoegen van citroenzuur aan water, lost het citroenzuur op. Door de indicator gaat de kleur van de oplossing veranderen. De oplossing wordt zuurder. Door toevoegen van natriumcarbonaat gebeurt er een chemische reactie en verkleurt de oplossing weer
- Moeilijkheid: eenvoudig
- Chemische stoffen: universele indicator – citroenzuur – natriumcarbonaat en water
- Thema: neutralisatiereactie – biochemie
- Tijd: 40 min
- Begrippen: titratie
4.6.8. Olie in schil citroen.

- Info: Wat gebeurt er als je de olie uit schil van een citroen in een vlam spuit? Bij het uitknijpen van de citroenschil, zie je vonken in de vlam. Deze vonkjes zijn oranje van kleur.
- Moeilijkheid: eenvoudig
- Chemische stoffen: citroen
- Thema: organische stoffen – biochemie
- Tijd: 20 min
- Begrippen: alkenen
4.6.9. Citroenbatterij.

- Info: Hoe kunnen we een batterij maken met citroenen? Door de zure eigenschappen van een citroen (of citrusvrucht) is het mogelijk om een spanning op te wekken met behulp van 2 elektroden bestaande uit 2 metalen die samen een REDOX koppel vormen. De elektronen van de oxidator komen vrij en migreren naar de reductor.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Koperplaatje – Magnesiumplaatje of zinkplaatje – Citroen
- Thema: chemische reacties – energetische aspecten – redoxreactie – biochemie
- Tijd: 40 min
- Begrippen: exo-energetische reacties – galvanische cel
4.6.10. Roest verwijderen met citroenzuur.

- Info: Hoe kan je corrosie verwijderen met citroenzuur? Citroenzuur is een zwak zuur, dit verwijdert de oxidelaag op de muntjes. Het zout versnelt het proces door zijn chloride ionen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Citroensap of citroenzuur en zout
- Thema: neutralisatiereactie – redoxreactie – biochemie
- Tijd: 20 min
- Begrippen: corrosie – roest
4.6.11. Brandbare citrusvruchten

- Info: In welke citrusvruchten is de schil brandbaar? De schil bevatten terpenen ( limoneen), dit zijn vluchtige verbindingen. Terpenen bestaan vooral uit koolstof en waterstof. Terpenoïden, ook geurstoffen, bevatten ook zuurstof.
- Moeilijkheid: eenvoudig
- Chemische stoffen: diverse verse citrusvruchten
- Thema: organische stoffen – biochemie
- Tijd: 20 min
- Begrippen: alkenen
4.6.12. Isoleren van oliën uit citrusschillen

- Info: Hoe kunnen we makkelijk etherische olie uit de schil van een citrusvrucht halen? Door een stoomdestillatie kan je lichte fracties makkelijk mee destilleren zonder dat deze worden blootgesteld aan hogere temperaturen waardoor deze zouden gaan ontbinden.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Citrusschillen.
- Thema: scheidingstechnieken – biochemie
- Tijd: 20 min
- Begrippen: stoomdestillatie
4.6.13. Spitse spijker

- Info: Kunnen we het koper van een muntje aanbrengen op een spijker? Het koper van de munten reageert met het zuur van de citroen en vormt het kopercitraat. Als de spijker in de oplossing komt, bedekt de stof de spijker met een dun laagje, wat niet is af te wrijven.
- Moeilijkheid: eenvoudig
- Chzmische stoffen: 20 doffe koperen munten – Zout – 1 grote schone spijker
- Thema: enkelvoudige stoffen – redoxreacties – biochemie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – spanningsreeks van metalen
4.6.14. Stoomdestillatie op citrusschillen

- Info: Destillatie van geurstoffen uit citrusvruchtschillen. De destillatie verloopt via stoom.
- Moeilijkheid: gemiddeld
- Chemische stoffen: citrusvruchtschillen (100 g)
- Thema: scheidingstechnieken – biochemie
- Tijd:35 min
- Begrippen: destillatie – stoomdestillatie
4.6.15. Geheime boodschap met citroensap

- Info: Citroensap geeft een rode verkleuring van het rodekoolsap en daardoor zichtbaar.Een alternatief is de verhitting waarbij een thermolyse van het citroenzuur optreedt met vorming van koolstof
- Moeilijkheid: gemiddeld
- Chemische stoffen: rodekoolsap – citroensap
- Thema: neutralisatiereacties – biochemie
- Tijd: 15 min
- Begrippen: pH-indicator
4.6.16. Geef een schok

- Info: Kunnen citroenen, koperen munten en andere munten stroom geven? Het citroensap is een zure oplossing die de elektriciteit die gemaakt werd door de 2 verschillende metalen van de munten geleidt. Meestal gebruikt men koper en zink. De standaardpotentiaal voor koper en zink half-cel reacties die dan gebruikt worden
- Moeilijkheid: eenvoudig
- Chemische stoffen: een citroen – stroken keukenpapier van 2,5 cm op 5 cm – 5 koperen munten – 5 andere munten, niet koper of aluminiumfolie
- Thema: chemische reacties – energetische aspecten – redoxreactie – biochemie
- Tijd: 30 min
- Begrippen: exo-energetische reacties – galvanische cel
4.6.17. TLC van citroensap

- Info: Is citroensap een zuivere stof? Kunnen we citroensap opsplitsen in haar verschillende componenten en bepalen of het gaat om zuren of basen?
- Moeilijkheid: gemiddeld
- Chemische stoffen:
- Citroensap,
- Citroenzuur,
- Vitamine C,
- wijnsteenzuur,
- Broomthymolblauwoplossing,
- loopvloeistof (n-butanol/azijnzuur/water: 75/15/10) en geconc ammoniak.
Thema: scheidingstechnieken – biochemie
- Tijd:10 min
- Begrippen: chromatografie – papier chromatografie – TLC
4.6.18. Oplossen van kalksteen in citroensap
- Info: Is citroensap zuur genoeg om kalksteen op te lossen? et kalksteen reageert met het citroenzuur dat aanwezig is in het citroensap. Hierbij wordt CO2 gevormd. Deze vorming van CO2 zorgt voor de vertroebeling van het kalkwater door de vorming van calciumcarbonaat.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Gefiltreerd citroensap – Kalksteen (kleine blokjes) – Kalkwater
- Thema: anorganische en organische reacties – biochemie
- Tijd: 30 min
- Begrippen: vorming van koolzuurgas
4.6.19. Winnen van citroenschilolie

- Info: Kunnen we de olie die in citroenschillen zit ontginnen? Na het toevoegen van sudanrood-oplossing zien we duidelijk 2 laagjes. Het bovenste laagje, de citroenschilolie “drijft” bovenop de waterachtige oplossing. Er is slechts heel weinig citroenschilolie gevormd doordat er veel verloren gaat door verdamping. Het uitvoeren van deze proef door gebruik te maken van een destillatieopstelling zou een groter resultaat kunnen opleveren
- Moeilijkheid: eenvoudig
- Chemische stoffen: citroenschillen, – ijs, – sudan-rood oplossing
- Thema: stofeigenschappen – biochemie
- Tijd: 30 min
- Begrippen: polariteit
4.6.20. Citroenvulkaan

- Info: Wat ontstaat er bij de reactie tussen bakpoeder en citroensap? Vorming van koolzuurgas
- Moeilijkheid: eenvoudig
- Chemische stoffen: Citroensap – Bakpoeder
- Thema: reacties met gasvorming – biochemie
- Tijd: 15 min
- Begrippen: gasvorming – vorming van koolzuurgas
4.6.21. Conserveren met citroenzuur

- Info: Waarom worden in plakjes gesneden appels niet bruin als je er citroenzuur aan toevoegt? Wanneer de appel wordt gesneden, worden de cellen op het snijvlak vernietigd. Dit combineert stoffen die voorheen werden gescheiden door celwanden. Naast celwater komen vooral enzymen naar voren. Enzymen zijn stoffen die chemische processen kunnen versnellen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Appel – 5 g citroenzuur
- Thema: redoxreactie – biochemie
- Tijd: 15 min
- Begrippen: oxidatie – enzymen
4.7. Gisten
4.7.1. Bereiding van ethanol

- Info: Hoe kun je ethanol bereiden? Het sucrose hydrolyseert tot enkelvoudige suikers in oplossing en in aanwezigheid van gist
- Moeilijkheid: gemiddeld
- Chemische stoffen: 100 ml suikeroplossing 60 g/100ml – 2 g bakkersgist
- Thema: organische stoffen – biochemie
- Tijd: 20 min
- Begrippen: concentratie – vergisting
4.7.2. Gistkanon

- Info:De gistcellen gaan in deze oplossing zich vermenigvuldigen en eveneens starten met de vergistingsreactie waarbij de suikers omgezet worden naar ethanol en koolstofdioxide.De gevormde koolstofdioxide gaat opstapelen boven de oplossing en door de hoger wordende gasdruk wordt de stop weggeschoten.
- Moeilijkheid: gemiddeld
- Chemische stoffen: sucrose – gist
- Thema: biochemie
- Tijd: 20 min
- Begrippen: gisten – sucrose
4.7.3. Olifantenpasta voor kinderen

- Info:H2O2 ontbindt in H2O en O2. Het proces wordt gekatalyseerd door de aanwezigheid van gist.Het gist bevat namelijk het katalase enzym. Deze ontbinding is exotherm. Het gevormde zuurstofgas doet de oplossing schuimen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 10% H202 oplossing – Actieve gist
- Thema: biochemie
- Tijd: 20 min
- Begrippen: gisten – katalysator
4.7.4. Uitvoeren van het gistproces bij verschillende temperaturen

- Info: Wat is het effect van temperatuur op het gistingsproces? De ideale temperatuur bij het gistingsproces is 35 °C. Bij temperaturen die hoger liggen dan 40 °C zullen de gistcellen afsterven.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Bakkersgist – 10% glucoseoplossing
- Thema: biochemie
- Tijd: 30 min
- Begrippen: gisten – katalysator
4.7.5. Welke gisten vormen ééncellige schimmels?

- Info: Welk gas vormen eencellige schimmels (de gist)? Bakkersgist laten groeien en dan vorming van koolzuurgas aantonen
- Moeilijkheid: eenvoudig
- Chemische stoffen: bakkersgist – 100 mg NaH2PO4 – glucose – kalkwater – fft – olie
- Thema: biochemie
- Tijd: 30 min
- Begrippen: gisten – identificatie koolstofdioxide
4.7.6. Werking van benzoëzuur als conserveermiddel

- Info: Hoe kan een zuur ervoor zorgen dat een voedingsmiddel lang goed blijft? Benzoëzuur is een sterk conserveermiddel. Zijn werking is mogelijk door de zure eigenschappen. In een neutrale en lichte zure omgeving is het onwerkbaar. Na enkele uren is het kalkwater in het rechterstaal, zonder benzoëzuur, troebel geworden door de reactie van koolstofdioxide met het kalkwater.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Glucose – Gist – Natriumbenzoaat – Kalkwater – Verdund azijnzuur
- Thema: organische stoffen – biochemie
- Tijd: 25 min
- Begrippen: carbonzuren – conserveren
4.7.7. Tijdens de alcoholische gisting wordt CO2 gevormd
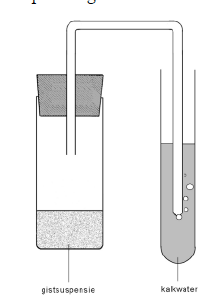
- Info: Wat wordt er bij het vergisten van suiker geproduceerd door gistcellen? Tijdens een alcoholische gisting wordt er glucose omgezet in ethanol en CO2. Het kalkwater wordt troebel in aanwezigheid van CO2.
- Moeilijkheid: eenvoudig
- Chemische stoffen: verse bakkersgist – 10 % glucoseoplossing
- Thema: organische stoffen – biochemie
- Tijd: 25 min
- Begrippen: gistingsproces
4.7.8. Kombucha

- Info: Hoe maak je een bioplastic met zwarte thee? Je maakt een bioplastic van thee door dat je een systeem creëert waarbij gist en bacteriën in symbiose met elkaar werken.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Warm water – Zwarte thee – Appel ciderazijn – Suiker
- Thema: kunststoffen- biochemie
- Tijd: 60 min
- Begrippen: bioplastics
4.8. Granen
4.8.1. Ijzer aantonen in cornflakes

- Info: Maak van het cornflakesmengsel een papje. Ga er overheen met een magneet. Je ziet dat er in de zak kleine zwarte deeltjes aangetrokken worden door de magneet.
- Moeilijkheid: gemiddeld
- Chemische stoffen: cornflakes
- Thema: enkelvoudige stoffen – stofeigenschappen – biochemie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – magnetisme – identificatiereactie
4.9. Honing
4.9.1. Zilverspiegel met honing

- Info:In een basisch milieu reageert fructose tot glucose De reactie met de basische zilveroplossing vormt een zilverspiegel
- Moeilijkheid: eenvoudig
- Chemische stoffen: honing – wijnsteenzuur – ethanol 96% – zilvernitraat – ammoniumnitraat – NaOH – water
- Thema: organische stoffen – biochemie
- Tijd: 25 min
- Begrippen: organische reacties – aldehyden – identificatiereactie
4.10. Planten en bloemen
4.10.1. Blauwe rozen
- Info:De kleurpigmenten in de rode roos veranderen door de pH. In zuur milieu zijn de pigmenten rood, in basisch milieu blauw.
- Moeilijkheid: eenvoudig
- Chemische stoffen: aceton – ammoniakoplossing 25% – rode half uitgebloeide rozen
- Thema: neutralisatiereactie – biochemie
- Tijd: 25 min
- Begrippen: pH indicator
4.10.2. Curcumapoeder als zuur base indicator

- Info:Hoe is curcumapoeder te gebruiken als indicator? Curcumarine is goed oplosbaar in alcohol en basen. Het neemt dan een roodbruine kleur aan
- Moeilijkheid: eenvoudig
- Chemische stoffen: Curcuma poeder – Water
- Thema: neutralisatiereactie – biochemie
- Tijd: 15 min
- Begrippen: pH indicator
4.10.3. Gekleurde bloem

- Info: Hoe kunnen we een witte bloem verkleuren? De inkt lost op in het water doordat het beide polaire stoffen zijn. De bloem neemt de volledige oplossing op en kleurt hierdoor blauw.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Witte bloem – Water – Inkt
- Thema: stofeigenschappen – biochemie
- Tijd: 15 min
- Begrippen: polariteit – capillariteit
4.10.4. Indicatoren in de tuin
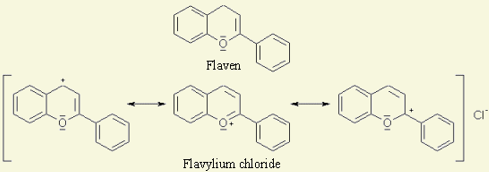
- Info: Anthocyanidines zijn planten kleurstoffen die in de cel vakuole gelokaliseerd zitten. Ze veroorzaken de rode, paarse en blauwe verkleuring van vele bloemen en fruitsoorten.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 100g plantenmateriaal
- Thema: stofeigenschappen – biochemie
- Tijd: 15 min
- Begrippen: pH-indicator
4.10.5. Aantonen fotosynthese van waterpest

- Info: Hoe kunnen we fotosynthese met waterpest aantonen? Planten doen aan fotosynthese omdat ze energie nodig hebben. Ze nemen hierbij koolstofdioxide en water op en onder invloed van licht zetten ze deze stoffen om in zuurstofgas en andere organische stoffen. Dit proces noemen we fotosynthese.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Waterpest – Natriumwaterstofcarbonaat (5 g/l)
- Thema: redoxreactie – biochemie
- Tijd: 40 min
- Begrippen: fotosynthese
4.10.6. Bloeiende bloemen

- Info: Hoe kunnen we papieren bloemen laten bloeien? Wanneer je het opgevouwen papier (de bloem) op water brengt zal het water naar boven stromen door het papier. Dit komt door de capillaire werking die het papier bezit. Het natte papier zal de vorm niet bewaren en de blaadjes spreiden zich uit.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Water – papier
- Thema: stofeigenschappen– biochemie
- Tijd: 20 min
- Begrippen: polariteit – capillariteit
4.11. Rode kool
4.11.1. pH bepalen m.b.v. rode koolsap

- Info: Hoe kun je rode koolsap gebruiken om te bepalen of een oplossing zuur, neutraal of basisch is? Je kunt rodekoolsap goed gebruiken als een indicator voor zuurgraden, want alle 3 keren toonde de rode koolsap de pH goed aan.Wanneer er meer protonen beschikbaar zijn doordat er een zuur aanwezig is, wordt de kleur van het rodekoolsap roder.Wanneer er weinig protonen beschikbaar zijn doordat er een base aanwezig is, wordt de kleur van het rodekoolsap geler.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Rode koolsap – Gedestilleerd water – Schoonmaakazijn (7 – 8 %) – Oplossing van soda
- Thema: neutralisatiereactie– biochemie
- Tijd: 20 min
- Begrippen: pH-indicatoren
4.11.2. Groengebakken ei d.m.v. rodekoolsap

- Info: Wat is het effect van rode koolsap bij het bakken van een ei? De pigmenten in de rode kool zijn anthocyanen. De anthocyanen veranderen van kleur door de pH-waarde. De rode kool is rood in zure omstandigheden en verandert naar blauw-groen in basisch mileu. Het ei-wit is alkalisch (pH 9) en wordt zo groen. De pH verandert wanneer we het eitje bakken, namelijk het wordt minder basisch. We zien dit aan de blauwere kleur.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Ei – Rode koolsap
- Thema: neutralisatiereactie– biochemie
- Tijd: 20 min
- Begrippen: pH-indicatoren
4.11.3. Geheime boodschap

- Info: Hoe kunnen we met rode koolsap een geheime boodschap schrijven? De kleurstof is paarsblauw. Dit komt omdat het rodekoolsap van nature een pH van 7 à 8 heeft. Maar in een zure vloeistof wordt het rodekoolsap rood. Citroensap is zuur en staat daarom protonen (H+) af. Deze reageren met het anhydrobase (de kleurstof in het rodekoolsap) en vormt zo flavylium cation. Dit heeft een rode kleur.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 400 gram rode kool (fijn gesneden) – 500 ml water – Citroensap
- Thema: neutralisatiereactie– biochemie
- Tijd: 15 min
- Begrippen: pH-indicatoren
4.11.4. Complexvorming rodekool

- Info: Hoe kunnen we complexen vormen m.b.v. rodekool? Kaliumaluminiumsulfaat en ijzertrichloride vormen samen met rodekoolsap complexen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Rodekoolsap – Magnesiumchloride – Aluin/aluminiumkaliumsulfaat – Ijzertrichloride
- Thema: neutralisatiereactie– biochemie
- Tijd: 15 min
- Begrippen: complexreacties – indicator
4.11.5. Ionuitwisseling aantonen met rodekoolsap

- Info: Welk resultaat krijgen we bij elektrolyse van rode koolsap? Aan de anode ontstaat een geel/groene kleur. Dit komt omdat er protonen worden vrijgemaakt waardoor het anhydrobase (pH = 6-7) reageert tot chalcone (pH > 8)Aan de kathode ontstaat een rode kleur. Dit komt omdat de protonen reageren met het anhydrobase ter vorming van flavylium cation.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Rodekoolsap
- Thema: redoxreacties– biochemie
- Tijd: 15 min
- Begrippen: elektrolyse – indicator
4.11.6. Indicatorpapier maken

- Info: Hoe kunnen we zelf indicatorpapier maken? Door een papier te impregneren met rodekoolsap. Kleurt roze wanneer we te maken hebben met een zuur en kleurt groen bij een basen. Rode koolsap is een goede universele indicator.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Rodekoolsap
- Thema: neutralisatiereactie– biochemie
- Tijd: 15 min
- Begrippen: pH-indicator – indicator
4.11.7. Kleurrijk schilderij maken

- Info: Hoe kunnen we een kleurrijk schilderij maken met melk en rode koolsap? Wanneer er meer protonen beschikbaar zijn doordat er een zuur aanwezig is, wordt de kleur van het rodekoolsap roder. Wanneer er weinig protonen beschikbaar zijn doordat er een base aanwezig is, wordt de kleur van het rodekoolsap geler.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Rode kool sap – HCl 0.1 mol/l – NaOH 0.1mol/l – NaHSO4
- Thema: neutralisatiereactie– biochemie
- Tijd: 15 min
- Begrippen: pH-indicator – indicator
4.11.8. Diffusie van een gas via microschaal

- Info: Hoe kunnen we diffusie aantonen met rode koolsap? De ammoniakdeeltjes gaan zich geleidelijk aan verspreiden volgens een willekeurige beweging. Dit ten gevolge van de kinetische energie die ze bezitten. Omdat ons aangezuurd rode koolsap een universele indicator is zullen we het diffusieproces van het ammoniak goed kunnen waarnemen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: rode koolsap – geconcentreerd ammoniak – enkele druppels van een zuur van 2 mol/l
- Thema: neutralisatiereactie– biochemie
- Tijd: 15 min
- Begrippen: pH-indicator – indicator
4.11.9. Lavalamp maken

- Info: Hoe kan je met een voedingsstof een lavalamp maken? Het bruistablet reageert met het water en maakt piepkleine belletjes koolzuurgas. De belletjes blijven aan de bubbels gekleurd water hangen en drijven naar de oppervlakte. Wanneer de belletjes uiteenspatten, zinken de gekleurde lavabubbels weer naar de bodem van de fles toe.Door dat we de fles gesloten hebben zal de CO2 aanwezig blijven. Dit zal zorgen voor daling van de zuurtegraad. We verkrijgen H2CO3 hierdoor kunnen we een kleurverandering waarnemen namelijk naar violet.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Rodekoolsap – Sla-olie – Bruistablet – keukenzout
- Thema: neutralisatiereactie– biochemie
- Tijd: 15 min
- Begrippen: pH-indicator – indicator
4.11.10. Basische drankjes met rode koolsap

- Info: Hoe kunnen we kleurrijke drankjes maken met behulp van koolsap? Basen zijn een protonacceptor en deze zullen protonen uit de omgeving van het rodekoolsap wegnemen. Hierdoor zal de kleurstof in het neutrale rodekoolsap, het anhydrobase, veranderen in chalcone. Dit heeft een groen/gele kleur afhankelijk van hoe basisch het natriumhydroxide is. (Hoe basischer, hoe geler.)
- Moeilijkheid: eenvoudig
- Chemische stoffen: Rodekoolsap – Zout – Suiker – Soda – Azijn (7-8%) – Citroensap – ammoniak
- Thema: neutralisatiereactie– biochemie
- Tijd: 25 min
- Begrippen: pH-indicator – indicator
4.12. Snoep Chocolade
4.12.1. Smeltcurve chocolade

- Info: Hoe ziet de smeltcurve van chocolade eruit? We plaatsen de proefbuis met chocolade in een warmwaterbad zodat de chocolade geleidelijk opwarmt. Hierdoor heb je een mooie smeltcurve om af te lezen. Doordat chocolade een mengsel van stoffen is, zien we een smelttraject op de smeltcurve.
- Moeilijkheid: eenvoudig
- Chemische stoffen: chocolade
- Thema:stofeigenschappen – biochemie
- Tijd: 15 min
- Begrippen: smelten – smeltcurve – smelttraject
4.12.2. De brandbaarheid van chocolade

- Info: Hoe kan je een theelichtje maken van chocolade? Door een stuk chocolade in de kaarsvlam te houden met behulp van een hittebestendige tang, verkolen we de chocolade. De verkoolde chocolade plaatsen we in de koelkast zodat de chocolade weer hard wordt. Deze is namelijk zacht geworden doordat het dicht bij een kaarsvlam gehouden is. Daarna houden we de verkoolde chocolade in de kaarsvlam. Dit doen we om het verkoolde gedeelte van de chocolade te doen ontvlammen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: chocolade – kaars
- Thema:stofeigenschappen – biochemie
- Tijd: 15 min
- Begrippen: brandbaarheid
4.12.3. Is het pure chocolade of melkchocolade?

- Info: Hoe kan een persoon die niet kan zien, pure chocolade van melkchocolade onderscheiden? De melkchocolade smelt eerder in je hand dan pure chocolade. Bij het afkoelen van gesmolten chocolade in heet water, zie je twee lagen ontstaan. Deze lagen zijn duidelijker zichtbaar bij melkchocolade.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Twee stukken melkchocolade – Twee stukken pure chocolade – Heet water uit de kraan
- Thema:stofeigenschappen – biochemie
- Tijd: 15 min
- Begrippen: soorten mengsels
4.12.4. Chocolade absorbeert aroma’s

- Info: Hoe komt het dat chocolade niet altijd naar chocolade ruikt? Chocolade is een absorptiemiddel die aroma’s absorbeert. De meeste geurstoffen zijn namelijk vet oplosbaar (zie onder: apolair) en in chocolade zit cacaoboter en eventueel melkvetten. Sommige geuren zullen beter opgenomen worden, bv. knoflook. Het aroma van knoflook is heel apolaire. Witte chocolade zal het beste aroma’s absorberen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Chocolade – ajuin, knoflook, pepermunt, mandarijn, citroen,
- Thema:stofeigenschappen – biochemie
- Tijd: 15 min
- Begrippen: absorptie
4.12.5. Onderscheid tussen chocolade en ‘dieetchocolade’

- Info: Hoe kunnen we chocolade onderscheiden van ‘dieetchocolade’? In het eerste deel van de proef gaan we chocolade laten smelten in aceton. Dit doen we omdat aceton vet oplost en wij willen het vet scheiden van de chocolade. Daarna filteren we het mengsel.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Verschillende soorten chocolade, – aceton,
- Thema: scheidingstechnieken – biochemie
- Tijd: 25 min
- Begrippen: filtratie – extractie
4.12.6. Chocolade: de zilverspiegel

- Info: Hoe reageert chocolade met Tollensreagens? De suikers in chocolade gaan ervoor zorgen dat de opgeloste Ag+-ionen in het Tollensreagens gaan reduceren tot zilveratomen. Hierdoor wordt er een zilverspiegel gevormd aan de wand van de proefbuis.
- Moeilijkheid: eenvoudig
- Chemische stoffen: AgNO3 (m%=10%), – NaOH (m%=10%), – NH3(Geconcentreerd), – Cacao met en zonder toegevoegde suikers, – Glucose, – H2O,
- Thema: redoxreactie- biochemie
- Tijd: 25 min
- Begrippen: suikers – reductie – aldehyden
4.12.7. Met chocolade de lichtsnelheid berekenen

- Info: Hoe berekenen we de snelheid van het licht met behulp van chocolade? We kunnen d.m.v. chocolade en een magnetron de lichtsnelheid ongeveer berekenen. We maten ongeveer 6 cm tussen de 2 smeltpunten. De golflengte is 2 keer deze afstand en hieruit berekende we de lichtsnelheid: en de frequentie is 2,45.109 /s. Hierdoor is de door ons berekende snelheid 297.106 meter per seconde.
- Moeilijkheid: moeilijk
- Chemische stoffen: magnetron – chocolade
- Thema: stofeigenschappen – biochemie
- Tijd: 15 min
- Begrippen: lichtsnelheid
4.12.8. Het kleuren van een cacao-oplossing

- Info: Hoe kunnen we chocolade donker en bleker maken? Soda zorgt ervoor dat een cacao-oplossing donkerder gaat kleuren
- Moeilijkheid: eenvoudig
- Chemische stoffen: Na2CO3 – bakcacao – ontkleuringzout (natriumdithioniet) – H2O
- Thema: redoxreactie – biochemie
- Tijd: 15 min
- Begrippen: kleurverandering
4.12.9. Chocolade als emulgator

- Info: Hoe werkt een emulgator in chocolade? Lecithine heeft een hydrofiele kop en een lipofiele staart. Hierdoor lost het zowel op in water als in olie. Als we water, olie en lecithine samenbrengen, zal de lecithine ervoor zorgen dat de oliedruppels fijn verdeeld worden in het water. Het is een emulgator.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Kookolie – water – paprikapoeder – lecithine
- Thema: stofeigenschappen – biochemie
- Tijd: 15 min
- Begrippen: emulsie – emulgator
4.12.10. Aminozuren aantonen met chocolade

- Info: Hoe kunnen we in een product (chocolade) aminozuren aantonen? De chocoladeoplossing kleurt violet met ninhydrine, terwijl de proefbuis zonder chocolade kleurloos blijft.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Ninhydrineoplossing – Volle melkchocolade – Gedestilleerd water
- Thema: biochemie
- Tijd: 15 min
- Begrippen: identificatie aminozuren
4.12.11. Chocolade en eieren verwarmen

- Info: Hoe kunnen we het verschil tussen een chemisch en fysisch verschijnsel aantonen met behulp van chocolade en eiwit?
- Moeilijkheid: gemiddeld
- Chemische stoffen: Chocolade – Eiwit van ei
- Thema:stofeigenschappen – biochemie
- Tijd: 20 min
- Begrippen: fysische en chemische reacties
4.12.12. Snoepjesbord

- Info: Wat gebeurt er wanneer je water bij gekleurd snoep voegt? Water heeft negatieve en positieve deeltjes net zoals de suikerlaag rondom de snoepjes. De positieve deeltjes van water gaan reageren met de negatieve deeltjes van de suikerlaag en omgekeerd. Zo gaan deze twee stoffen mengen en gaat de suikerlaag, dat gepaard gaat met een kleurstof, verspreiden.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Gekleurde snoepjes (M&M’s of Skittles) – Water
- Thema:stofeigenschappen – biochemie
- Tijd: 20 min
- Begrippen: oplosbaarheid
4.13. Gummibeertjes
4.13.1.Kleurstoffen in gummibeertjes

- Info: Hoe kunnen we kleurstoffen aantonen in gummibeertjes? De kleurstoffen in het gummibeertje bezitten vooral negatieve substituenten zoals een sulfonylgroep. Met de gepositiveerde eiwitten ontstaat een ionbinding die met water niet kan verbroken worden.Toevoeging van ammoniak verstoort de ionbinding en kan de kleurstof terug isoleren
- Moeilijkheid: eenvoudig
- Chemische stoffen: azijnzuuroplossing 1 mol/l (CH3COOH)opl – gekleurde gummibeertjes (van dezelfde kleur) – aceton (CH3COCH3)
- Thema: scheidingstechnieken– biochemie
- Tijd: 30 min
- Begrippen: adsorptie
4.13.2. Groeiende gummibeertjes

- Info: Hoe kunnen we een gummibeertje laten groeien eventueel laten krimpen? Als de gelatine in de gummibeer water opneemt, dan zwelt de gummibeer op. Hij wordt groter en zachter. Ook heeft hij een minder felle kleur, omdat evenveel kleurstoffen nu een grotere gummibeer moeten kleuren. Het opslorpen steunt op het principe van osmose
- Moeilijkheid: eenvoudig
- Chemische stoffen: gummibeertjes – water
- Thema: stofeigenschappen– biochemie
- Tijd: 10 min
- Begrippen: osmose
4.13.3. Gummy Bear Vuurwerk

- Info: Wat gebeurt er als we een gummy-beertje mengen met kaliumchloraat?
- Moeilijkheid:gemiddeld
- Chemische stoffen: Gummibeertjes – Kaliumchloraat – CuSO4
- Thema: chemische reacties – energetische aspecten – redoxreactie – biochemie
- Tijd: 20 min
- Begrippen: exo-energetische reacties – lichtvorming – oxidans
4.13.4.Blauwe fles met gummibeertjes

- Info: Hoe kunnen we een fles water blauw kleuren zonder gebruik te maken van de kleurstof aanwezig in de gummibeertjes? In deze experimentele opstelling, duurt het ongeveer 15 minuten, totdat de reactie start. Gedurende deze tijd, blijkt glucose uit de gummiberen in oplossing te gaan. In het alkalische milieu van glucose reduceert methyleenblauw tot het kleurloze leuko-methyleenblauw. De glucose wordt geoxideerd tot gluconzuur. Door krachtig schudden met de kleurloze oplossing diffundeert zuurstof in de oplossing en reoxideert de leuko-methyleenblauw naar methyleenblauw. De twee reacties gaan zo lang op tot de glucose volledig wordt toegepast of er geen zuurstofmeer aanwezig is.
- Moeilijkheid:gemiddeld
- Chemische stoffen: Gummibeertjes (geen rode) – Natriumhydroxide schilfers – methyleenblauwoplossing
- Thema: chemische reacties – redoxreactie – biochemie
- Tijd: 20 min
- Begrippen: klokreactie
4.13.5. Zilverspiegel met gummibeertjes

- Info: Hoe kunnen we een zilverspiegel/ afzetting van zilver aan de wand met behulp van een gummybeertje? Uit de zilvernitraatoplossing en de ammoniakoplossing wordt het Tollensreagens bereid. Hierbij worden zilverionen gecomplexeerd. Uit het gummibeertje lost langzaam glucose/sucrose op in water. Dit reduceert het complex van de zilverionen waarbij zilver ontstaat wat zich aan de wand afzet.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Zilvernitraatoplossing 0,1mol/l – Verdunde ammoniakoplossing – gummibeertje
- Thema: chemische reacties – biochemie
- Tijd: 20 min
- Begrippen: aldehyde – identificatie – suikers
4.13.6. Vruchtzuren in gummibeertjes
- Info: Wat is de pH van de verschillende gummibeertjes? We leiden uit de metingen af dat de pH van witte beertjes 3,8 bedraagt, de pH van gele en oranje beertjes 3,9 bedraagt , de pH van groene beertjes 4,0 bedraagt en de pH van rode beertjes 4,6 bedraagt
- Moeilijkheid: eenvoudig
- Chemische stoffen: gummibeertjes in verschillende kleuren
- Thema: neutralisatiereactie – biochemie
- Tijd: 20 min
- Begrippen: pH
4.13.9. Onverzadigde verbindingen in gummibeertjes

- Info: Hoe kunnen we dubbele bindingen in gummibeertjes aantonen? In gummibeertjes zijn onverzadigde verbindingen aanwezig met dubbele bindingen. Door additiereactie gebeurt de omzetting tot een halogeenalkaan. Hierdoor treedt er een kleurverandering op van het broomwater
- Moeilijkheid: eenvoudig
- Chemische stoffen: broomwater – kleurloos gummibeertje
- Thema: organische stoffen – biochemie
- Tijd: 20 min
- Begrippen: alkenen
4.13.10. Lijm uit gummibeertjes

- Info: Hoe kan je uit gummibeertjes lijm maken? In gummibeertjes zit gelatine. Door de gelatine absorbeert het gummibeertje water en wordt rekbaarder. Er zijn dus grote cohesiekrachten aanwezig tussen de moleculen van de oplossing en grote adhesiekrachten tussen de moleculen van de oplossing en het papier/karton.
- Moeilijkheid: eenvoudig
- Chemische stoffen: gummibeertjes – water
- Thema: kunststoffen – biochemie
- Tijd: 20 min
- Begrippen: intermoleculaire krachten
4.13.11. Rode gummibeertjes in een proefbuisje

- Info: Hoe kun je een grotere beer maken? Door osmosewerking in het polymeer
- Moeilijkheid: eenvoudig
- Chemische stoffen: Natriumalginaat-rodekoolsapmenging – 4 druppels zoutzuur geconcentreerd
- Thema: kunststoffen – biochemie
- Tijd: 20 min
- Begrippen: intermoleculaire krachten
4.13.12. Reductie van kaliumpermanganaat met gummibeertje

- Info: Hoe kleurveranderingen uitvoeren van een permanganaatoplossing met gummibeertjes. Door een aantal redoxreacties treedt er een kleurverandering op.
- Moeilijkheid: eenvoudig
- Chemische stoffen: KMnO4-oplossing (0,01 mol/l) – NaOH-oplossing (3 mol/l) – een gummibeer of glucosetabletje
- Thema: redoxreacties – biochemie
- Tijd: 20 min
- Begrippen: verschillende oxidatiegetallen van mangaan
4.13.13. Lichtgevende gummibeertjes

- Info: Waarom kunnen gummibeertjes oplichten?
- Moeilijkheid: eenvoudig
- Chemische stoffen: UV-lamp – Gummibeertjes
- Thema: energetische aspecten van chemische reacties – biochemie
- Tijd: 10 min
- Begrippen: exo-energetische reactie
4.13.14. Eiwitonderzoek in beertjes

- Info: Hoe kunnen we eiwitten aantonen in gummibeertjes? Na toevoeging van de kopersulfaatoplossing ontstaat een blauw-paarse kleur. Dit duidt op de aanwezigheid van eiwitten, hier is dat gelatine. De kopersulfaatoplossing (CuSO4)opl is een indicator op eiwitten op te sporen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: kopersulfaatoplossing 1% CuSO4opl – natriumhydroxideoplossing 10 % NaOHopl – gummibeertjes
- Thema: biochemie
- Tijd: 10 min
- Begrippen: eiwitten – identificatie
4.13.15. Productie van gummibeertjes

- Info: Kun je zelf gummibeertjes maken? Gelatine bestaat uit eiwitmoleculen die tot draden zijn gedraaid. Bij menging met water vormen zich bolletjes van deze eiwitdraden. Als deze eiwitballen worden verhit, scheiden de draden van elkaar en wordt het mengsel vloeibaar. Na afkoeling zijn de gelatinedraden met elkaar verbonden om een netwerk te vormen. Dit netwerk is flexibel. De water- , suiker- , kleur- en smaakmoleculen passen in de gaten in het netwerk
- Moeilijkheid: eenvoudig
- Chemische stoffen: 3 g citroenzuur – 15 g gelatine – 35 ml water – 20 g sucrose – 10 g honing – 30 g vruchtensiroop
- Thema: biochemie
- Tijd: 10 min
- Begrippen: eiwitten – mengsel
4.14. Algemeen
4.14.1. Endotherme reactie met zure hosties

- Info: Hoe kunnen we een endotherme reactie spontaan laten verlopen met een zure hostie? Meten van temperatuur bij toevoegen aan inhoud van een zure hostie.
- Moeilijkheid: eenvoudig
- Chemische stoffen:bakpoeder – wijnsteenzuur
- Thema: chemische reacties – energetische aspecten – biochemie
- Tijd: 10 min
- Begrippen: endo-energetische reacties – spontane reactie
4.14.2. Energetische waarde van pinda

- Info: Wat is de energetische waarde van pinda’s? Je bepaalt dit door de vrijgegeven warmte van een bepaalde hoeveelheid
- Moeilijkheid: eenvoudig
- Chemische stoffen: pinda’s
- Thema: thermodynamica – biochemie
- Tijd: 30 min
- Begrippen: energetische waarde
4.14.3. Extractie van olie uit pindanootjes met Soxhlet

- Info: Hoe kunnen we vet/olie isoleren uit pindanoten? Bij het toevoegen van water gebeurt geen visuele reactie. Er ontstaat wel een aantal olie-achtige druppels bovenop het water (breken het licht). Bij het toevoegen van ether gebeurt wel een visuele reactie, namelijk de ether wordt troebel. Dit wil zeggen dat de olie van de pindanoten oplost in ether, olie lost niet op in water.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Pindanoten – Ether – Water
- Thema: scheidingstechnieken – biochemie
- Tijd: 10 min
- Begrippen: extractie
4.14.4. Fluorescerende pudding

- Info: Door natriumdithioniet wordt het riboflavine door protonenafgifte naar een kleurloze verbinding gereduceerd. Het ditioniet wordt geoxideerd. Deze reactie verloopt ook omgekeerd zodat door opname van lucht de reactie omgekeerd verloopt.
- Moeilijkheid: gemiddeld
- Chemische stoffen: puddingpoeder van vanillesmaak – verzadigde natriumdithionietoplossing
- Thema: chemische reacties – energetische aspecten – biochemie
- Tijd: 15 min
- Begrippen: exo-energetische reacties – lichtvorming -fluorescentie
4.14.5. Gloeiende mentosfontein

- Info: Tonic ziet er kleurloos en helder uit onder normaal licht maar is helder gekleurd onder ultra violet licht.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Mentos – flesje tonic met kinine
- Thema: chemische reacties – energetische aspecten – biochemie
- Tijd: 15 min
- Begrippen: exo-energetische reacties – lichtvorming -fluorescentie
4.14.6. Kunstmatige kaviaar

- Info: Algenzuur is een kleurloze met carboxylgroepen polysaccharide welke men in bruinalgen vindt. In koud water zijn ze onoplosbaar, in warmer water eventueel aangezuurd, lossen ze op.De algenzuren worden gebruikt als verdikkingsmiddel in confituur, cosmetica, lijm, sauzen…Bij toedruppelen van de natriumalginaatoplossing komt het oppervlak van de druppels in contact met de kopersulfaatoplossing. Er vormt zich een onoplosbaar koperzout van het algenzuur.
- Moeilijkheid: eenvoudig
- Chemische stoffen: – kopersulfaat5.H2O – natriumalginaat
- gedestilleerd water
- Thema: kunststoffen – biochemie
- Tijd: 15 min
- Begrippen: bioplastics
4.14.7. Temperatuurmeting bij reactie met zure hosties

- Info: Hoe verloopt de temperatuur bij de reactie met zure hosties, wijnsteenzuur en bakpoeder?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Zure hosties – Wijnsteenzuur – Natriumwaterstofcarbonaat (NaHCO3)
- gedestilleerd water
- Thema: energetische aspecten van een reactie – biochemie
- Tijd: 15 min
- Begrippen: endo-energetische reactie
4.14.8. Suiker aantonen in kauwgom

- Info: Hoe kunnen we suiker aantonen in kauwgom? We kunnen het verschil in kauwgom aantonen door gist toe te voegen. Gist zet suiker om tot ethanol en koolstofdioxide. Dit is zichtbaar bij de suikerhoudende kauwgom. Koolstofdioxide nemen we waar door de belletjes die ontstaat en het Staalname potje en doordat de ballon licht opblaast.
- Moeilijkheid: eenvoudig
- Chemische stoffen: suikervrije kauwgom – suikerhoudende kauwgom – droge gist – water
- Thema: organische stoffen – biochemie – redoxreactie
- Tijd: 20 min
- Begrippen: enkelvoudige suikers – gistreactie
4.14.9. Snoepjes: gelatine of pectine?

- Info: Hoe kunnen we vaststellen of het geleermiddel in een snoepje gelatine of pectine is? Peptidebindingen in gummibeertjes vormen met kopersulfaat een violette complex zout . De kleur kan variëren van blauwviolet naar roodviolet afhankelijk van de hoeveelheid peptidebindingen. De kleurintensiteit is een maat voor de eiwitconcentratie.
- Moeilijkheid: eenvoudig
- Chemische stoffen: gummibeertjes – zure snoepjes – CuSO4-oplossing (0,1 mol/l) – NaOH-oplossing (3 mol/l)
- Thema: biochemie – chemische reactie
- Tijd: 10 min
- Begrippen: suikers – identificatie
4.14.10. Lijm uit gelatine

- Info: Hoe kunnen we verlijmen met gummibeertjes ? Gelatine ontbindt door de warmte en wordt terug hard bij het afkoelen.De water oplosbare gelatine wordt industrieel gewonnen uit het koken van haren, huid en beenderen van dieren. De gelatine ontstaat hierbij uit hydrolyse van het water onoplosbaar collageen. De kleefkracht berust op de cohesie tussen de macromoleculen van de kleefstof en de adhesie tussen kleefstoffen en te verlijmen materiaal.
- Moeilijkheid: eenvoudig
- Chemische stoffen: gummibeertjes – water
- Thema: biochemie – kunststoffen
- Tijd: 20 min
- Begrippen: intermoleculaire krachten
4.14.11. Zilveren snoepparels

- Info: Wat gebeurt er wanneer we snoepparels in een oplossing brengen? Zilver is een edel metaal en is hierdoor een (relatief) zwakke reductor. Zilver zal dus niet reageren met de meeste zure oplossingen. Het zal dus ook alleen zilverionen vormen in aanwezigheid van een sterke oxidator. Het nitraation aanwezig in salpeterzuur heeft de eigenschap dat het een sterke(re) oxidator is en dat het dus gemakkelijk met zilver reageert. Bij de reactie ontstaan zilverionen: Ag+. Als hieraan een oplossing van natriumchloride wordt toegevoegd, welke chloride-ionen bevat, slaat het slecht oplosbare zilverchloride neer onder vorm van een wit neerslag.
- Moeilijkheid: eenvoudig
- Chemische stoffen: zilveren snoepparels – salpeterzuur (65%) – natriumchloride (0,1 mol/l)
- Thema: biochemie – neerslagreacties
- Tijd: 20 min
- Begrippen: identificatie zilver
4.14.12. Extractie van vet uit een pindanoot

- Info: Wat gebeurt er tijdens de extractie van vet uit een pindanoot? Via de scheidingstechniek wordt vet geïsoleerd uit de noten.
- Moeilijkheid: gemiddeld
- Chemische stoffen: paprikachips – diethylether
- Thema: scheidingstechnieken – biochemie
- Tijd: 60 min
- Begrippen: extractie
4.14.13. Zetmeel in Smarties en M&M’s

- Info: Hoe kun je aantonen dat zetmeel aanwezig is in Smarties of M&M’s? Jodiumoplossing is een indicator die bruin/paars kleurt als deze in contact komt met zetmeel.
- Moeilijkheid: gemiddeld
- Chemische stoffen: M&M’s – Smarties – Jodiumoplossing
- Thema: chemische reacties – biochemie
- Tijd:15 min
- Begrippen: identificatie
4.14.14. Natuurlijke en kunstmatige kleurstoffen in levensmiddelen

- Info: Hoe kunnen we aantonen dat de kleurstoffen in onze levensmiddelen natuurlijk of kunstmatig zijn? NaOH laat natuurlijke kleurstoffen van kleur veranderen
- Moeilijkheid: gemiddeld
- Chemische stoffen: Verschillende soorten snoepjes – NaOH 0,1 mol/l
- Thema: neutralisatiereactie – biochemie
- Tijd:15 min
- Begrippen: identificatie – indicator
4.14.15. Papierchromatografie met M&M’s

- Info: Hoe bekom je (in groep) de mooiste chromatografie tekening met M&M? Maak een M&M vochtig door hem onder te dompelen in het water.
- Moeilijkheid: eenvoudig
- Chemische stoffen: TLC plaatje – 2 M&M’s – Aceton – Water
- Thema: scheidingstechnieken – biochemie
- Tijd:10 min
- Begrippen: chromatografie – papierchromatografie
4.14.16. Exploderende bonbons

- Info: Wat ontstaat er wanneer je suiker, citroenzuur en bakpoeder samenvoegt? Er wordt CO2 gevormd door reactie tussen bakpoeder en citroenzuur indien contact met water. Hierdoor knettert het in de mond.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Suiker – Citroenzuur – Bakpoeder
- Thema:chemische reactie – biochemie
- Tijd:10 min
- Begrippen: vorming van gassen
4.14.17. pH van zure snoepjes

- Info: Wat nemen we waar wanneer we een “zure mat” snoepje in water doen? De zure snoepjes bevatten citroenzuur als deze in contact komen wat water lost dit op in het water en daalt de pH van dit water.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Zure maten – Gedemineraliseerd water
- Thema: neutralisatiereactie – biochemie
- Tijd:10 min
- Begrippen: pH-meting
4.15. Soda en bakpoeder
4.15.1. Bereiding van keukenzout uit soda

- Info: Hoe kunnen we keukenzout bereiden uit soda? Na toevoeging van het zoutzuur ontstaat er CO2 gas dat verdwijnt en een NaCl –oplossing. Het water verdampt door kristallisatie en er ontstaan NaCl kristallen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Soda (Na2CO3) – HCl (2 mol/l)
- Thema: neutralisatiereactie – biochemie
- Tijd:10 min
- Begrippen: reactie zout en zuur
4.15.2. Zijn alle zuren even sterk?

- Info: Hoe kunnen we een verschil in zuursterkte tussen 2 verschillende zuren aantonen? We kunnen een verschil in zuursterkte aantonen door de zuren te laten reageren met eenzelfde base. Bij het sterkste zuur, in dit geval HCl, zal de reactie sneller verlopen (sneller opblazen van de ballon).
- Moeilijkheid: eenvoudig
- Chemische stoffen: 0,8 g bakpoeder (NaHCO3) (2 * 0,4 g) – 8 ml Azijnzuuroplossing (1 mol/l) – 8 ml HCl-oplossing (1 mol/l)
- Thema: neutralisatiereactie – biochemie
- Tijd:10 min
- Begrippen: zuursterkte
4.15.3. Blauw geheimschrift

- Info: Hoe kunnen we een geheimschrift ontwikkelen m.b.v. natriumcarbonaat? Thymolftaleïne is een indicator die kleurloos is in zuur milieu en blauw kleurt in basisch milieu. Natriumcarbonaat vormt OH– ionen in water. Dit verklaart waarom we een blauwe kleur verkrijgen bij het samenvoegen van de thymolftaleïne -oplossing en de basische natriumcarbonaat-oplossing.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Thymolftaleïne – Ethanol – Natriumcarbonaat – Gedestilleerd water – Natriumhydroxide-oplossing (NaOH, 1 mol/l)
- Thema: neutralisatiereactie – biochemie
- Tijd:10 min
- Begrippen: identificatiereactie – indicator
4.15.4. Cola met soda

- Info: Wat gebeurt er als we soda en cola samenvoegen? Het voedseladditief E338, fosforzuur, gaat reageren met de soda. Hierbij ontstaat het gas koolstofdioxide. Zo komt het dat het mengsel gaat bruisen en stijgen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Grote lepel Soda (Na2CO3) of bakpoeder – 75 ml cola
- Thema: neutralisatiereactie – biochemie
- Tijd:10 min
- Begrippen: reactie zout en zuur
4.15.5. Endotherme reactie met soda

- Info: Hoe kunnen we temperaturen behalen onder de nul graden Celsius m.b.v. natriumcarbonaat? In het proefje is de vorming van het koolzuurgas de oorzaak van de voortstuwing. Deze reactie onttrekt energie uit de omgeving, in dit geval het water, hetgeen waargenomen kan worden door het meten van een dalende temperatuur.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Natriumcarbonaat (10 aq) (Na2CO3.10H2O) = soda – Citroenzuur
- Thema: energetische aspecten – biochemie
- Tijd:15 min
- Begrippen: endo-energetische reactie
4.15.6. Kleurrijk geschrift

- Info: Hoe kunnen we een geheimschrift maken in meerdere kleuren dat zichtbaar wordt door te besproeien met slechts één stof? Door een boodschap te schrijven met verschillende stoffen die allemaal een andere kleur complex of neerslag vormen, bij het besproeien met eenzelfde stof.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Vernevelaar – IJzer(III)chloride (6 aq) (FeCl3.6H2O) – Kaliumhexacyanoferraat(II) (3 aq) (K4Fe(CN)6.3H2O) – Kaliumthiocyanaat (KSCN) – Tannine – Salicylzuur (C6H4(OH)COOH) – Natriumcarbonaat (Na2CO3) – Ethanol (C2H5OH)
- Thema: chemische reactie – redoxreacties – biochemie
- Tijd:35 min
- Begrippen: complexreacties – redoxreacties
4.15.7. Kleurveranderingen en reactiesoorten met soda

- Info: Welke soorten reacties kunnen aangetoond worden met behulp van soda? Redox- en neutralisatiereacties met telkens kleurveranderingen
- Moeilijkheid: gemiddeld
- Chemische stoffen: Koper(II)sulfaat (5 aq) (CuSO4.5H2O) – Lugol – Rode koolsap – Natriumcarbonaat (0 aq) (Na2CO3) – Gedestilleerd water – Tafelazijn – Calciumdihydroxide (Ca(OH)2)
- Thema: chemische reactie – redoxreacties – biochemie
- Tijd:35 min
- Begrippen: complexreacties – redoxreacties – indicator
4.15.8. Ontleding van bakpoeder tot soda

- Info: Welk gas ontstaat er bij de thermolyse van bakpoeder? Bij de thermolyse van bakpoeder ontstaat het gas koolstofdioxide, dat we aantonen met behulp van kalkwater.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Kalkwater – Bakpoeder (NaHCO3)
- Thema: chemische reactie – biochemie
- Tijd:35 min
- Begrippen: ontledingsreactie
4.15.9. Zelf rennie maken

- Info: Hoe kunnen we zelf tabletten tegen maagzuur maken? Bij het samenbrengen van CaCl2 en Na2CO3 wordt er een neerslag gevormd: CaCO3.Deze stof is basisch en kunnen we gebruiken om het zuur te neutraliseren. Net zoals het maagzuur wordt geneutraliseerd met behulp van een rennie
- Moeilijkheid: eenvoudig
- Chemische stoffen: 1g Soda (Na2CO3) – 1g CaCl2 – HCl -oplossing (0,1 mol/l)
- Thema: chemische reactie – biochemie
- Tijd:15 min
- Begrippen: synthesereacties – reactie zouten en zuren
4.15.10. Schuim in een glas

- Info: Hoe kunnen we het schuim bij champagne namaken? Als je azijn en bakpoeder bij elkaar doet, ontstaat CO2. Het gas en het afwasmiddel vormen samen kleine zeepbelletjes, waardoor het lijkt alsof champagne is bekomen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 3g bakpoeder – 20ml huishoudazijn – Geel afwasmiddel
- Thema: chemische reactie – biochemie
- Tijd:15 min
- Begrippen: gasvorming
4.16. Vitamine C
4.16.1. Dosering van vitamine C door redoxtitratie

- Info: Hoe kunnen we gehalte vitamine C bepalen? Jodaat vormt met jodide in een zure oplossing jood.Ascorbinezuur is in oplossing makkelijk te oxideren tot dehydro-ascorbinezuur. Als oxidator kan een joodoplossing gebruikt worden:
- Moeilijkheid: gemiddeld
- Chemische stoffen: vitamine C tabletten – zwavelzuur 2 mol/l – KI oplossing 2 mol/l – KIO3 oplossing 0.03 mol/l – zetmeeloplossing
- Thema: redoxreactie – biochemie
- Tijd: 40 min
- Begrippen: titratie
4.16.2. Dosering van vitamine C: via zuurbasetitratie

- Info: Hoe kunnen we gehalte vitamine C bepalen? Vitamine C tabletten bestaan meestal uit ascorbinezuur (C6H8O6) en een bindmiddel zetmeel. Het ascorbinezuur is een éénwaardig zuur. De pKz waarde bedraagt 4.17.
- Moeilijkheid: gemiddeld
- Chemische stoffen: vitamine C tabletten – NaOH 0.1 mol/l – fft
- Thema:neutralisatiereactie – biochemie
- Tijd: 40 min
- Begrippen: titratie
4.16.3. Elektrisch kleuren

- Info: Hoe tonen we de elektrolyse van KI aan? Ascorbinezuur is een sterke reductor en dringt daarom weer elektronen op aan het jodium. Daarmee verdwijnt de blauwe kleur weer. Met niet te veel reductor in de oplossing, wordt hij helemaal verbruikt en ontstaat terug jodium door de elektrische stroom
- Moeilijkheid: gemiddeld
- Chemische stoffen: Water (H2O): 150 mL – Kaliumjodide (KI): ½ gram – Ascorbinezuur (C6H8O6): 0,1 gram – Stijfsel-oplossing (0,2%): 5 mL
- Thema: redoxreactie – biochemie
- Tijd: 20 min
- Begrippen: elektrolyse
4.16.4. Groen blauwe kolf

- Info:In het experiment wordt de geoxideerde vorm van methyleenblauw MB+ door ascorbinezuur gereduceerd naar MBH2+ en vervolgens door luchtzuurstof weer geoxideerd tot MB+. De zuurstof wordt door het schudden in de oplossing gebracht. Bij staan reduceert het ascorbinezuur MB+ terug naar zijn kleurloze vorm. Cu2+ ionen katalyseren deze laatste reactie
- Moeilijkheid: gemiddeld
- Chemische stoffen: zuiver vitamine C in poedervorm – oplossing van methyleenblauw in ethanol (0.1 g in 100ml ethanol 70%) – kopersulfaatoplossing 1,6 massa%
- Thema: chemische reacties – complexreactie – redoxreactie – chemisch evenwicht – reactiesnelheid – biochemie
- Tijd:20 min
- Begrippen: stofveranderingen – complexreacties – oscillerende reactie
4.16.5. Magische hand

- Info:Hoe kunnen we met onze hand oplossingen van kleur doen veranderen?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Zetmeeloplossing van 1% – Vitamine C of ascorbinezuur – Lugol-oplossing
- Thema:biochemie – chemische reacties
- Tijd: 25 min
- Begrippen: zetmeel – identificatiereactie
4.16.6.pH doorlopen met een gas

- Info: Wat gaat er gebeuren als je een bruistablet in de broomthymolblauwoplossing laat vallen? De kleur van de basische broomthymolblauwoplossing gaat van blauw naar geel door toevoeging van de bruistablet. Dit komt doordat de bruistablet koolzuurgas vrijlaat en samen met water vormt dit waterstofcarbonaat (H2CO3). Dit is een zuur.Door de beker een tijdje te laten staan krijgen we een neutraal milieu. Dit kunnen we zien aan de groene kleur en verklaren doordat het koolzuurgas de zure oplossing gaat neutraliseren.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Bruistablet – Broomthymolblauwoplossing
- Thema:biochemie – neutralisatiereacties
- Tijd: 15 min
- Begrippen: indicator– identificatiereactie
4.16.7. Zwart wit geeft kleurloos

- Info:Hoe kan bij het samenvoegen van een witte en een zwarte oplossing, een kleurloze oplossing worden gevormd? Verschillende redoxreactie treden op met telkens een kleurverandering
- Moeilijkheid: gemiddeld
- Chemische stoffen: 10 ml joodtinctuur – 90 ml azijn – ascorbinezuur opgelost in 30 ml water – zetmeeloplossing – 15 ml hypochloriet in 45 ml water (=javel) – 150 ml water – een halve theelepel magnesiumsulfaat – huishoudammoniak 1 mol/l
- Thema: chemische reacties – redoxreacties – complexreactie – biochemie
- Tijd:35 min
- Begrippen: stofveranderingen – kleurveranderingen
4.16.8. Vitamine C detectie

- Info:Welke voedingsmiddelen (fruit, groenten) bevatten veel vitamine C? De teststrips bevatten waarschijnlijk een mengsel van kaliumjodaat en zetmeel in hun testgebied . Omdat ascorbinezuur (vitamine C) een krachtig reducerend middel is, wordt jodaat teruggebracht naar kaliumjodide . Kaliumjodide vormt samen met het zetmeel het karakteristieke blauwviolette jodium- zetmeelcomplex.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Appel – Wortel – Paprika – Citroen – 4 vitamine C teststicks
- Thema: chemische reacties – biochemie
- Tijd:35 min
- Begrippen: identificatie – kleurveranderingen
4.17.Vlees en vis
4.17.1.Chitine in schaaldieren
- Info:De schalen van krabben, kreeften en garnalen bestaan voor een groot deel uit calciumcarbonaat. Chitine is een polymeer van N acetyl-D-glucosamine. Met een eenvoudige proef is dit chitinegehalte in schalen te bepalen. Los eerst de schaal op in verdund zuur. Er blijft eiwit over. Dit eiwit los je deels op door koken in een natriumhydroxideoplossing. Uiteindelijk blijft chitine over. Met ether en alcohol maak je de chitine watervrij.
- Moeilijkheid: gemiddeld
- Chemische stoffen: schalen van krabben, kreeften of garnalen – 50 ml HCl-opl 2mol/l – 50 ml NaOH-opl 1mol/l – norvanol D (ethanol 96% + ether)
- Thema: scheidingstechnieken– biochemie
- Tijd:35 min
- Begrippen: identificatie – extractie
4.18. Zout
4.18.1.Bereiding van keukenzout uit soda

- Info: Hoe kunnen we keukenzout bereiden uit soda? Na toevoeging van het zoutzuur ontstaat er CO2 gas dat verdwijnt en een NaCl –oplossing. Het water verdampt door kristallisatie en er ontstaan NaCl kristallen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Soda (Na2CO3) – HCl (2 mol/l)
- Thema: neutralisatiereactie – biochemie
- Tijd:10 min
- Begrippen: reactie zout en zuur
4.18.2. Invloed van temperatuur bij het oplossen van een stof

- Info: Hoe heeft de temperatuur een invloed bij een oplossen van een stof? Door zout in water te doen gaat deze ook zijn intermoleculaire krachten verliezen. Deze zoekt een evenwicht tussen de intermoleculaire krachten van het oplosmiddel (water). Net zoals bij het smelten van een vaste stof, zal ook bij het oplossen van een vaste stof de temperatuur een invloed hebben. Door een hogere temperatuur zullen de intermoleculaire krachten tussen de zout-deeltjes sneller verbroken worden waardoor deze bij een warm water sneller zal oplossen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: water – keukenzout
- Thema: oplosbaarheid – biochemie
- Tijd:10 min
- Begrippen: invloed van temperatuur op de oplosbaarheid
4.18.3. Peper en zout scheiden

- Info: Hoe kunnen we zout en peper van elkaar scheiden? Als je over de ballon wrijft met je trui of met een stok, wordt de ballon elektrisch geladen. De peper voelt dat. Daarom wil de peper naar de ballon toe. De peperkorrels zijn klein en licht. De zoutkorrels voelen de aantrekking van de ballon ook, maar ze zijn groter en zwaarder dan de peperkorrels.
- Moeilijkheid: eenvoudig
- Chemische stoffen: water – keukenzout
- Thema: bouw van atomen– biochemie
- Tijd:10 min
- Begrippen:elektrostatica
4.18.4. Zoutbatterij

- Info: Hoe is het mogelijk om met zout een batterij te maken? Natrium ionen (Na+) stromen richting de koper elektrode om daar de OH- ionen te neutraliseren, analoog stromen de chloride ionen (Cl–) richting aluminium elektrode om de OH– ionen te vervangen die geconsumeerd worden. Het resultaat is dat elektronen bewegen van de koper naar de aluminium elektrode.
- Moeilijkheid: eenvoudig
- Chemische stoffen: koperen munten – aluminiumpapier – keukenzout
- Thema: redoxreactie – biochemie
- Tijd:20 min
- Begrippen: galvanische cellen
4.18.5. Scheiden van plastiek met keukenzout

- Info: Hoe kunnen we verschillende soorten plastiek om de beurt uit water halen? De verschillende soorten plastiek hebben ieder een andere massadichtheid.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Keukenzout (NaCl) – PE ( vb. inpakfolie ) – PP ( vb. plastiek mapje voor in ringmappen ) – PVC ( vb. afvoerbuizen of tuinslangen ) – PS ( vb. wegwerp koffiebekers of piepschuim ) – PET ( vb. flessen van prik houdende dranken )
- Thema: kunststoffen – biochemie
- Tijd:20 min
- Begrippen: massadichtheid
4.18.6. Kristallisatie in snel tempo

- Info: Hoe kunnen we op een snellere manier zoutkristallen maken? NaOH is een base en HCl is een zuur, wanneer deze reageren met elkaar wordt er NaCl en H2O gevormd (neutralisatiereactie). Doordat deze stoffen zeer geconcentreerd zijn, komt er ook warmte vrij (reactie-enthalpie) zodat het water sneller kan verdampen. De vrije ionen Na+ en Cl– kunnen zo in een ionenrooster geplaatst worden. Door het gebruik van de hoge concentraties ga je zodanig veel zout maken dat de zoutoplossing (je reactieproduct) verzadigd raakt en je dus het gevormde zout kan zien.
- Moeilijkheid: eenvoudig
- Chemische stoffen: NaOH 40% = 10mol/l – HCl (geconcentreerd 37% ~ 10.5 mol/l)
- Thema: scheidingstechnieken – biochemie – neutralisatiereactie
- Tijd:10 min
- Begrippen: kristallisatie – reactie zuur en base
4.18.7. Zout doet water bruisen

- Info: Hoe kunnen we aantonen dat er in bruiswater dat lang openstaat nog steeds een gas aanwezig is? Het opgeloste CO2 is apolair. Deze wordt ingesloten de polaire watermoleculen. Door de vanderwaalskrachten tussen beide stoffen zal er nog altijd CO2 aanwezig zijn in het water. Als er zout wordt toegevoegd ontstaan er ion-dipoolkrachten tussen de zoutionen en de waterdipolen. Deze krachten ontstaan, omdat water en zout beide een partieel positieve en negatieve lading hebben. Het zout zal dus de plaats innemen van het CO2.
- Moeilijkheid: eenvoudig
- Chemische stoffen: NaOH 40% = 10mol/l – HCl (geconcentreerd 37% ~ 10.5 mol/l)
- Thema: neutralisatiereactie
- Tijd:10 min
- Begrippen: intermoleculaire krachten
4.18.8. pH verschillen van zouten aangeven met gelatine

- Info: Hoe kunnen met gelatine het verschil in pH van primaire, secundaire en tertiaire fosfaten aantonen? Wat in de gelatine gebeurt, is niet alleen het oplossen van een zout in water. In de gelatine zit ook universeelindicator die een reactie aangaat met de gevormde ionen. Er worden steeds Na+ ionen gedissocieerd, deze beïnvloeden de pH niet (ze zijn afkomstig van een sterk base NaOH). De negatieve ionen zorgen dus voor het verschil in pH-waarde. Deze negatieve ionen (H2PO4– of PO43-) gaan een reactie aan met water. Zo worden er H+ of OH– als reactieproduct gevormd waardoor het milieu respectievelijk zuur of basisch wordt. De universeelindicator neemt in ieder milieu een andere kleur aan.
- Moeilijkheid: eenvoudig
- Chemische stoffen: NaH2PO4 – Na3PO4 – Na2HPO4 – Universeelindicator – NaCl
- Thema: neutralisatiereactie – biochemie
- Tijd:10 min
- Begrippen:pH-indicator
4.19. Additieven in de voeding
4.19.1. Smeltkaas maken

- Info: Hoe kun je smeltkaas maken?Bij smeltkaas wordt kaas gesmolten met smeltzouten. Smeltkazen kunnen in verschillende vormen voorkomen. Als smeltzouten dienen natrium- en kaliumfosfaten, polyfosfaten, natrium- of kaliumcitraat en natriumalginaat.In gewone kaas komt eiwit voor als vooral calciumcaseïnaat.
- Moeilijkheid: eenvoudig
- Chemische stoffen: boter – water – kaas – smeltzout
- Thema: mengsels – biochemie
- Tijd:30 min
- Begrippen: vorming van een mengsel
4.19.2. Onderzoek van fosfaten in worst

- Info: Hoe werken fosfaten in voedingsmiddelen? Worsten en smeltkaas bevat fosfaten en pyrofosfaten. Fosfaten hebben een waterbindend vermogen en beïnvloeden de pH.Verder hebben de fosfaten een emulgerende werking waarbij een gelering optreedt en een kleurverandering wordt verhindert. Ammoniummolybdaat is in een zure omgeving een reagens dat fosfaten aantoont. Het vormt een gele neerslag.
- Moeilijkheid: eenvoudig
- Chemische stoffen: vlees – ammoniummolybdaat
- Thema: neerslagreactie – biochemie
- Tijd:20 min
- Begrippen: identificatie
4.19.3. Koolzuurgas vormen uit bakpoeder

- Info: Hoe werkt een rijsmiddel? Vrijzetting van koolzuurgas door verhitten
- Moeilijkheid: eenvoudig
- Chemische stoffen: water – bakpoeder – kalkwater
- Thema: gasvormingsreactie – biochemie
- Tijd:20 min
- Begrippen: identificatie
4.19.4. Verdikkingsmiddelen

- Info: Hoe werkt een verdikkingsmiddel? Als verdikkingsmiddelen zijn er gelatine, agar, zetmeel, carragenan.Het meest gebruikte is gelatine, te bekomen uit eiwitten van uitgekookte knoken. Een alternatief is carragenan, polysacchariden uit de celwanden van rode algen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Gelatine – Carrageen – Zetmeel – Lugoplossing
- Thema: biochemie
- Tijd:20 min
- Begrippen: identificatie – suikers – eiwitten
4.19.5. Emulgatoren
- Info: Hoe werkt een emulgator? Eieren worden veel gebruikt in de keuken. De belangrijkste bestanddelen van mayonaise zijn olie en water. Beide stoffen mengen niet met elkaar. Het eigeel bevat lecithine, een molecuul met een hydrofiele en een hydrofoob gedeelte. Dit molecule omsluit het oliedeel in de mayonaise en laat toe dat deze oliedeeltjes zich kunnen verdelen in de waterfase.
- Moeilijkheid: eenvoudig
- Chemische stoffen:Eigeel – Tafelazijn – Mosterd – Zonnebloemolie – Zout
- Thema: biochemie
- Tijd:20 min
- Begrippen: mengsel – emulsie – emulgator
4.19.6. Werking van benzoëzuur
- Info: Hoe werkt benzoëzuur? Benzoëzuur is een sterk conserveermiddel vooral in een sterk zuur milieu
- Moeilijkheid: eenvoudig
- Chemische stoffen: glucose -benzoëzuur – gist – kalkwater
- Thema: biochemie
- Tijd:20 min
- Begrippen: mengsel – conserveermiddel
4.19.7. Sorbinezuur als conserveermiddel

- Info: Hoe werkt het conserveermiddel sorbinezuur? Een aantal organismen kunnen sterk giftige stoffen vormen. Daarvoor zijn conserveermiddelen zoals sorbinezuur toegelaten.
- Moeilijkheid: eenvoudig
- Chemische stoffen: gelatine -aspic – kaliumsorbaat – tafelazijn
- Thema: biochemie
- Tijd:20 min
- Begrippen: mengsel – conserveermiddel
4.19.8. Bepaling van suikergehalte in limonade

- Info: Wat is het suikergehalte in limonade? Lost men suiker op in water dan heeft dit effect op de dichtheid. De dichtheid van zuiver water bedraagt 1g/cm³. De dichtheid van een suikeroplossing is hoger. Daar andere stoffen in de limonaden de dichtheid beperkt beïnvloeden (buiten koolzuurgas) kan men via de dichtheid het suikergehalte bepalen. Als maatstaf kan de hoeveelheid uitgedrukt worden in massaconcentratie.
- Moeilijkheid: eenvoudig
- Chemische stoffen: limonade
- Thema: biochemie
- Tijd:20 min
- Begrippen: dosering – massadichtheid
4.19.9. Bepaling van het alcoholgehalte in alcopops

- Info: Wat is het alcoholgehalte in alcopops? Om het alcoholgehalte in alcopops te bepalen is een destillatie-opstelling nodig. Hierbij wordt het alcohol in de alcopops over gedestilleerd als een derde is overgeheveld van de vloeistof. Het alcoholgehalte kan dan met een alcoholmeter worden bepaald.
- Moeilijkheid: eenvoudig
- Chemische stoffen: tannine – alcopops
- Thema: biochemie – scheidingstechnieken
- Tijd:30 min
- Begrippen: dosering – destillatie
4.19.10. Verhogen van de sapopbrengst met pectinase

- Info: Hoe kan je de sapopbrengst uit appelen verhogen? Pectinase splitst pectine in kleinere bestanddelen waardoor het persen en de sapwinst wordt verbeterd.
- Moeilijkheid: eenvoudig
- Chemische stoffen: appelen – pectinase
- Thema: biochemie – scheidingstechnieken
- Tijd:30 min
- Begrippen: dosering – destillatie
5. Natuurproducten
5.1. Bereiding van pH indicatorpapier met natuurproducten
- Info: Hoe kun pH indicatorpapier maken met natuurlijke stoffen ? Tannines zijn condensaten met meerdere fenolgroepen. In de basissubstantie zijn twee fenolverbindingen terug te vinden pyrocatechine en pyrogallol. Deze tanninens kunnen uit kastanjes, eikels en bladeren worden gewonnen.De tannines kunnen aangewend worden bij kleurstoffen. Met galluszuur kunnen de pyrogalloltanninen een pH indicator geven.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Galluszuur 0.05 mol/l – Ijzer(III)chloride oplossing 0.015 mol/l – Zoutzuur 2 mol/l – Natriumhydroxide oplossing 2 mol/l
- Thema: biochemie – neutralisatiereacties
- Tijd: 20 min
- Begrippen: dosering – pH-indicator
5.2. Bereiden van gelachtige melkachtige voedingsmiddelen met natriumalginaat
- Info: Hoe kun je gels maken met zuivelproducten ?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Natriumfosfaat – Natriumalginaat – Zoetstoftabletten – Volle melk
- Thema: biochemie – bouw van materie
- Tijd: 20 min
- Begrippen: mengsels – gelering
5.3. Immobiliseren in een alginaatgel
- Info: Hoe kun je enzymen immobiliseren ? Na toevoegen van de gistcellen-alginaat-suspensie aan de calciumchlorideoplossing ontstaan bolletjes die zich na ongeveer 10 minuten tot de bodem zinken. Deze gisten zitten in de bolletjes ingebed en zijn gefixeerd.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Natriumalginaat – 1 pakje verse gistcellen – Calciumchloride
- Thema: biochemie
- Tijd: 20 min
- Begrippen: enzymen – immobiliseren

- Info: Hoe kun je wol kleuren met meekrap ? Met plantaardige kleurstoffen kan wol met verschillende kleurtonen worden gekleurd. De meekrap en rode biet zijn mogelijke planten met kleurstoffen. De meekrap bevat grote wortelstoffen die kleurstoffen bevatten. Weinige andere plantaardige kleurstoffen binden zich zo sterk als deze kleurstoffen aan wol. De wol moet wel vooraf worden voorbereid. Als beitsmiddel kan aluin met wijnsteenzuur worden gebruikt. Toevoeging van tarwezemelen geeft een rode kleur, met ijzersulfaat een blauwe kleur, met kopersulfaat een bruine kleur
- Moeilijkheid: eenvoudig
- Chemische stoffen: Zeep (om de wol uit te wassen) – Aluin – Meekrap (al dan niet gemalen) – Wijnsteenzuur – Tarwezemelen – Ijzer(II)sulfaat – Kopersulfaat
- Thema: biochemie
- Tijd: 20 min
- Begrippen: adsorptie
5.5. Kleurstoffen op basis van kwark
- Info: Hoe kun je kleurstoffen op basis van kwark maken ? Een hoofdbestanddeel van kwark is caseïne. Caseïne kan als grondstof voor verf worden gebruikt als het met borax en kalk wordt gemengd. Voegt men poedervorige pigmenten toe kan men een verf bekomen. Door toevoegen van lijnolie wordt de verf stabieler. De verven als plakkaatverf kunnen gebruikt worden op papier en karton en ook op hout.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 250 g kwark – Borax – Kalk – Kleurpigmenten – Lijnolie
- Thema: biochemie
- Tijd: 20 min
- Begrippen: mengsel
5.6. Lijmen met papier

- Info: Hoe kun je papier verlijmen ? Ambiëtinezuur is een hoofdbestanddeel in hars dat bij de bereiding van cellulose uit dennenhars als nevenproduct voorkomt. Dit product kan gebruikt worden voor het verlijmen van papier. Dit verlijmen is aan te tonen door proberen te schrijven op papier behandeld met deze stof.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Abiëtinezuur – Natriumhydroxide – Aluminiumsulfaat
- Thema: biochemie
- Tijd: 20 min
- Begrippen: mengsel
5.7. Papier verlijmen met chitosananhydride

- Info: Hoe kun je papier verlijmen met chitosan? Lost men chitosan op in zoutzuur dan ontstaat een wateroplosbare chitosanhydrochloride door de binding van protonen aan de aminogroepen. Brengt men de oplossing op papier aan dan ontstaat aan het oppervlak een film. Hierdoor wordt het papier waterafstotend wat met een stift kan worden aangetoond.
- Moeilijkheid: eenvoudig
- Chemische stoffen: chitosan
- Thema: biochemie – kunststoffen
- Tijd: 20 min
- Begrippen: mengsel – bioplastic
5.8. Kwantitatieve analyse van koperionen in het eluens van chitosancomplexen
- Info: Hoe kun je de koperionen in het eluens van chitosan terugvinden?
- Moeilijkheid: eenvoudig
- Chemische stoffen: EDTA oplossing 0.01 mol/l – Natriumacetaatoplossing 2 mol/l – Chrimazurol S oplossing
- Thema: biochemie – kunststoffen
- Tijd: 20 min
- Begrippen: mengsel – bioplastic – complexreactie
5.9. Complexerende werking van chitosan
- Info: Hoe kun je de complexerende werking aantonen van chitosan? Aminogroepen kunnen door de vrije elektronenparen bindingen vormen met kationen. Zo kan een ammoniakmolecule een ligand vormen met koperionen tot een stabiel tetra-aminecomplex. Analoog kan chitosan kationen complexeren. Een voordeel van koperionen is dat door de kleur de complexerende werking zichtbaar kan worden.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Chitosanvlokken – Kopersulfaatoplossing (0.1 mol/l) – Zwavelzuuroplossing 2 mol/l – Verdunde natriumhydroxide oplossing
- Thema: biochemie – kunststoffen
- Tijd: 20 min
- Begrippen: mengsel – bioplastic – complexreactie
5.10. Bereiding van folies uit chitosan

- Info: Hoe kun je foliën maken uit chitosan? Chitosan is een macromolecule dat uit de chitinepanser van insecten kan worden gewonnen. Zoals zetmeel kan men hiervan een folie maken. Daarvoor is het oplossen in een oplosmiddel noodzakelijk om het verdund te laten drogen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Chitosan – Azijnzuuroplossing 2 mol/l
- Thema: biochemie – kunststoffen
- Tijd: 20 min
- Begrippen: mengsel – bioplastic
5.11. Bereiding van eetbare folies uit zetmeel

- Info: Hoe kun je eetbare foliën maken uit zetmeel? Verantwoordelijk voor de filmvorming van de zetmeel zijn de inter- en intramoleculaire waterstofbindingen. Vooral e gestrekte amylosemoleculen zorgen voor een folie. Door partiële hydrolyse worden de amylopectinemoleculen licht afgebroken. Daarbij wordt de folievorming gemakkelijker. Filmvorming met zuiver zetmeel is door de vorming van intermoleculaire bindingen bij de kristalvorming moeilijker.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Aardappelzetmeel – Glycerine oplossing 85% – Zoutzuuroplossing 0.1 mol/l – Natriumhydroxide oplossing 0.1 mol/l
- Thema: biochemie – kunststoffen
- Tijd: 20 min
- Begrippen: mengsel – bioplastic
5.12. Winnen van terpenen uit sinaasappelschillen
- Info: Hoe kun je terpenen uit sinaasappelschillen winnen? In de schillen van citrusvruchten bevinden zich poriën die kleine wateroplosbare vluchtige stoffen bevatten. Worden deze poriën geplet dan wordt een intensieve geur van citrusvruchten waargenomen. Deze.vluchtige stoffen zijn terpenen, alcoholen alkanalen en esters. Afhankelijk van de vrucht zijn deze samen in een mengsel tot 0.4-0.5% van het gewicht van de schillen? Sinaasappelolie bevat vooral de terpenen Limonen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Diethylether – Sinaasappelschillen
- Thema: biochemie – organische stoffen
- Tijd: 20 min
- Begrippen: mengsel – extractie
5.13. Bereiding van een anionisch detergent uit een vetalcohol

- Info: Hoe kun je anionische tensiden bereiden?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Dodecanol – Diëthylether – Geconcentreerd zwavelzuur – NaOH oplossing – Fenolftaleïneoplossing (0,05%) – Azijnzuuroplossing 1 mol/l – Magnesiumchloride oplossing 1 mol/l
- Thema: biochemie – mengsels
- Tijd: 20 min
- Begrippen: detergent
5.14. Winnen van kokosvet uit kokosraspelen

- Info: Hoe kun je kokosvet winnen uit kokosraspsel? Met benzine kan het kokoksvet worden gelost en vervolgens wordt de benzine afgedestilleerd. Men bekomt een wit, goed ruikend vet.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Benzine (50-70° C kookpunt) – Kokosraspels 25 g – Natriumsulfaat (watervrij)
- Thema: biochemie – scheidingstechnieken
- Tijd: 30 min
- Begrippen: extractie
5.15. Winnen van kokosraspelen uit kokosnoot

- Info: Hoe kun je kokos winnen uit kokosnoten? De vruchten van de kokospalm, de kokosnoten, bevatten veel vet. Uit 100 g pulp kan tot 20 g vet worden gewonnen. Kokosvet is rijk aan laurine- en myristinezuur.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Kokosnoot – Calciumchloride
- Thema: biochemie – scheidingstechnieken
- Tijd: 30 min
- Begrippen: extractie
6.DNA
6.1. Isoleren van DNA uit kalfszwezerik
- Info: Hoe kan je de DNA isoleren uit kalfszwezerik? De natriumdodecylsulfaatoplossing treedt op als een detergent en zal cellen en kernmembranen afbreken. Door toevoeging van zoutzuur zullen nucleïnezuren neerslaan.
- Moeilijkheid: eenvoudig
- Chemische stoffen: kalszwezerik – zoutzuuroplossing – natriumdodecylsulfaat
- Thema: biochemie
- Tijd: 40 min
- Begrippen: extractie – DNA
6.2. Zure hydrolyse van DNA en identificeren van de bestanddelen

- Info: Hoe kan je de bestanddelen van DNA aantonen? Door hydrolyse ontstaan de bouwstenen van DNAHet Dische reagens bevat difenylamine dat reageert met desoxyribose.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Dialreagens – universele indicator – Dische reagens – DNA
- Thema: biochemie
- Tijd: 40 min
- Begrippen: hydrolyse – DNA
7. Enzymen
7.1.Factoren die een invloed hebben op de enzymactiviteit
- Info: Welke factoren beïnvloeden de werking van enzymen? Bijna alle enzymen zijn temperatuurafhankelijk. Bij een hoge temperatuur denatureren de enzymen en zijn onwerkzaam. De optimale temperatuur ligt meestal bij 37°C.Het incuberen met zware metalen is bekend bij eiwitten, dus ook bij enzymen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: eiwitsuspensie – trypsine – verse melk
- Thema: biochemie
- Tijd: 40 min
- Begrippen: enzymen – factoren die invloed hebben op activiteit
- Info: Wat is de werking van proteïnasen? Door pepsine en trypsine worden peptidebindingen in eiwitten afgebroken.
- Moeilijkheid: eenvoudig
- Chemische stoffen: pepsine – trypsine – kippenei
- Thema: biochemie
- Tijd: 30 min
- Begrippen: enzymen – eiwittenafbraak
7.3. Werking van lipase

- Info: Wat is de werking van lipase? Door lipase wordt vet gehydrolyseerd. Er ontstaan vetzuren die een verkleuring van indicator kunnen veroorzaken
- Moeilijkheid: eenvoudig
- Chemische stoffen: lipase – melk – universele indicator – fft – olijfolie
- Thema: biochemie
- Tijd: 30 min
- Begrippen: enzymen – vetafbraak
- Info: Wat is de werking van peroxidase? De oplossing kleurt na korte tijd roodoranje. Uit het pyrogallol ontstaat purpurgalline.
- Moeilijkheid: eenvoudig
- Chemische stoffen: myrikswortel -pyrogallol – waterstofperoxide
- Thema: biochemie
- Tijd: 30 min
- Begrippen: enzymen – peroxidase activiteit
7.5. Enzymatische splitsing van sucrose

- Info: Hoe kan sucrose worden gehydrolyseerd? Sucrose wordt door gist via het enzyme invertase gesplitst in glucose en fructose. Via glucosestix kan glucose worden aangetoond.
- Moeilijkheid: eenvoudig
- Chemische stoffen: sucrose – gist – stix
- Thema: biochemie
- Tijd: 30 min
- Begrippen: enzymen – invertase
7.6. Onderzoek van zuurstofgas bekomen door de enzymatische afbraak van waterstofperoxide

- Info: Hoe kan je zuurstofgas ontstaan door de katalase werking aanduiden? Het gevormde gas is zuurstofgas wat vrijkomt van het waterstofperoxide door inwerking van gistcellen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: waterstofperoxide – gist
- Thema: biochemie
- Tijd: 30 min
- Begrippen: enzymen – peroxidasewerking
7.7. Werking van katalase
- Info: Wat is de werking van katalase? Bij de stalen treedt schuimvorming op. Het waterstofperoxide wordt door katalase afgebroken.
- Moeilijkheid: eenvoudig
- Chemische stoffen: dierenlever – waterstofperoxide
- Thema: biochemie
- Tijd: 30 min
- Begrippen: enzymen – katalase
7.8. Werking van amylase

- Info: Wat is de werking van amylase? Na een aantal minuten behandeling van zetmeel door amylase blijft de geelbruine kleur van lugol bestaan. Dit duidt op de afbraak van zetmeel.
- Moeilijkheid: eenvoudig
- Chemische stoffen:amylase – zetmeel – lugol
- Thema: biochemie
- Tijd: 30 min
- Begrippen: enzymen – amylase
7.9. Werking van urease

- Info: Wat is de werking van urease? Ureum wordt afgebroken door een urease in ammoniak en koolstofdioxide
- Moeilijkheid: eenvoudig
- Chemische stoffen: ureum – urease – fft
- Thema: biochemie
- Tijd: 30 min
- Begrippen: enzymen – amylase
7.10. De chemische opbouw van enzymen
- Info: Wat is de chemische samenstelling van een enzym? Enzymen zijn eiwitten
- Moeilijkheid: eenvoudig
- Chemische stoffen: urease – lipase – koper(II)sulfaat – ammoniak – salpeterzuur
- Thema: biochemie
- Tijd: 30 min
- Begrippen: enzymen – samenstelling
7.11. Onderzoek van de chemische elementen in enzymen

- Info: Hoe kun je de elementen in een enzym aantonen? Door het verhitten ontstaat koolstof. Er zetten zich ook waterdruppels af tegen de wand wat kan aangetoond worden met het kobaltchloridepapiertje. Universele indicator kleurt blauw. Behandeling met geconcentreerde zoutzuur geeft een nevel van ammoniumchloride waarbij het stikstof is aangetoond.
- Moeilijkheid: eenvoudig
- Chemische stoffen: urease – natriumhydroxide – universele indicator – zoutzuur – amylase – kobaltchloride
- Thema: biochemie
- Tijd: 30 min
- Begrippen: enzymen – samenstelling
7.12. Winnen van amylase

- Info: Hoe kun je amylase bekomen? Door toevoeging van ethanol kan uit sojaboonmeel amylase worden bekomen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: sojameel – ethanol
- Thema: biochemie
- Tijd: 30 min
- Begrippen: enzymen – amylase
7.13. Winnen van urease

- Info: Hoe kun je urease bekomen? Door toevoeging van aceton kan uit sojaboonmeel urease worden bekomen. Het is een witte vaste stof.
- Moeilijkheid: eenvoudig
- Chemische stoffen: sojameel – aceton
- Thema: biochemie
- Tijd: 30 min
- Begrippen: enzymen – urease








