Chemische kameleon
1.Onderzoeksvraag
Hoe kunnen we kleuren van stoffen veranderen met behulp van sacharose?
2.Voorbereiding
a.Begrippen als achtergrond voor experiment
- Oxidator: een chemische stof die in een chemische reactie elektronen kan opnemen.
- Reductor: een chemische stof die in een chemische reactie elektronen kan afstaan.
- Oxidatie: een chemisch proces waarbij een stof (de reductor) elektronen afgeeft aan een andere stof (de oxidator) waarbij het oxidatiegetal van de reductor toeneemt.
- Reductie: is het scheikundige proces waarbij een deeltje elektronen opneemt
b.Materiaal + stoffen
- erlenmeyer
- proefbuisje
- KMnO4
- sacharose
- NaOH
c.Bereiding oplossingen
Maak een oplossing van 0,5g NaOH in 100 ml water en voeg hieraan 2 lepels suiker.
Maakt een KMnO4 – oplossing van 1g/L
d.Opstelling (foto)

e.Etiketten

3.Uitvoeren
a.Werkwijze
- Maak een kaliumpermanganaatoplossing en verdeel deze over de 3 petrischaaltjes
- Dompel met een tang een suikerklontje onder in de NaOH oplossing en leg deze in het midden van de petrischaaltjes.
- De kleurverandering is beter zichtbaar.
- (Je kan aan de kaliumpermanganaatoplossing gelatine toevoegen. Zo gaat het proces trager3.)
b.Waarneming (+ foto’s)

4.Reflecteren
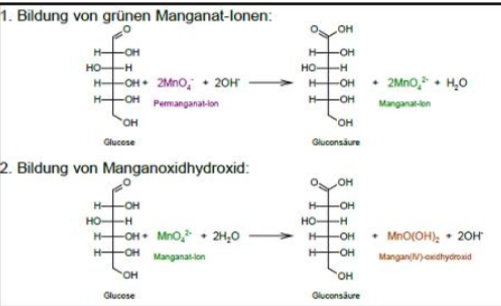
Suiker is de reductor en zorgt ervoor dat het kaliumpermanganaat kan reduceren. De sucrose reageert met het paarse permanganaation en het
In basisch milieu met de aldehydefunctie ter vorming van gluconzuur , een groen mangaanaation (oxidatiegetal van Mn = +VI) en water.
Het manganaation reageert met de glucose en het water tot gluconzuur, bruin mangaan(IV)oxide.
Het oxidatiegetal van mangaan gaat van +VII naar + VI naar + IV. Er treedt een reductie op.






