Hoofdstuk 3 – Experimenten
0. Algemeen
0.1.Wat zijn de verschillen tussen metalen en niet-metalen?

- Info:Wat zijn de verschillen tussen metalen en niet-metalen? Via geleiding, uitzicht onderscheid maken
- Moeilijkheid: eenvoudig
- Chemische stoffen: Aluminium – Grafiet – Houtskool – IJzer – Koper – Lood – Zink
- Thema: enkelvoudige stoffen
- Tijd: 30 min
- Begrippen: enkelvoudige stoffen – eigenschappen – metalen – niet-metalen
0.2. Reactie van metalen met zuurstofgas

- Info: Hoe beïnvloedt de verdelingsgraad de verbrandingsreactie?
- Moeilijkheid: eenvoudig
- Chemische stoffen: ijzerpoeder- spijker
- Thema: enkelvoudige stoffen
- Tijd: 10 min
- Begrippen: enkelvoudige stoffen – eigenschappen – metalen – niet-metalen – verbrandingsreactie
0.3. Enkelvoudige stoffen indelen op basis van elektrische eigenschappen

- Info: Hoe kun je enkelvoudige stoffen indelen op basis van elektrische geleiding?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Aluminium – Grafiet – Houtskool – IJzer – Koper – Lood – Zink
- Thema: enkelvoudige stoffen
- Tijd: 30 min
- Begrippen: enkelvoudige stoffen – eigenschappen – metalen – niet-metalen
0.4. Enkelvoudige stoffen indelen op basis van warmtegeleiding

- Info: Hoe kun je enkelvoudige stoffen indelen op basis van warmtegeleiding?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Aluminium – Grafiet – Houtskool – IJzer – Koper – Lood – Zink
- Thema: enkelvoudige stoffen
- Tijd: 30 min
- Begrippen: enkelvoudige stoffen – eigenschappen – metalen – niet-metalen
0.5. Inwerking van zuren op metalen
- Info: Hoe werken zuren in op metalen?
- Moeilijkheid: gemiddeld
- Chemische stoffen: verdund HCl 6mol/l – verdund H2SO4 6mol/l – geconcentreerd salpeterzuur 12mol/l – kleine maatcilinder met 1 ml CuSO4-oplossing 1% – papier met mespunt ijzerpoeder – ijzernagels – zinkplaatjes – 3 aluminiumplaatjes
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 30 min
- Begrippen: enkelvoudige stoffen – reactie metalen met zuren
1. Aluminium
1.1. Aluminiumbatterij

- Info: Hoe kunnen we een batterij bouwen met aluminium?
- Moeilijkheid: gemiddeld
- Chemische stoffen: Koperen plaatje – Aluminium plaatje – Demi-water – Zout – Bleek (Chloor)
- Thema: enkelvoudige stoffen – galvanische cel
- Tijd: 30 min
- Begrippen: enkelvoudige stoffen – batterij – galvanische cel
1.2. Reactie van natriumhydroxidekorrels met aluminium

- Info: Welk effect heeft natriumhydroxide (sterke base) op aluminium?
- Moeilijkheid: gemiddeld
- Chemische stoffen: 1g NaOH-korrels (ontstopperkorrels) – Aluminiumfolie
- Thema: enkelvoudige stoffen – anorganische stoffen – chemische reactie
- Tijd: 30 min
- Begrippen: enkelvoudige stoffen – corrosie – sterke base
1.3. Aluminium, lucht een batterij

- Info: Hoe kunnen we een batterij bouwen met aluminium?
- Moeilijkheid: gemiddeld
- Chemische stoffen: Koperen plaatje – Aluminium plaatje – Demi-water – Zout – Bleek (Chloor)
- Thema: enkelvoudige stoffen – galvanische cel
- Tijd: 30 min
- Begrippen: enkelvoudige stoffen – batterij – galvanische cel
1.4. Aluinkristallen uit aluminiumfolie

- Info: Hoe kun je kristallen maken met aluminiumfolie?
- Moeilijkheid: gemiddeld
- Chemische stoffen: aluminiumfolie – kaliumhydroxideoplossing 1,5 mol/l – zwavelzuuroplossing 9 mol/l
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 30 min
- Begrippen: enkelvoudige stoffen – redoxreactie
1.5. Aluminiumfolie reageert met kopersulfaatoplossing

- Info: Dit experiment illustreert de verplaatsing van koper uit koper(II)sulfaatoplossing (CuSO4) met aluminiumfolie.
- Moeilijkheid: gemiddeld
- Chemische stoffen: aluminiumfolie – 2g NaCl – 0,8 mol/l Koper(II)sulfaat (CuSO4(aq))
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 30 min
- Begrippen: enkelvoudige stoffen – redoxreactie – verdringingsreeks metalen

- Info: Hoe kunnen we elektrische energie bekomen met een blikje? Wanneer we de grafietelektrode in de natriumchloride-oplossing brengen, begint een chemische reactie. Chemische energie wordt omgezet in elektrische energie.
- Moeilijkheid: gemiddeld
- Chemische stoffen: 2mol/l NaCl – leeg blikje – grafiet elektrode
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 30 min
- Begrippen: enkelvoudige stoffen – galvanische cel

- Info: Veel metalen verbranden, maar brandt aluminium ook?
- Moeilijkheid: gemiddeld
- Chemische stoffen: Al-poeder – Al-folie
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 30 min
- Begrippen: enkelvoudige stoffen – verbrandingsreactie – deeltjesgrootte
2. Boor
2.1. Semi-kwantitief onderzoek boor met curcuma-poeder
- Info: Met welk alledaags product kan ik de aanwezigheid van boor onderzoeken? Borium uit boorzuurionen vormt een rood complex genaamd rosocyanine met curcumine. In dit complex coördineert een booratoom met twee moleculen curcumine.
- Moeilijkheid: gemiddeld
- Chemische stoffen: curcumine – natriumtetraboraatdecahydraat (Borax) – ethanol
- Thema: enkelvoudige stoffen – identificatiereactie
- Tijd: 30 min
- Begrippen: enkelvoudige stoffen – kleurreactie – identificatiereactie
2.2. Ijs brandt groen (proef niet uitvoeren in klas wegens gebruik van boorzuur)

- Info: Hoe verklaren we de kleur van de vlam bij het verbranden van ijs?
- Moeilijkheid: gemiddeld
- Chemische stoffen:Methanol – boorzuur
- Thema: enkelvoudige stoffen – bouw van atomen
- Tijd: 30 min
- Begrippen: enkelvoudige stoffen – vlamproef – atoommodel van Bohr
3. Calcium
3.1. Calciumgehalte in kraantjeswater

- Info: Hoe kun je het calciumgehalte in drinkwater bepalen?
- Moeilijkheid: gemiddeld
- Chemische stoffen: Aquanal educase (reagens 1,2,3; 5ml pipet en gegradueerde 1ml pipet) – Eriochrome Black T (indicator)
- Thema: enkelvoudige stoffen – doseren
- Tijd: 30 min
- Begrippen: enkelvoudige stoffen – complexreactie
3.2. Gekleurde vlam in een gel

- Info: Wat gebeurt er met een gel van calciumacetaat wanneer we deze in contact brengen met vuur?
- Moeilijkheid: eenvoudig
- Chemische stoffen: ethanol 96%, – calciumacetaat monohydraat, – gedemineraliseerd water
- Thema: enkelvoudige stoffen – bouw van atomen
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – vlamproef – atoommodel van Bohr
3.3. Heat packs

- Info: Hoe kun je je handen opwarmen in de winter met water en een zout?
- Moeilijkheid: eenvoudig
- Chemische stoffen: 10g CaCl2 , 25g H2O
- Thema: enkelvoudige stoffen – thermodynamica – chemische reactie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – oploswarmte
3.4. Knalgas bereiden met calcium

- Info: Hoe kun je je handen opwarmen in de winter met water en een zout?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Calcium, – gedemineraliseerd water, – fft-oplossing 0,05%
- Thema: enkelvoudige stoffen – chemische reactie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – reactie aardalkalimetalen met water
3.5. Thermolyse van calciumcarbonaat

- Info: Wat gebeurt er met calciumcarbonaat wanneer we het verhitten en vervolgens terug water aan toevoegen? Wanneer we calciumcarbonaat verwarmen zien we dat er een gas wordt gevormd en ook een witte aanslag ontstaat. Wanneer we de witte aanslag in water brengen, wordt het water eerst licht melkwit. Bij het uitademen in het mengsel, wordt het mengsel melkwit van kleur.
- Moeilijkheid: eenvoudig
- Chemische stoffen: calciumcarbonaat, – gedemineraliseerd water
- Thema: enkelvoudige stoffen – chemische reactie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – thermolyse
3.6. Vriespuntsverlaging met CaCl2

- Info: Welke invloed heeft calciumchloride op het vriespunt van water?
- Moeilijkheid: eenvoudig
- Chemische stoffen: ijsblokjes, – vast calciumchloride
- Thema: enkelvoudige stoffen – chemische reactie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – endo-energetisch – vriespuntsverlagende werking – oploswarmte
4. Dibroom
4.1. Bromering van pentaan o.i.v. licht

- Info: Welke stof wordt er gevormd bij de fotolyse van pentaan met dibroom? Halogeenalkanen ontstaan bij de reactie tussen het halogeen en het alkaan. Tijdens de reactie moet het mengsel bestraald worden met zichtbaar (Br2) of U.V.-licht (Cl2).
- Moeilijkheid: gemiddeld
- Chemische stoffen: n-pentaan – dibroom – 5% AgNO3
- Thema: enkelvoudige stoffen – organische stoffen
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – identificatie koolwaterstoffen – substitutiereactie
4.2. Broomse regenboog in tomatensap

- Info: Kunnen we een kleurenpatroon maken met tomatensap? Het belangrijkste pigment in tomaten is het lycopeen. In de structuur zijn geconjugeerde electronensystemen aanwezig die blauwe kleur absorberen en daardoor een rode kleur hebben. Door additie met broom verkleint de lengte van het geconjugeerd systeem waardoor de geabsorbeerde golflengte verkort.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Tomatensap – Broomwater (verzadigd)
- Thema: enkelvoudige stoffen – organische stoffen
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – identificatie koolwaterstoffen – substitutiereactie
4.3. Tomatensap met broom

- Info: Kunnen we een kleurenpatroon maken met tomatensap? Het belangrijkste pigment in tomaten is het lycopeen. In de structuur zijn geconjugeerde electronensystemen aanwezig die blauwe kleur absorberen en daardoor een rode kleur hebben. Door additie met broom verkleint de lengte van het geconjugeerd systeem waardoor de geabsorbeerde golflengte verkort.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Tomatensap – Broomwater (verzadigd)
- Thema: enkelvoudige stoffen – organische stoffen
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – identificatie koolwaterstoffen – substitutiereactie
5. Dichloor
5.1. Elektrolyse van waterstofchloride

- Info: Hoe kunnen we de elektrolyse van waterstofchloride aantonen? De samengestelde stof HCl zal dus ontleed worden in tot enkelvoudige stoffen, namelijk chloorgas en waterstofgas.
- Moeilijkheid: gemiddeld
- Chemische stoffen: druppelflesje gevuld met HCl-oplossing 1 mol/l
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 10 min
- Begrippen: enkelvoudige stoffen – elektrolyse

- Info: Bleekwater reageert met HCl – Het ZnS neemt een gele kleur door de vorming van S – Het KI wordt donker door de vorming van I2 – Er treedt geen verandering op met Zn
- Moeilijkheid: gemiddeld
- Chemische stoffen: bleekwater – HCl 1 mol/l – ZnO – CuS – KI
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 10 min
- Begrippen: enkelvoudige stoffen – spanningsreeks niet-metalen
5.3. Identificatiereacties van chloorgas in een petrischaal

- Info: Hoe kunnen we redoxreacties visueel voorstellen in een chemische reactie? Hoe kunnen we chloorgas bereiden en aantonen? Het NaClO reageert met het zuur ter vorming van chloorgas. Door de beperkte concentratie is de geel-groene kleur van het gas minder duidelijk te zien. Het gas verspreidt zich in het petrischaaltje. Doordat het chloorgas reageert met NaOH daalt de pH en ontkleurt de indicator. Het chloorgas reageert met KI, reactiviteit van niet-metalen waardoor dijood ontstaat. Het dijood is aan te tonen met zetmeel.
- Moeilijkheid: gemiddeld
- Chemische stoffen: NaClO (javel) – H2SO4 1 mol/l – NaOH 0,1 mol/l – Fenolftaleïne/thymolftaleïne 0,05% – KI 0,1 mol/l – Zetmeel 1% – Fe(II)SO4 0,1 mol/l – KSCN 0,1 mol/l
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – spanningsreeks niet-metalen

- Info: Het KI verandert in geel door de vorming van I2 – Het KBr verandert in geel door de vorming van Br2 – Met NaCl treedt geen reactie op.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Bleekwater – HCl 1 mol/l – NaCl 0,2 mol/l – KBr 0,2 mol/l – KI 0,2 mol/l
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – spanningsreeks niet-metalen
5.5. Micro-opstelling voor bereiding van chloorgas

- Info:Welke reactie doet chloorgas vormen? We hebben aan de hand van elektrolyse chloorgas gemaakt. In de industrie wordt deze techniek ook gebruikt om chloorgas te winnen. De NaCl – oplossing gaat splitsen.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Zoutoplossing KI/zetmeel – oplossing – Broomcresolgroen
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – elektrolyse
5.6. Bleken van papier met dichloor

- Info:Hoe kun je papier of stof ontkleuren? Chloorgas is een sterk oxidans, dat gebruikt wordt als bleekmiddel zowel op grote schaal als op huishoudelijke schaal.
- Moeilijkheid: gemiddeld
- Chemische stoffen: commerciële javel – HCl-oplossing geconcentreerd – stalen van felgekleurd papier of textiel
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – oxidans
5.7. Spanningsreeks bepalen van niet-metalen met dichloor
- Info: Hoe kunnen we de spanningsreeks van niet-metalen aantonen met een luciferdoosje?
- Moeilijkheid: gemiddeld
- Chemische stoffen: KI oplossing 1 mol/l – 10% zoutzuuroplossing
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – spanningsreeks van niet-metalen
5.8. Dichloor bereid met huishoudproducten

- Info: Hoe kunnen we Cl²-gas verkrijgen met huishoudproducten?
- Moeilijkheid: gemiddeld
- Chemische stoffen: bleekwater (NaOCl) – zoutzuur – KI
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – redoxreactie – spanningsreeks van niet-metalen
5.9. Chloorsynthese

- Info: Hoe kunnen we Cl²-gas verkrijgen met huishoudproducten? Zodra het zoutzuur op de kaliumpermanganaatkristallen druppelt, schuimt het op. Er ontstaat een gas.
- Moeilijkheid: gemiddeld
- Chemische stoffen: 2 g kaliumpermanganaat – 20 ml zoutzuur – 100 ml natriumthiosulfaat verzadigd
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – redoxreacties
6. Dijood
6.1. Chemische patronen in een waterige oplossing

- Info: Het jood is deels gesublimeerd en zal bij contact met zetmeel een donker blauwe kleur geven aan de oplossing. Boodschap met zetmeel ontcijferen
- Moeilijkheid: eenvoudig
- Chemische stoffen: joodoplossing in ethanol 10%, – 0.1 mol/l KI, – zetmeeloplossing 0,5%
- Thema: enkelvoudige stoffen – identificatie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – identificatiereactie – sublimatie
6.2. Geheime boodschappen korte tijd zichtbaar

- Info: Het jood is deels gesublimeerd en zal bij contact met zetmeel een donker blauwe kleur geven aan de oplossing. Boodschap met zetmeel ontcijferen
- Moeilijkheid: gemiddeld
- Chemische stoffen: 2.5g I2 – 1.7 g KI – 1 g zetmeel – 2.32 g Na2S2O3.5H20 – water
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – identificatiereactie – sublimatie – redoxreactie
6.3. Jood in zeewier
- Info: Hoe kunnen we testen of er jood in zeewier zit? Omdat dijood een apolaire stof is zal het oplossen in de cyclohexaan. Als dan de cyclohexaan verdampt, blijft enkel nog dijood over.
Zeewier bevat een aantoonbare hoeveelheid dijood.
- Moeilijkheid:moeilijk
- Chemische stoffen: Waterstofperoxide 6% – Cyclohexaan – Zwavelzuur 0,5mol/l – Zeewier
- Thema: enkelvoudige stoffen -scheidingstechnieken
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – identificatiereactie – extractie

- Info: Klokreactie met kaliumjodide, waterstofperoxide en thiosulfaatoplosossingen. Kleur wordt gevormd door ontstaan van dijood en reactie met zetmeel.
- Moeilijkheid:moeilijk
- Chemische stoffen:
- OplossingA: 2 ml 30% H2O2 + 93 ml gedestilleerd water
- Oplossing B: Breng 1 g zetmeel in 100ml water aan het koken. Kook eventjes door. Voeg nu 0,124 g Na2S2O3.5H2O aan de 100ml oplossing
- OplossingC: 1,74 g KI, 1,4 g CH3COONa en 3ml 6M azijnzuur in 200 ml oplossing
- Thema: enkelvoudige stoffen – reactiesnelheid
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – klokreactie
- Info: Hoe kunnen we met onze hand oplossingen van kleur doen veranderen?
- Moeilijkheid:moeilijk
- Chemische stoffen: KIO3 – geconcentreerd zwavelzuur – ethanol – Na2SO3 – zetmeel
- Thema: enkelvoudige stoffen – reactiesnelheid
- Tijd: 30 min
- Begrippen: enkelvoudige stoffen – klokreactie
6.6. Oscillerende reactie met dijood

- Info: Oscillerende reactie waarbij geleidelijk dijood wordt gevormd met een bepaalde snelheid
- Moeilijkheid:moeilijk
- Chemische stoffen: Zetmeeloplossing van 1% – Vitamine C of ascorbinezuur – Lugol-oplossing
- Thema: enkelvoudige stoffen – reactiesnelheid
- Tijd: 30 min
- Begrippen: enkelvoudige stoffen – klokreactie
6.7. Vorming van een éénwaardig koperzout

- Info: Wat gebeurt bij samenvoegen van kopersulfaatoplossing met kaliumjodide? Toevoeging van KI aan de koperoplossing geeft een bruinkleuring welke verdwijnt na toevoeging van de thiosulfaatoplossing. In de proefbuis is een witte neerslag van het CuI aanwezig.
- Moeilijkheid: eenvoudig
- Chemische stoffen: KI oplossing 0,1 mol/l – CuSO4-oplossing 0,1 mol/l – Verzadigde Na2S2O3 oplossing
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 10 min
- Begrippen: enkelvoudige stoffen -redoxreactie
6.8. Zwart en wit geeft kleurloos

- Info: Hoe kan bij het samenvoegen van een witte en een zwarte oplossing, een kleurloze oplossing worden gevormd?
- Moeilijkheid: eenvoudig
- Chemische stoffen: 10 ml joodtinctuur – 90 ml azijn – ascorbinezuur opgelost in 30 ml water – zetmeeloplossing – 15 ml hypochloriet in 45 ml water (=javel) – 150 ml water – een halve theelepel magnesiumsulfaat – huishoudammoniak 1 mol/l
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 10 min
- Begrippen: enkelvoudige stoffen -redoxreactie
6.9. Jood-Bloem

- Info: Wat gebeurt er als we lugol en zetmeel in dezelfde afgesloten ruimte brengen?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Zetmeel – Lugoloplossing
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 10 min
- Begrippen: enkelvoudige stoffen -redoxreactie – identificatiereactie
7. Fosfor
7.1. Raket met lucifers

- Info: Hoe kunnen we met aluminiumfolie en een kaars, lucifers laten wegschieten als een raket? Door verhitting gaat de kaliumchloraat en de paraffine ontleden. Er wordt veel koolstof en zuurstofgas gevormd. Als deze in contact komen met de vlam van de kaars wordt er enorme hoeveelheid koolstofdioxide gevormd. Deze grote gasontwikkeling is de stuwkracht.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Lucifers – Aluminiumfolie – Kaars
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 10 min
- Begrippen: enkelvoudige stoffen – verbrandingsreactie
8. Helium
8.1. Inademen van helium

- Info: Waarom verandert de stem als je helium inademt en dan spreekt?
- Helium heeft minder weerstand tegen de stembanden dan lucht. Ze trillen sneller, waardoor de toonhoogte van de stem toeneemt.
- Moeilijkheid: eenvoudig
- Chemische stoffen:1 ballon met helium
- Thema: enkelvoudige stoffen – periodiek systeem
- Tijd: 5 min
- Begrippen: enkelvoudige stoffen – edelgassen
9. Ijzer

- Info: Hoe kunnen we corrosie zichtbaar maken? De corrosie van een metaal is een redoxproces. Als metallisch ijzer oxideert wordt zuurstofgas of waterstofgas gereduceerd waarbij ferro-ionen en hydroxide ionen of waterstofgas gevormd worden.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Gelatine – Nagel – Fenolftaleine – Kaliumferricyanide (K3Fe(CN)6)
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – corrosie
9.2. Elektrochemische corrosie

- Info: Hoe beïnvloedt een koperdraad het roesten van een nagel/spijker? We zien dat de gelatine rond de spijker/nagel groen is gaan kleuren. Rond het koper verschijnt de paarse kleur van het fft. Er ontstaat eveneens de kleur van berlijnsblauw
- Moeilijkheid: gemiddeld
- Chemische stoffen: Fenolftaleïne oplossing in ethanol – Oplossing K4Fe(CN)6: 0, 1 mol/l – Ijzeren nagel – Koperdraad van 4 cm
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – corrosie
9.3. Exotherme reactie van azijn met staalwol

- Info: Hoe beïnvloedt een koperdraad het roesten van een nagel/spijker? We zien dat de gelatine rond de spijker/nagel groen is gaan kleuren. Rond het koper verschijnt de paarse kleur van het fft. Er ontstaat eveneens de kleur van berlijnsblauw
- Moeilijkheid: gemiddeld
- Chemische stoffen: tafelazijn – staalwol
- Thema: enkelvoudige stoffen – chemische reactie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – exo-energetische reactie
9.4. Ijzer aanduiden in cornflakes

- Info: Maak van het cornflakesmengsel een papje. Ga er overheen met een magneet. Je ziet dat er in de zak kleine zwarte deeltjes aangetrokken worden door de magneet.
- Moeilijkheid: gemiddeld
- Chemische stoffen: cornflakes
- Thema: enkelvoudige stoffen – stofeigenschappen
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – magnetisme – identificatiereactie
9.5. Ijzer in munten

- Info: Welke munten zijn magnetisch ? We houden boven iedere munt een magneet en kijken welke munten aangetrokken worden
- Moeilijkheid: eenvoudig
- Chemische stoffen: munten – magneet
- Thema: enkelvoudige stoffen – stofeigenschappen
- Tijd: 10min
- Begrippen: enkelvoudige stoffen – magnetisme – identificatiereactie
9.6. Magnetiet

- Info: Hoe kunnen we een stof laten aantrekken door een magneet ? Ijzeroxide is een mineraal met de naam magnetiet.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Sterke magneet (neodynium-, of uit fietsdynamo) – Ged. water (H2O): ca 6 mL – 0,250 g IJzer(III)chloride (FeCl3•6H2O) – 0,128 g IJzer(II)sulfaat (FeSO4•7H2O) – 4 ml 2 mol/l NH3 (aq) – 4ml zoutzuur 2mol/l
- Thema: enkelvoudige stoffen – stofeigenschappen
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – magnetisme
9.7. Roest

- Info: Welke factoren beïnvloeden roestvorming? Vocht dat zich in de lucht bevindt of in het gekookte water, tast het ijzer aan. Bij ijzer is dit waar te nemen door het ontstaan van roest. Enkel wanneer de spijker niet in contact kwam met water of lucht vertoonde hij geen roest.
- Moeilijkheid: gemiddeld
- Chemische stoffen: 3 afsluitbare potjes – 3 nagels – water
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – corrosie
9.8. Roestpreventie

- Info: Hoe is roesten te voorkomen? Roesten is een complexe reactie tussen ijzer, zuurstof en water waarbij gehydrateerde ijzeroxiden worden gevormd. In het begin gaat ijzer in oplossing als Fe2+ ionen en verliest daarbij elektronen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 5 g gelatine in 100ml water en los daarin 0,2 g – kaliumhexacyanoferraat(III) op. Houd de oplossing warm, maar niet heet, omdat dan giftige stoffen kunnen vrijkomen. – 10ml 1mol/l zoutzuur – Ca 2 cm magnesiumlint – Klein stukje zinkfolie – Klein stukje koperfolie – Vaseline
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – corrosie
9.9. Verkoperen van een ijzeren plaat

- Info: Het element koper heeft een normpotentiaal van +0,34 V en is edeler dan ijzer met een normpotentiaal van -0,44 V. Deze reactie loopt niet als het ijzer vooraf in de salpeterzuur wordt gebracht. Er blijkt een beschermlaag te ontstaan die verwijderd wordt door het schudden of tikken..
- Moeilijkheid: eenvoudig
- Chemische stoffen: CuSO4 oplossing – 5% geconcentreerd HNO3 – aceton – ijzeren plaatje
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – galvaniseren
9.10. Vorming van FeS uit ijzerpoeder

- Info: Hoe kunnen we aantonen dat we ijzersulfide (FeS) anders is dan ijzer (Fe) en zwavel (S)?
- Moeilijkheid: gemiddeld
- Chemische stoffen:ijzer poeder (Fe-poeder) – Zwavel poeder (S-poeder) – Demiwater
- Thema: enkelvoudige stoffen – redoxreacties – chemische reacties
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – massaverhouding in een chemische reactie
9.11. Passivering van ijzeren nagels met geconcentreerd salpeterzuur

- Info: Wat gebeurt er bij de passivering van ijzer door geconcentreerd salpeterzuur? Ijzer reageert niet met geconcentreerd salpeterzuur maar wel met verdund salpeterzuur. Dit komt doordat de metalen hun oppervlak beschermen door een passiverende laag van de overeenkomstige nitraten. Wanneer water wordt toegevoegd om het mengsel te verdunnen verloopt de reactie plots zeer snel en ontstaan de bekende bruine nitreuze dampen.
- Moeilijkheid: gemiddeld
- Chemische stoffen: staalwol – aceton – gedemineraliseerd water – geconcentreerd salpeterzuur
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – redoxreacties
9.12. Reactie tussen ijzer en ammoniumchloride

- Info: Welke soort reactie vindt er plaats tussen ijzer en ammoniumchloride na verhitten?
- Moeilijkheid: gemiddeld
- Chemische stoffen: 1g ijzerpoeder – 1g ammoniumchloride – Water
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – redoxreacties
9.13. Een bloedende nagel

- Info: Hoe kunnen we ervoor zorgen alsof het lijkt dat een nagel bloedt? De oplossing is helder. Als de nagel in de oplossing wordt gebracht , lijkt het alsof de nagel begint te bloeden.
- Moeilijkheid: gemiddeld
- Chemische stoffen: 100 ml 10% KSCN-oplossing – geconcentreerde HCl-oplossing – geconcentreerde waterstofperoxide oplossing
- Thema: enkelvoudige stoffen – chemisch evenwicht
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – redoxreacties – chemisch evenwicht
9.14. Magnetisch Slijm

- Info: Wat voor mengsel bekomen we als we borax, PVA en ijzerpoeder samenvoegen?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Borax (Natriumtertraboraat, Na2[B4O5(OH)4] ·8H2O) – Knutsellijm (PVA) -) IJzerpoeder
- Thema: enkelvoudige stoffen – kunststoffen – stofeigenschappen
- Tijd: 10 min
- Begrippen: enkelvoudige stoffen – magnetisme – slijm
9.15. Magnetische lucifers

- Info: Hoe kan ik lucifers via een magneet aantrekken? In het uiteinde van lucifers met een rood kopje zit ijzer(III)oxide. De ijzerionen blijven aanwezig in de verbrandde lucifers . Hierdoor kan de magneet het verbrandde deel van de lucifer aantrekken en dit ook mede doordat het reactieproduct zeer licht werd.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Lucifers – Sterke magneet
- Thema: enkelvoudige stoffen – stofeigenschappen
- Tijd: 10 min
- Begrippen: enkelvoudige stoffen – magnetisme
9.16. Het bloedend hart

- Info: Hoe kunnen we ijzeren nagel laten “bloeden”? Het geconcentreerd zoutzuur samen met het waterstofperoxide zorgt voor een oxidatie van het Fe naar Fe2+. Waterstofperoxide zorgt ervoor dat het Fe2+ verder oxideert naar Fe3+. Het Fe3+ reageert met het thiocyanaation tot ijzer(III)thiocyanaat, wat een rood complex is.
- Moeilijkheid: gemiddeld
- Chemische stoffen: 10 gram ammoniumthiocyanaat – Geconcentreerd zoutzuur – 3 % waterstofperoxide
- Thema: enkelvoudige stoffen – chemisch evenwicht – complexreactie
- Tijd: 10 min
- Begrippen: enkelvoudige stoffen – chemisch evenwicht – complexreactie
9.17. Vervaardigen van ijzer: thermiet

- Info: Welke methode gebruiken spoorwegarbeiders om spoorrails te lassen? Het aluminium brandt. Het aluminium haalt de hiervoor benodigde zuurstof uit het ijzer (III) oxide , aangezien het magnesium de zuurstofgas uit de lucht verbrandt en het thermietmengsel alleen van bovenaf in aanraking kan komen met zuurstofgas . Er worden elementair, magnetisch ijzer en aluminiumoxide en magnesiumoxide gevormd .
- Moeilijkheid: gemiddeld
- Chemische stoffen: Aarden pot – 15 g ijzer(III)oxide – 5 g aluminium
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 10 min
- Begrippen: enkelvoudige stoffen – thermietreactie
10. Kalium
10.1. KOH schilfers reageren met koolstofdioxide uit de lucht

- Info: Hoe kun je de hoeveelheid CO2 verminderen in de lucht? De KOH schilfers zijn sterk hygroscopisch. Hierdoor lossen ze op in het aangetrokken water. De KOH oplossing reageert vervolgens met de CO2 in de lucht. Na kristallisatie worden K2CO3 kristallen bekomen. De kristallen bruisen door reactie met het azijnzuur.
- Moeilijkheid: gemiddeld
- Chemische stoffen: tafelazijn – KOH schilfers
- Thema: enkelvoudige stoffen – neerslagreactie
- Tijd: 10 min
- Begrippen: enkelvoudige stoffen – binden van koolstofdioxide
11. Koolstof
11.1. Blauwe inkt wordt kleurloze inkt met koolstof

- Info: Hoe kunnen we inkt uit onze kleren krijgen? We kunnen de inktvlekken kleurloos maken met koolstof. Dit wil niet zeggen dat de inkt volledig uit onze kleren is. We maken de inkt kleurloos.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Actieve kool – Inkt of voedingskleur – Moutazijn
- Thema: enkelvoudige stoffen – scheidingstechnieken
- Tijd: 10 min
- Begrippen: enkelvoudige stoffen – adsorptie
11.2. Een zwarte slang met suiker

- Info: Hoe bekomen we de grootste zwarte slang uit suiker door middel van dehydratatie? De suiker wordt eerst bruin en later zwart.Het begint te borrelen en te roken.Er wordt eveneens een hoop hitte geproduceerd (exotherme reactie).Er vind echter nog een reactie plaats: oxidatie.
- Moeilijkheid: gemiddeld
- Chemische stoffen:Kristalsuiker (C12H22O11) – Geconcentreerd zwavelzuur (H2SO4)
- Thema: enkelvoudige stoffen – reactie met geconcentreerd zuur
- Tijd: 10 min
- Begrippen: enkelvoudige stoffen – corrosie
11.3.Ijzer maken uit roest met koolstof

- Info: Op welke manier kunnen we ijzer uit roest halen? We kunnen ijzer uit roest halen door een redoxreactie te laten plaatsvinden. We laten koolstof reageren met ijzer(III)oxide zodat er ijzer en koolstofdioxide gevormd wordt.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Na2CO3 – Fe2O3 – Een lucifer
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – corrosie
11.4. Koolstof isoleren uit eierschalen

- Info: Op welke manier kunnen we koolstof bereiden uit eierschalen? Eierschalen bevatten calciumcarbonaat. Dit gaat met magnesium koolstof vormen. Het wit licht dat tijdens de verbranding ontstaat, is afkomstig van het magnesium en de oranje vonkjes zijn afkomstig van het calciumcarbonaat in de eierschalen.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Droge eierschalen – Magnesiumpoeder – Zoutzuur 1mol/l
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – verdringingsreactie metalen
11.5. Verbrandingsproducten van koolstof

- Info: Welk verbrandingsproduct van een theelichtje wordt er bij een verbranding nog gevormd, naast waterdamp en koolstofdioxide bij onvoldoende aanwezigheid van zuurstofgas? We zien dat er een zwarte stof op de witte, porseleinen kroes gevormd wordt. Dit gebeurt op de plaats waar de kroes zich het kortst bij de vlam bevindt.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Theelichtje
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – verbrandingsreactie – vlam van een bunsenbrander
11.6. Reductie van koperoxide met koolstof

- Info: Hoe kunnen we koper uit koperoxide bekomen?
- Moeilijkheid: gemiddeld
- Chemische stoffen: koperoxide – koolstofpoeder
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – verdringingsreactie metalen
11.7. Verbranden van koolstof in een proefbuis

- Info: Hoe kan je ijzer bekomen uit roest met behulp van houtskool? Met deze proef kan je ook de magnetische eigenschap van ijzer aantonen doordat het ijzer gaat meebewegen met de magneet.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Ijzer(III)oxide – Houtskoolpoeder
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – verdringingsreactie metalen
11.8. Vloeibare Geleiders

- Info: Hoe kunnen we een lijntje actieve kool geleidend maken? et natriumsilicaat zorgt voor een stroopachtige structuur, soms wordt het ook wel vloeibaar glas genoemd. Het gaat geen reactie aan met het water maar zorgt meer voor een indikkend effect Grafiet is een goede elektrische geleider en het vloeibare glas “lijmt” zijn deeltjes aan elkaar om een continu circuit te vormen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Grafiet (actieve kool) – Natriumsilicaat – Water
- Thema: enkelvoudige stoffen – elektrisch eigenschappen
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – geleiding koolstof
11.9. Aantonen van koolstof

- Info: Wat gebeurt er als koolstofhoudende stoffen worden verhit? De suiker karameliseert bij een temperatuur van 160 ° C. Bij verbranding of verhitting tot hoge temperatuur laten organische stoffen een mengsel van koolstof, waterstof , zwavel , stikstof , zuurstof en andere elementen achter
- Moeilijkheid: eenvoudig
- Chemische stoffen: 10 g keukenzout – 10 g suiker
- Thema: enkelvoudige stoffen – ontledingsreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – identificatie koolstof – thermolyse
12. Koper
12.1. Het koperbriefgeheim

- Info: Welk verschil nemen we waar tussen koper dat bij verhitting wordt blootgesteld aan zuurstof en koper die niet wordt blootgesteld aan zuurstof?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Koperplaatje
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 10 min
- Begrippen: enkelvoudige stoffen – redoxreacties – verbranding – verschillende oxidatiegetallen
12.2. Koper Odyssee

- Info: Hoe kunnen we de wet van behoud van atomen aantonen met koper?
- Moeilijkheid: gemiddeld
- Chemische stoffen: Koperdraad – HNO3 –oplossing 6 mol/l – Ijs – NaOH-oplossing 6 mol/l – HCl-oplossing 2 mol/l – Water – Aluminiumfolie
- Thema: enkelvoudige stoffen – chemische reacties
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – wet van behoud van atomen
12.3. Kwalitatief onderzoek van koper in munten

- Info: Hoe kunnen we d.m.v. NH3-oplossing en HNO3-oplossing aantonen dat er koper zit in een munt? Na aanbrengen van de salpeterzuuroplossing, lijken de munten properder te zijn. Wanneer we met het wattenstaafje met ammoniakoplossing over deze munten wrijven, wordt dit wattenstaafje blauw.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Euromunten – HNO3-oplossing 1 keer verdund – NH3-oplossing 1 keer verdund
- Thema: enkelvoudige stoffen – chemische reacties
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – identificatiereactie
12.4. Omkeerbare omzetting van kopermetaal tot koperoxide en terug
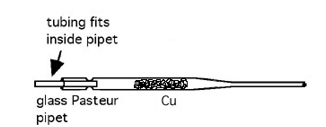
- Info: Verwarm de Cu-pipet gedurende 30s en blaas traag 60ml lucht door de pipet terwijl de pipet in de vlam blijft. De koper wordt zwart. Verbind de spuit met waterstofgas aan de pipet. Verhit de CuO-pipet en spuit traag waterstofgas in de pipet. Er ontstaan druppels water aan de wand van de pipet.
- Moeilijkheid: gemiddeld
- Chemische stoffen: wat koperpoeder of kleine stukjes – waterstofgas 50ml
- Thema: enkelvoudige stoffen – chemische reacties
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – omkeerbare reactie
12.5. Oscillatie aan koper

- Info: Wat gebeurt er met een verhitte koperdraad in de buurt van methanol? Er ontstaat een wisselwerking van gloei en vlammen en dit gedurende dertig minuten.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Methanol – Aluminiumplaat – Koperdraad
- Thema: enkelvoudige stoffen – chemisch evenwicht
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – oscillerende reactie
12.6. Reactie tussen koper en methanol

- Info: Wat zal er gebeuren als we verhit koper in methanol onderdompelen? Het roodbruine koper wordt bij verhitting zwart. In de methanol verdwijnt de zwarte kleur weer. Bovendien is er gasontwikkeling waarneembaar.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Dun stukje koper – Methanol
- Thema: enkelvoudige stoffen – chemisch evenwicht
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – oscillerende reactie
12.7. Mooie koperspiegel

- Info: Hoe kunnen we een fijn koperlaagje vormen? Ammoniumchloride ontleedt door verhitting.Op koper bevindt zich altijd een dun laagje koper(I) dat samen met het ontstane waterstofchloride wat koper(I)chloride vormt.Het koper(I)chloride ontleedt op de hete glaswand koper(II)chloride en koper: de koperspiegel
- Moeilijkheid: gemiddeld
- Chemische stoffen: 1 g ammoniumchloride (NH4Cl) – 0,5 g koperpoeder of -vijlsel (Cu)
- Thema: enkelvoudige stoffen – chemische reactie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – koperspiegel
12.8. Verkoperen van een ijzeren plaat

- Info: Het element koper heeft een normpotentiaal van +0,34 V en is edeler dan ijzer met een normpotentiaal van -0,44 V. Deze reactie loopt niet als het ijzer vooraf in de salpeterzuur wordt gebracht. Er blijkt een beschermlaag te ontstaan die verwijderd wordt door het schudden of tikken..
- Moeilijkheid: eenvoudig
- Chemische stoffen: CuSO4 oplossing – 5% geconcentreerd HNO3 – aceton – ijzeren plaatje
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – galvaniseren
12.9. Zwevende magie
- Info: Hoe kunnen we de zwaartekracht tarten op aarde? Als de magneet door de buis valt wordt het metaal blootgesteld aan een veranderend magnetisch veld. Het magnetische veld dwingt de elektronen in het (elektriciteit geleidend) metaal in een cirkelachtige baan, wervelstromen of ook wel Eddy currents genoemd.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Cu-buis – Neodymiummagneet
- Thema: enkelvoudige stoffen – stofeigenschap
- Tijd: 5 min
- Begrippen: enkelvoudige stoffen – magnetisme
12.10. Reactie tussen koper en salpeterzuur in microvorm

- Info: Hoe beïnvloedt de concentratie van de salpeterzuuroplossing de chemische reactie tussen koper en salpeterzuur? En hoe beïnvloedt hij die?
- Moeilijkheid: gemiddeld
- Chemische stoffen: koperkrullen – salpeterzuur (5% ) – salpeterzuur (53%)
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – redoxreactie
12.11. Reactie tussen koper en methanol

- Info: Wat zal er gebeuren als we verhit koper in methanol onderdompelen? Het roodbruine koper wordt bij verhitting zwart. In de methanol verdwijnt de zwarte kleur weer. Bovendien is er gasontwikkeling waarneembaar.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Dun stukje koper – Methanol
- Thema: enkelvoudige stoffen – organische stoffen
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – redoxreactie
12.12. Bruisend koper
- Info: Hoe kunnen we koper proper maken door het te laten bruisen? Vanaf het moment dat het koperplaatje in de oplossing wordt gezet treedt een reactie op aan het koperoppervlak met vorming van gasbellen. Het plaatje wordt lichter rood van kleur en de oplossing wordt blauw.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Koperplaatje – H2SO4 geconcentreerd – H2O2 geconcentreerd
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – redoxreactie
12.13. Oxidatie van koper en reductie van koperoxide

- Info: Hoe kan het metaal worden teruggewonnen uit een metaaloxide? Wanneer je de koperen plaat voor het eerst in de brandende vlam houdt, begint de plaat te gloeien. Na afkoeling is de plaat niet meer koperkleurig, maar grijszwart. De houtskool in de kom begint te gloeien en wordt grijswit. Nadat de actieve kool in de porseleinen kom is gegoten, is het grijszwarte vel onder de actieve kool roodbruin geworden.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 1 spatelpunt actieve kool – 1plaatje koper
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – redoxreactie
13. Kwik
13.1. Kwikdruppel op en neer

- Info: Breng de kwik op een petrischaaltje. Overgiet het met de zwavelzuuroplossing totdat de kwik onder staat. Breng nu een nagel zodat deze steekt in het zwavelzuur en juist contact maakt met de kwik. De kwikdruppel begint plots te trillen.
- Moeilijkheid: gemiddeld
- Chemische stoffen: 1.5 ml kwik – 6 mol/l H2SO4 – 0.1 mol/l K2Cr2O7
- Thema: enkelvoudige stoffen – chemisch evenwicht
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – oscillerende reactie
14. Lithium
14.1. Lithiumbatterij

- Info: Hoe verkrijg ik lithium uit een lithiumbatterij? We kunnen lithium uit een batterij halen door veel te pellen aan de batterij.
- Moeilijkheid: gemiddeld
- Chemische stoffen: lithiumbatterij,
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – galvanische cel
14.2. Drakenadem

- Info: Hoe kunnen we lithium herkennen?
- Moeilijkheid: eenvoudig
- Chemische stoffen: sprayfles – 100ml ethanol – 3g lithiumzout
- Thema: enkelvoudige stoffen – bouw van atoom
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – atoomodel Bohr – vlamproef
14.3. Reactie van lithium en natrium met water

- Info: Wat gebeurt er als alkalimetalen reageren met water? De alkalimetalen reageren hevig met vorming van vlam door warmte en vorming van waterstofgas
- Moeilijkheid: eenvoudig
- Chemische stoffen: Mes – Klein stukje rond filter – 1 stukje Li en Na
- Thema: enkelvoudige stoffen – periodiek systeem
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – alkalimetalen
14.4. Lithium en ethanol

- Info: Alkalimetalen reageren heftig met water (OH-groep). Is dat hetzelfde met ethanol (ook OH-groep)? Het lithium schijnt omdat het een metaal is. Alleen verse lithium snijvlakken glanzen doordat het reageert met de vochtigheid in de lucht.
Er moet waterstofgas in de reageerbuis zitten . - Moeilijkheid: gemiddeld
- Chemische stoffen: 5 ml ethanol – 1 stukje lithium
- Thema: enkelvoudige stoffen – periodiek systeem
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – alkalimetalen
15. Lood
15.1. Een oplaadbare batterij maken

- Info: Hoe kunnen we een oplaadbare batterij maken?
- Moeilijkheid: gemiddeld
- Chemische stoffen: loodfolie – platte batterij van 4.5V – motortje 2V (schakeling van lampje) – zwavelzuuroplossing 5%
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – galvanische cel – elektrolyse
16. Magnesium
16.1. Verhit magnesium reageert met water

- Info: Hoe beïnvloedt kokend water de verbranding van magnesiumlint? Verhit magnesium reageert met water waarin zuurstof gebonden zit. Magnesium is onedeler dan waterstof
- Moeilijkheid: gemiddeld
- Chemische stoffen: Water – Magnesiumlint
- Thema: enkelvoudige stoffen – periodiek systeem
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – aardalkalimetalen
16.2. Magnesium en zink reageren met dichloor

- Info: Hoe reageren zink en magnesium met dichloor? Beide metalen reageren onder fel licht fenomeen in een sterk exotherme reactie met het chloor. Chloor behoort tot de groep van halogenen..
- Moeilijkheid: gemiddeld
- Chemische stoffen: Zinkpoeder – Chloorgas – Magnesiumlint
- Thema: enkelvoudige stoffen -chemische reactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – reactie metaal en niet-metaal
16.3. Flitslicht

- Info: Hoe werden voorwerpen belicht vóór de uitvinding van de elektrische flitser? Er treedt een heldere, flitsachtige verbranding op. Wat overblijft is een ongedefinieerde, bruin / grijs / zwarte massa.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Aluminium schaal – 20 g suiker – 10 g kaliumchloraat – 10 g kaliumpermanganaat – 10 g magnesiumpoeder
- Thema: enkelvoudige stoffen – verbrandingsreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – verbranding magnesium
16.4. Potloodslijper branden

- Info: Wat gebeurt er als je een metalen puntenslijper in de brandende vlam houdt? De puntenslijper begint te branden aan de randen waar de brandervlam raakt.Er worden helderwitte lichtflitsen gevormd die op kleine sterren lijken.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Puntenslijper (gemaakt van metaal)
- Thema: enkelvoudige stoffen – verbrandingsreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – verbranding magnesium
16.5. Blus magnesiumbrand met water

- Info: Wat gebeurt er als je een vuur van een metaal met water blust? Het magnesium brandt met een helderwitte vlam. Zodra er water wordt toegevoegd, gaat de vlam niet uit, maar wordt hij groter als een knipperende vlam.
- Moeilijkheid: gemiddeld
- Chemische stoffen: 10 cm magnesiumlint – 10 druppels water
- Thema: enkelvoudige stoffen – verbrandingsreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – verbranding magnesium
17. Natrium
17.1. Bereiden van natriummetaal

- Info: Hoe kunnen we natriummetaal bereiden? Natrium kunnen we bereiden vertrekkende vanuit natriumhydroxide. Onder invloed van spanning zal natrium ontstaan
- Moeilijkheid: moeilijk
- Chemische stoffen: vast NaOH
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – elektrolyse
17.2. Golflengte van een natriumlamp

- Info: Hoe kunnen we de golflengte van een natriumlamp bepalen? Licht van een natriumlamp wordt doorheen een vlam gestuurd waarin veel natriumionen zitten, deze zijn afkomstig van een prop die eerst in een sterke oplossing van keukenzout gedompeld werd en daarna in de vlam gehouden wordt. Op een scherm ziet men een lichtvlek met daarin donkere gebieden die overeenstemmen met gebieden van hoge natriumconcentratie.
- Moeilijkheid: gemiddeld
- Chemische stoffen: voeding voor Na-lamp – pekelwater (NaCl)
- Thema: enkelvoudige stoffen – bouw van atomen
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – atoommodel Bohr
18. Silicium
18.1. Bereiden van zuiver zand

- Info: Hoe kunnen we met een neutralisatiereactie zand maken?
- Moeilijkheid: gemiddeld
- Chemische stoffen: zoutzuur (HCl) 2 mol/l (35ml) – waterglas (Na2SiO3) 37% (20ml) – water (H2O) (50ml)
- Thema: enkelvoudige stoffen – reacties
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – sterk zuur verdrijft zwak zuur uit zouten
18.2. Chemische tuin

- Info: Kunnen we een chemische tuin maken door met zoutkristallen te laten reageren met waterglas?
- Moeilijkheid: gemiddeld
- Chemische stoffen: natriumsilicaatoplossing (Na2O3Si) (waterglas) – Co(NO3)2.6H2O(s): cobalt(II)nitraat – Fe(NO3)3.9H2O(s): ijzer(III)nitraat – Mg(NO3)2.6H2O(s): magnesiumnitraat – MnSO4.7H2O(s): mangaan(II)sulfaat – Ni(NO3)2.6H2O(s):: nikkel(II)nitraat
- Thema: enkelvoudige stoffen – stofeigenschappen
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – diffusie
18.3. Maken van silicium

- Info: Hoe maak je d.m.v. Magnesium zuiver silicium uit zand? Magnesium reageert met siliciumdioxide (zand en verbranding) , en vormt het zuiver element Silicium.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Zand – Magnesiumpoeder – Verdund zwavelzuur 1 mol/l
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – spanningsreeks metalen
18.4. Maken van siliconen uit zand

- Info: Hoe kunnen we siliconen maken uit zand? Wanneer magnesium en zand samen worden verwarmd, wordt er silicium gevormd door een exotherme reactie. Dit reactieproduct wordt aan zoutzuur toegevoegd om het gevormde magnesiumoxide en niet gereageerd magnesium te verwijderen.
- Moeilijkheid: gemiddeld
- Chemische stoffen: 1 g droog magnesiumpoeder (Licht ontvlambaar) – 1 g droog zilverzand – ongeveer 50 mL van ongeveer 2 mol/l zoutzuur
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen
19. Stikstof
19.1. Bereiding van stikstofgas

- Info: Hoe kan je stikstofgas maken?Door de ontbinding van vloeibaar ammoniumnitriet ontstaat er stikstofgas. Het bruisen is oscillerend doordat er bij deze reactie een natuurkundig evenwicht is tussen oplossingen, condensatiekernen, kleine en grote gasbelletjes en het verdwijnen van stikstofgas uit de oplossing.
- Moeilijkheid: gemiddeld
- Chemische stoffen: gedestilleerd water – zoutzuur 2mol/l – ammoniumchloride – natriumnitriet
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – oscillerende reactie
19.2. Geheime boodschap met ammoniumchromaat

- Info: Hoe kan men stikstofgas verkrijgen uit ammoniumdichromaat? Door het verwarmen van ammoniumdichromaat, ontstaat er door ontleding stikstofgas, chroomoxide en water.
- Moeilijkheid: gemiddeld
- Chemische stoffen: ammoniumdichromaat – gedestilleerd water
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – gasvorming door redoxreactie
20. Tin
20.1. Maak een tinnen sterrenplaatje
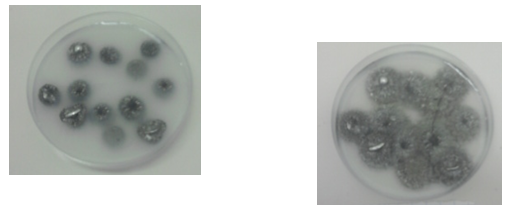
- Info:Hoe krijg ik de grootste en mooiste sterretjes van tin ? Op de zinkkorrels gebeurt een afzetting van tin. Dit zorgt voor een stervormige afzetting in het petrischaaltje.
- Moeilijkheid: gemiddeld
- Chemische stoffen: tin(II)chloride – 18% zoutzuur
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – elektrolyse
20.2. Sterren van tin (methode2)

- Info:Hoe krijg ik de grootste en mooiste sterretjes van tin ? Op de zinkkorrels gebeurt een afzetting van tin. Dit zorgt voor een stervormige afzetting in het petrischaaltje.
- Moeilijkheid: gemiddeld
- Chemische stoffen: tin(II)chloride – 18% zoutzuur
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – elektrolyse
21. Waterstof
21.1.Bereiding van diwaterstof

- Info: Hoe kunnen we waterstofgas bereiden?
- Moeilijkheid: gemiddeld
- Chemische stoffen: Mg lint – HCl 2mol/l
- Thema: enkelvoudige stoffen – redoxreactie – chemische reactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – spanningsreeks metalen – reactie metaal en zuur
21.2. Elektrolyse van waterstofchloride

- Info: Hoe kunnen we waterstofgas bereiden? Elektrolyse van zoutzuur
- Moeilijkheid: eenvoudig
- Chemische stoffen: druppelflesje gevuld met HCl – oplossing
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – elektrolyse
21.3. Knalgas ontploft in een ei

- Info: Hoe kunnen we knalgas vormen in een ei? Het ei heeft zich gevuld met het knalgas doordat dit lichter is dan lucht en het stijgt. Wanneer we dan een lucifer in de buurt houden van het ei, ontploft het ei. Door de reactie van HCl met magnesium ontstaat er H2-gas, ook wel knalgas genoemd.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Uitgeblazen ei – Tape – HCl
- Thema: enkelvoudige stoffen – redoxreactie – chemische reactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – exo-energetische reactie – synthesereactie
21.4. Migratie van waterstof is sneller dan lucht

- Info: Het waterstofgas is in staat te migreren door de ballon
- Moeilijkheid: eenvoudig
- Chemische stoffen: ballon van 25cm diameter – elastieken – waterstofgas 60ml
- Thema: enkelvoudige stoffen – stofeigenschappen
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – diffusie
21.5. Plaats van waterstof in de spanningsreeks van metalen

- Info: Hoe reageren verschillende metalen met HCl ?
- Moeilijkheid:gemiddeld
- Chemische stoffen: 6 mol/l HCl oplossing – Stukjes van volgende metalen: Mg, Pb, Fe, Zn en Cu
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – spanningsreeks van metalen
21.6. Potloodslijper vormt knalgas en verdwijnt in zuur

- Info: De slijper is uit magnesium. Magnesium verbrandt na warmtetoevoer en geeft een sterk wit licht.
- Moeilijkheid:gemiddeld
- Chemische stoffen: Magnesiumpotloodslijper – geconcentreerde HCl
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – spanningsreeks van metalen
21.7. Racer is de kleinste waterstofauto ter wereld

- Info: Wanneer we de energiebron op het autootje aansluiten, ontstaat er een chemische reactie met het water. Het water splitst zich namelijk op in waterstofgas in het ene vaatje en zuurstofgas in het andere vaatje.
- Moeilijkheid:gemiddeld
- Chemische stoffen: Kleine versie van het toestel van Hoffman – brandstofcel
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – ontleding water – knalgas
21.8. Verhit magnesium reageert met water

- Info: Hoe beïnvloedt kokend water de verbranding van magnesiumlint? Verhit magnesium reageert met water waarin zuurstof gebonden zit. Magnesium is onedeler dan waterstof
- Moeilijkheid:gemiddeld
- Chemische stoffen: Water – Magnesiumlint
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – spanningsreeks van metalen
21.9. Verschijnen en verdwijnen van een kaarsvlam met waterstofgas

- Info: Hoe beïnvloedt kokend water de verbranding van magnesiumlint? Verhit magnesium reageert met water waarin zuurstof gebonden zit. Magnesium is onedeler dan waterstof
- Moeilijkheid:gemiddeld
- Chemische stoffen: HCl 2 mol/l 5ml- 1 cm Mg lint
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – spanningsreeks van metalen – verbrandingsreactie
21.10. Waterstofgas aantonen

- Info:Wat is de plaats van H+ in de spanningsreeks van metalen?
- Moeilijkheid:gemiddeld
- Chemische stoffen: Vaste stoffen, en poeder: Zn, Fe, Cu, Mg, Sn, Al, – lucifer, – HCl-oplossing 6 mol/l
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – spanningsreeks van metalen – verbrandingsreactie
21.11.Waterstofgas vormen

- Info:Hoe kun je waterstofgas detecteren? De reactie tussen een basismetaal en een zuur levert altijd waterstof en een zout op.
De waterstof verzamelt zich in de bovenste reageerbuis omdat het een lagere dichtheid heeft dan lucht. - Moeilijkheid:gemiddeld
- Chemische stoffen: HCl 2 mol/l 5ml- 1 cm Mg lint – kaars
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – spanningsreeks van metalen – verbrandingsreactie
21.12. Zelfontbranding van een lucifer

- Info:Hoe kun je waterstofgas detecteren? De reactie tussen een basismetaal en een zuur levert altijd waterstof en een zout op.
De waterstof verzamelt zich in de bovenste reageerbuis omdat het een lagere dichtheid heeft dan lucht. - Moeilijkheid:gemiddeld
- Chemische stoffen: HCl 2 mol/l 5ml- 1 cm Mg lint – kaars
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – spanningsreeks van metalen – verbrandingsreactie
21.13. Maken van knalgas met aluminium en ontstopper

- Info:Hoe kunnen we met dagdagelijkse stoffen waterstofgas maken? Na een tijd ontstaat gas in de erlenmeyer. Deze wordt opgevangen in de detergentoplossing. De bellen geven een knal als ze worden aangestoken.
- Moeilijkheid:gemiddeld
- Chemische stoffen: Aluminiumfolie – NaOH
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – spanningsreeks van metalen – verbrandingsreactie – knalproef
21.14. Waterstofgasbellen

- Info:Hoe kan ik waterstofgas creëren uit water? Door elektrolyse toe te passen op water ontstaat er waterstofgas.
- Moeilijkheid:gemiddeld
- Chemische stoffen: lucifer – Natriumsulfaat-oplossing 5%
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – elektrolyse – knalproef
21.15. Zelf een elektrolysetoestel bouwen

- Info:Hoe kan ik waterstofgas creëren uit water? Door elektrolyse toe te passen op water ontstaat er waterstofgas.
- Moeilijkheid:gemiddeld
- Chemische stoffen: lucifer – Natriumsulfaat-oplossing 5%
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – elektrolyse – knalproef
22. Zilver
22.1. Kerstbal maken

- Info:Hoe maak je je eigen spiegel?
- Moeilijkheid:gemiddeld
- Chemische stoffen: Salpeterzuur 70% – AgNO3 – KOH – Glucose – Ammoniak 35%
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – zilverspiegel
22.2. Zilver maken met honing

- Info:Hoe maak je je eigen spiegel? In een basisch milieu reageert fructose tot glucose. De reactie met de basische zilveroplossing vormt zilvermetaal
- Moeilijkheid:gemiddeld
- Chemische stoffen: honing – wijnsteenzuur – ethanol 96% – zilvernitraat – ammoniumnitraat – NaOH – water
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – zilverspiegel
22.3. Zilveren snoepparels

- Info:Wat gebeurt er wanneer we snoepparels in een oplossing brengen? Zilver is een edel metaal en is hierdoor een (relatief) zwakke reductor. Zilver zal dus niet reageren met de meeste zure oplossingen. Het zal dus ook alleen zilverionen vormen in aanwezigheid van een sterke oxidator.
- Moeilijkheid:gemiddeld
- Chemische stoffen: zilveren snoepparels – salpeterzuur (65%) – natriumchloride (0,1 mol/l) – water
- Thema: enkelvoudige stoffen – redoxreacties
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – oxidans
22.4. Zilveren spiegel

- Info:Hoe kunnen we een spiegel maken? De zilverlaag komt er door een reductie van zilverionen uit ons mengsel met een aldehydegroep. Bij ons is de aldehydegroep de glucose. De gereduceerde zilver zet zich af op de buitenkant van de maatkolf. Dit vormt een spiegel.
- Moeilijkheid:gemiddeld
- Chemische stoffen: Zilvernitraatoplossing 5g/l – Glucose-oplossing 5 g/l (geen suiker) – Ammoniak oplossing 10% (in labo te vinden op 25%) – Natriumhydroxide-oplossing 5g/l
- Thema: enkelvoudige stoffen – organische stoffen
- Tijd: 25 min
- Begrippen: enkelvoudige stoffen – redoxreactie – aldehyden – zilverspiegel
22.5. Explosief Zilver

- Info:Hoe kun je vast materiaal doen knallen? Door acetyleengas te laten reageren met Tollensreagens, krijgen we zilveracetylide. Dit een zeer instabiele neerslag die gevormd, door er een vlam aan te houden gaat de explosie plaatsvinden.
- Moeilijkheid:gemiddeld
- Chemische stoffen: Calciumcarbide – Water – Tollensreagens
- Thema: enkelvoudige stoffen – redoxreactie – organische stoffen
- Tijd: 25 min
- Begrippen: enkelvoudige stoffen – calciumcarbide – ethyn
23. Zink
23.1. Explosie van een ei

- Info:Breng wat waterstofgas in een uitgeblazen ei door het op een proefbuis met HCl 3M en Zn poeder te zetten. Steek het op afstand aan met een lont.
- Moeilijkheid:gemiddeld
- Chemische stoffen: uitgeblazen ei – waterstofgas bekomen door reactie tussen HCl en Zn-poeder
- Thema: enkelvoudige stoffen – chemische reactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – exo-energetische reactie – knalproef
23.2. Maak een kleurrijk muntenkunstwerk

- Info:Maak zelf gouden en zilveren muntstukken
- Moeilijkheid:gemiddeld
- Chemische stoffen: zinkkorrels (Zn) – NaOH – azijnzuur (huishoudazijn) – koperen muntstukjes
- Thema: enkelvoudige stoffen – mengsel – chemische reactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – messing
23.3. Zink en koperchloride

- Info:Wat gebeurt er wanneer we zink en koperdichloride samenvoegen? Redoxreactie tussen koperionen en een onedel metaal. De Cl– -ionen katalyseren de reactie. Deze reactie treedt daarom niet op met kopersulfaat.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Zinkpoeder – koper(II)chloride
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – spanningsreeks metalen
23.4. De reactie tussen zink en zoutzuur

- Info:Wat gebeurt er wanneer we zink en zoutzuur samenvoegen? Er ontstaat een chemische reactie met gasontwikkeling. Deze chemische reactie is een exo-energetische reactie.
- Moeilijkheid: eenvoudig
- Chemische stoffen: waterstofchloride (2mol/l ) – zink poeder
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – spanningsreeks metalen – reactie zuur en metalen
24. Zuurstofgas
24.1. Bereiding van zuurstofgas
- Info: Hoe kan je zuurstofgas maken? Je kan zuurstofgas maken door gebruik te maken van MnO2, H2O2 en KI. Deze laatste treedt op als katalysator.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 0,05 g KI – 5 ml 6% H2O2 – spatelpunt MnO2– poeder
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – katalysator – ontledingsreactie
24.2. De blauwe kolfproef

- Info: Methyleenblauw is een aromatische verbinding die opgelost in water blauw kleurt. Het is een redoxindicator die een duidelijke kleurverandering ondergaat op een specifieke potentiaal. Methyleenblauw wordt gereduceerd tot een kleurloze vorm.Als er niet voldoende zuurstof aangeleverd wordt bv als de fles teveel gevuld is dan zal zich geen blauwe kleur vormen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 1 korrel KOH 0,01 g – dextrose 0.9 g – 1 druppel methyleenblauw
- Thema: enkelvoudige stoffen – redoxreactie – chemisch evenwicht
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – katalysator – redoxindicator
24.3. Dynamietzeep

- Info: Verbind een spuit met waterstofgas via een darm aan een spuit met zuurstofgas. Druk het waterstofgas bij het zuurstofgas.Meng wat in het sop om wat bellen te bekomen.Spuit de inhoud onder het zeepoppervlak. Steek een aantal zeepbellen met een brandende lucifer aan.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 30 ml waterstofgas – 30ml zuurstofgas – 10ml 3% zeepoplossing
- Thema: enkelvoudige stoffen – redoxreactie – chemische reactie
- Tijd: 10 min
- Begrippen: enkelvoudige stoffen – knalgas – exo-energetische reactie
24.4. Exotherme reactie met gedroogde gist

- Info: H2O2 ontbindt in H2O en O2. Het proces wordt gekatalyseerd door de aanwezigheid van
gist.Het gist bevat namelijk het katalase enzyme. - Moeilijkheid: eenvoudig
- Chemische stoffen: 1 pakketje of koffielepel gedroogde gist- 5% H202
- Thema: enkelvoudige stoffen – redoxreactie – chemische reactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – katalyse
24.5. Koolstofdioxide voorkomt branden

- Info:Breng het zuurstofgas in een grote proefbuis via een slang. Steek de kaars aan en breng het in de proefbuis. De kaars brandt heviger.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 50ml zuurstofgas – 2ml kalkwater
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – verbrandingsreactie
24.6. Maak de meeste olifantenpasta

- Info: H2O2 ontbindt in H2O en O2. Het proces wordt gekatalyseerd door de aanwezigheid van
gist.Het gist bevat namelijk het katalase enzyme. - Moeilijkheid: eenvoudig
- Chemische stoffen: KI-oplossing (10 g in 10 ml water); – detergent; – gedestilleerd water; – H2O2 (30%).
- Thema: enkelvoudige stoffen – redoxreactie – chemische reactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – katalyse
24.7. Reactie tussen zuurstofgas en methyleenblauw
- Info:Eerst ontstaat in de pipet door reactie tussen H2O2 en KMnO4 O2 gas. De kleurloze oplossing van methyleenblauw wordt terug blauw door contact met zuurstofgas.
- Moeilijkheid: eenvoudig
- Chemische stoffen: H202 – 5%KMnO4 0,1 mol/l – Methyleenblauwoplossing – Glucose
- Thema: enkelvoudige stoffen – redoxreactie – chemische reactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – katalyse
24.8. Zuurstof bevordert verbranding

- Info: Breng het zuurstofgas in een grote proefbuis via een slang. – Steek de kaars aan en breng het in de proefbuis. De kaars brandt heviger.
- Moeilijkheid: eenvoudig
- Chemische stoffen: zuurstofgas – kalkwater
- Thema: enkelvoudige stoffen – redoxreactie – chemische reactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – verbrandingsreactie
24.9. Bruisend koper

- Info:Hoe kunnen we koper proper maken door het te laten bruisen? Vanaf het moment dat het koperplaatje in de oplossing wordt gezet treedt een reactie op aan het koperoppervlak met vorming van gasbellen. Het plaatje wordt lichter rood van kleur en de oplossing wordt blauw.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Koperplaatje – H2SO4 geconcentreerd – H2O2 geconcentreerd
- Thema: enkelvoudige stoffen – redoxreactie – chemische reactie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – katalysator
24.10. Drie lagen gekleurde vloeistof

- Info:Hoe kunnen we een bruisend mengsel maken met drie verschillende kleuren? Van het moment dat het zuurstofwater is toegevoegd, treedt er reactie op aan de interfase.. De interfase wordt donker blauw. Geleidelijk aan verkleurt de ether ook blauw en begint te bruisen. Wanneer dichromaat en waterstofperoxiden in zuur milieu reageren ontstaat een onstabiele vorm: chroomoxide peroxide. Het toegevoegd diethylether stabiliseert de verbinding en gaat hierdoor verkleuren.
- Moeilijkheid: gemiddeld
- Chemische stoffen: diethylether – H2SO4 6 tot 9 mol/l – H2O2 geconcentreerd – K2Cr2O7-oplossing 5%
- Thema: enkelvoudige stoffen – redoxreactie – organische stoffen
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – katalysator
24.11. Een bloedende nagel

- Info:Hoe kunnen we ervoor zorgen alsof het lijkt dat een nagel bloedt? De oplossing is helder. Als de nagel in de oplossing wordt gebracht , lijkt het alsof de nagel begint te bloeden.
- Moeilijkheid: gemiddeld
- Chemische stoffen: 100 ml 10% KSCN-oplossing – geconcentreerde HCl-oplossing – geconcentreerde waterstofperoxide oplossing
- Thema: enkelvoudige stoffen – complexreactie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – katalysator
24.12. Identificatie van zuurstofgas

- Info: Hoe kan je aantonen dat er na een reactie, zuurstofgas is gevormd? Met behulp van een houtenspaander/lucifer kan men aantonen dat er zuurstofgas gevormd is. Deze houtenspaander/lucifer zal meer vlam vatten wat te wijten is aan een hogere concentratie zuurstof. Bij de verbranding wordt er CO2 gevormd.
- Moeilijkheid: gemiddeld
- Chemische stoffen: 30 ml zuurstofgas – 2 ml kalkwater
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – identificatiereactie zuurstofgas – verbrandingsreactie
24.13. Stijgend water in een glas met een brandende kaars

- Info: Waarom stijgt het water in een glas dat boven een brandende kaars wordt gezet? De lucht in het glas wordt opgewarmd door de warmte van de kaars. Nadat de kaars dooft, koelt de lucht af en daalt de druk. De atmosferische druk buiten het glas is groter en duwt het water in het glas, het water wordt opgezogen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Kaars – lucifers
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 10 min
- Begrippen: enkelvoudige stoffen – verbrandingsreactie
25. Zwavel
25.1. Endotherme reactie met zwavel

- Info: Hoe kunnen we een spontane endotherme reactie uitvoeren met zwavel? De drijfkracht van de reactie is het vrijzetten van water uit beide zouten en de vorming van SO2. Tijdens het proces valt thiosulfaat uiteen in SO2 en S.De entropie neemt door de gasvorming toe waardoor het endotherme proces spontaan verloopt.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Fe(NO3)3.9H2O – Na2S2O3.5H2O
- Thema: enkelvoudige stoffen – chemische reactie
- Tijd: 15 min
- Begrippen: enkelvoudige stoffen – endo-energetische reactie
25.2. Naalden van zwavelkristallen

- Info: Zwavel is oplosbaar in hete olie, maar niet in koude, en evenmin in koude wasbenzine.
De schijnbaar amorfe zwavelbloem (d.w.z. zonder structuur) lost op, maar vormt bij het neerslaan kristallen en is dan duidelijk niet meer amorf. - Moeilijkheid: gemiddeld
- Chemische stoffen: kleurloze lampolie (paraffineolie) – Zwavelbloem
- Thema: enkelvoudige stoffen – chemische reactie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – kristalvorming
25.3. Ondergaande zon

- Info: Hoe kunnen we de een ondergaande zon voorstellen door een chemische reactie?
- Moeilijkheid: gemiddeld
- Chemische stoffen: 3 ml HCl 1 mol/l – 20 ml (0,1 mol/l) thiosulfaatoplossing
- Thema: enkelvoudige stoffen – reactiesnelheid
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – reactiesnelheid, invloed concentratie – klokreactie
25.4. Vorming van FeS met zwavel

- Info: Hoe kunnen we aantonen dat we ijzersulfide (FeS) anders is dan ijzer (Fe) en zwavel (S)?
- Moeilijkheid: gemiddeld
- Chemische stoffen: Zwavel poeder (S-poeder) – Demiwater
- Thema: enkelvoudige stoffen – chemische reactie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – wet van constante verhouding
25.5. Zwavelpolymeer

- Info:Giet de hete zwavel met een laag debiet in water. Wanneer dit wordt afgekoeld worden er rubberachtige polymeer vezels gevormd. Dit polymeer is niet stabiel bij kamertemperatuur en zal terug uitharden en terugkeren naar zijn originele gele kleur.
- Moeilijkheid: gemiddeld
- Chemische stoffen:Zwavel poeder (S-poeder) – Demiwater
- Thema: enkelvoudige stoffen – kunststoffen
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – plastisch polymeer
25.6. Tijdelijk ontkleuren van bloemblaadjes met zwaveldioxide

- Info: Hoe kunnen we een rode roos tijdelijk ontkleuren met zwavel? De ontkleuring is een redoxreactie met SO32- waarbij zuurstof wordt onttrokken aan het pigment. Dit is tijdelijk vermits het gereduceerd pigment terug zuurstof kan opnemen uit de lucht en terug de oorspronkelijke kleur krijgen.
- Moeilijkheid: gemiddeld
- Chemische stoffen:Zwavel poeder (S-poeder)
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – verbrandingsreactie van zwavel
25.7. Zwart poeder

- Info: Hoe maak je zelf zwart poeder? Uit de drie vaste stoffen ontstaat een grote hoeveelheid gasvormige stoffen die relatief weinig ruimte innemen. Het volume neemt toe met een factor 2000.
- Moeilijkheid: gemiddeld
- Chemische stoffen: 75% kaliumnitraat – 10% zwavelpoeder – 15% houtskool
- Thema: enkelvoudige stoffen – redoxreactie
- Tijd: 20 min
- Begrippen: enkelvoudige stoffen – buskruit






