Inwerking van zuren op metalen
1.Onderzoeksvraag
Hoe werken zuren in op metalen?
2.Voorbereiding
a.Begrippen als achtergrond voor experiment
- Zuur: Een zuur is in de scheikunde een stof die protonen (H+–ionen) af kan staan. Wat er overblijft is de negatieve zuurrest.
- Chemische reactie: Een chemische reactie is een proces waarbij bepaalde verbindingen (moleculen) of atomen via niet-fysische weg worden omgezet in andere verbindingen via het vormen dan wel breken van chemische bindingen
b.Materiaal + stoffen
- verdund HCl 6mol/l
- verdund H2SO4 6mol/l
- geconcentreerd salpeterzuur 12mol/l
- kleine maatcilinder met 1 ml CuSO4-oplossing 1%
- proefbuisrekje met zes proefbuizen
- bunsenbrander, lucifers, houtspaander
- 6 cm magnesiumlint
- 1 koperplaatje
- papier met mespunt ijzerpoeder
- ijzernagels
- zinkplaatjes
- 3 aluminiumplaatjes
c.Bereiding oplossingen
HCl 6mol/l vertrekkend vanuit geconcentreerde HCl:
Molecuulmassa HCl = 36 g/mol
Voor een 6 mol/l-oplossing hebben we dus 6 * 36 g/mol nodig.
Voor 1 l oplossing heb je dus 216 gram HCl nodig
1 ml HCl bevat 0,35 gram zuivere HCl.
We hebben dus 21,6/0,35 HCl nodig. Voor 100 ml oplossing
Voor 100 ml HCl 6 mol/l hebben we dus 61, 71 ml HCl nodig en 38,29 ml H2O
H2SO4 3mol/l vertrekkend vanuit geconcentreerd H2SO4
Molecuulmassa H2SO4= 98,1 g/mol
Voor een 3 mol/l-oplossing hebben we dus 6 * 98,1 g/mol nodig.
Voor 1 l oplossing heb je dus 588,6 gram H2SO4 nodig
1 ml H2SO4 © bevat 0,98 gram zuivere H2SO4
We hebben dus 58,9/0,98 H2SO4 nodig. Voor 100 ml oplossing
Voor 100 ml H2SO4 3 mol/l hebben we dus 60,1 ml H2SO4 nodig en 39,9 ml H2O
d.Opstelling (foto)
e.Etiketten
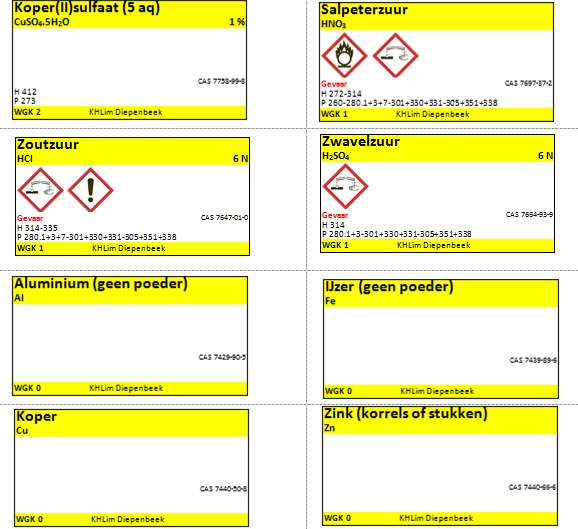
3.Uitvoeren
a.Werkwijze
- Breng in 5 pb telkens 5 ml verdund HCl.
- Voeg tegelijkertijd de volgende vijf metalen bij het zuur, elk in een afzonderlijke proefbuis: koperplaatje, ijzernagel, aluminiumplaatje, zinkplaatje en magnesiumlint.
- Onderzoek met een brandende houtspaander de brandbaarheid van het gas.
- Breng telkens bij 2 proefbuizen met 5 ml verdund HCl 6mol/l een even groot stukje zuiver aluminium. Voeg dan bij één van de twee proefbuizen 1 ml kopersulfaatoplossing.
- Breng in twee proefbuizen telkens 5 ml verdund HCl 6mol/l. Voeg bij de ene een ijzeren nagel en bij de andere een mespunt ijzervijlsel.
- Breng telkens een stukje zink in 5 ml oplossing van verdund zwavelzuur 3 mol/l en geconcentreerd salpeterzuur 12 mol/l.
b.Waarneming (+ foto’s)
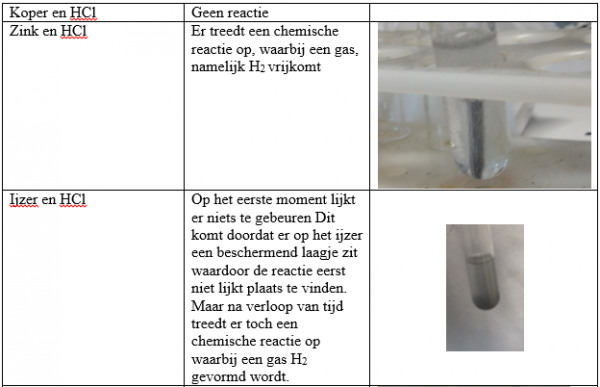


4.Reflecteren
a.Optredende reacties
Mg + 2 HCl –> MgCl2 + H2
2 Al + 6 HCl –> 2 AlCl3 + 3 H2
Zn + 2 HCl –> ZnCl2 + H2
2 Fe + 6 HCl –> 2 FeCl3 + 3 H2
b.Besluit
We kunnen besluiten dat bepaalde metalen wel met water reageren en anderen niet. Elk metaal reageert anders wanneer het in contact komt met een zuur. Dit verschijnsel is te wijten aan de edelheid van metalen. De edelheid van metalen is niets anders dan een maat voor de reactiviteit van metalen met oxidatoren. Edele metalen reageren bijna niet, onedele metalen reageren wel. In ons voorbeeld kunnen we dus besluiten dat Mg het meest onedel is, gevolgd door Al, Zn, Fe en tot slot Cu. Cu is dus het meest edel en zal dus het minst reactief zijn.
5. Aanvullingen
- Werk onder de zuurkast
- Laat deze proven niet door de leerlingen uitvoeren
- Gebruik bij het uitvoeren van deze proeven handschoenen, labojas en veiligheidsbril.
- Merk alle proefbuizen zodat je duidelijk de verschillende metalen kan onderscheiden
- Laat de leerlingen de waarnemingen doen (metalen)
Bronnen






