| BEGRIP | ZUUR-BASETITRATIE
OMSLAGGEBIED OMSLAGPUNT STANDAARDOPLOSSING STOICHIOMETRISCH PUNT EQUIVALENTIEPUNT
|
| DEFINITIE LEERPLAN |
|
|
EXPERIMENTEN |
|
|
FILMS |
Lesvideo’s:
|
| QUIZZEN | |
|
SPELLEN |
|
|
CARTOONS |
|
|
ANIMATIES SIMULATIES |
Titraties
Titratiecurve |
|
APPS |
Titratiecurven
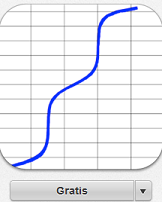
De app simuleert de titratie van een mono- of diprotisch zuur met 50 ml base. De gebruiker voert geschikte concentraties van zuur, base en het volume van het te titreren zuur in, evenals de pKa-waarde (n). Als u een schuifregelaar verplaatst, kunnen twee verschillende waarden voor de eerste pKa grafisch worden vergeleken. https://itunes.apple.com/nl/app/titrate/id801793893?mt=8
Waterige zuur-base-evenwichten kunnen vanuit meerdere perspectieven worden bestudeerd hoe verschillen in chemische structuur de chemische reactiviteit kunnen veranderen. Vaak neemt slechts één vorm van een molecuul deel aan een reactie en de fractie van die vorm kan aanzienlijk veranderen met kleine veranderingen in de pH. https://itunes.apple.com/be/app/titration-1.0/id1020960305?l=nl&mt=8 https://play.google.com/store/apps/details?id=com.nof.makanoh.simulasititrasiasambasa
Voer een titratie uit zo snel en zo nauwkeurig mogelijk https://itunes.apple.com/nl/app/utitrate/id619147829?mt=8 https://play.google.com/store/apps/details?id=com.mt.lab.ana.ti.uTitrateGame
De app analyseert de kleurveranderingen die betrokken zijn bij een titratie https://itunes.apple.com/nl/app/titration-simulator/id324156977?mt=8 https://play.google.com/store/apps/details?id=com.color.Titration_ColorCam
Deze app gebruikt de Henderson-Hasselbach-vergelijking en concepten in zuur-base-evenwichten om een simulatie van een titratie uit te voeren om de concentratie te bepalen. Titreren van een sterk zuur (HCl) met een sterke base (0,1 mol/l NaOH) of een zwak zuur (HCOOH) met een sterke base (1,0 mol/l NaOH). De concentratie van het zuur is onbekend om een laboratoriumexperiment te simuleren, maar het volume wordt vastgesteld op 50 ml. De pH-indicator is fenolftaleïne. https://itunes.apple.com/be/app/titration-simulator-to-learn/id1027828427?l=nl&mt=8 https://play.google.com/store/apps/details?id=com.nof.makanoh.simulasititrasiasambasa |
|
WEB2.0 |
|
|
KINDEREN EN CHEMIE |
Zuur-base titratie
Omslagpunt – omslaggebied – stoichiometrisch punt – equivalentiepunt
Definities
- zuur-basetitratie: Een zuur-basetitratie is een volumetrische methode om de concentratie van een zuur of een base te bepalen.
- omslaggebied:Het omslaggebied van een zuur-base-indicator is het pH-gebied waarin de kleurverandering gebeurt.
- omslagpunt: Het omslagpunt is de centrale pH-waarde van het omslaggebied.
- standaardoplossing: De standaardoplossing bij een titratie is de oplossing met de nauwkeurig gekende concentratie.
- stoichiometrisch punt (SP): Op het stoichiometrisch punt hebben stoichiometrisch hoeveelheden van zuur en base met elkaar gereageerd.
- def titratie
- def equivalentiepunt
- def titratieberekening
- wikipedia omslaggebied
- wikipedia titratie
Experimenten
- Bepaling van gehalte azijnzuur in tafelazijn in een nunclonschaaltje
- Bepaling van het alcoholgehalte in vensterreiniger door titratie
- Bepaling van het gehalte citroenzuur in een bloedrode sinaasappel
- Hoeveel koolstofdioxide bevat uitgeademde lucht?
- Dosering van vitamine C
- Het azijnzuurgehalte bepalen door titratie?
- Hoe kun je een hoeveelheid koolstofdioxide doseren?
- Microschaaltitratie van vitamine C in fruitsap
- Microschaaltitratie
- Neutralisatiereactie door temperatuurmeting
- Neutralisatiereactie
- Puzzeltitratie
- Titratie van bicarbonaat in leidingwater
- Titratie van fosforzuur in cola
- Zuur-base titratie in nuclonschaaltje
- Zuurgehalte van melkproducten
Filmfragmenten
Lesvideo's youtube
Eigen lesvideo's
Oefeningen lesvideo's
- Geef de titratiecurve van 25,00 ml 0,10 mol/l zoutzuur dat getitreerd wordt met 0,10 mol/l NaOH-oplossing.
- Geef de titratiecurven van 25,00 ml 0,10 ml CH3COOH dat getitreerd wordt met 0,100 mol/l NaOH (Na+ + OH–)
- Bij de titratie van 25 mL HAc-oplossing wordt het equivalentiepunt bereikt na toevoegen van 30 mL NaOH-oplossing 0,110 mol/L. Bereken de concentratie van de azijnzuuroplossing
- Bij de titratie van 25 mL HAc-oplossing wordt het equivalentiepunt bereikt na toevoegen van 30 mL NaOH-oplossing 0,110 mol/L. Hoe groot is de pH tijdens de titratie na toevoegen van 15 mL NaOH 0,110 mol/L?
- Bij de titratie van 25 mL HAc-oplossing wordt het equivalentiepunt bereikt na toevoegen van 30 mL NaOH-oplossing 0,110 mol/L. Hoe groot is de pH als we 50 ml NaOH 0,110 mol/L hebben toegevoegd?
- In een erlenmeyer bevindt zich 25,0 mL HAc 0,1 mol/L. Uit een buret voegen we NaOH 0,1 mol/L toe. Bereken de pH na toevoegen van 10 mL uit de buret.
- In een erlenmeyer bevindt zich 25,0 mL HAc 0,1 mol/L. Uit een buret voegen we NaOH 0,1 mol/L toe. Bereken de pH na toevoegen van 25 mL uit de buret.
- In een erlenmeyer bevindt zich 25,0 mL HAc 0,1 mol/L. Uit een buret voegen we NaOH 0,1 mol/L toe. Bereken de pH na toevoegen van 30 mL uit de buret.
Titraties
- Doekle bepaalt de [H2Se] van een oplossing via een terugtitratie. Hierbij neemt hij 75,00 ml van de H2Se-oplossing en voegt hier een overmaat van 10,00 ml 0,500 mol/l NaOH-oplossing aan toe. Alle H2Se wordt dan omgezet tot Se2- volgens H2Se + 2 OH– –> Se2- + 2 H2O. Hij voegt dan een geschikte indicator toe en titreert de overgebleven OH- ionen met 0,103 mol/l zoutzuur. Hiervoor blijkt 14,34 ml nodig te zijn.
- Bereken [H2Se] van de oorspronkelijke oplossing
- Bereken het massa% H2Se van de oorspronkelijke oplossing. De dichtheid van de H2Se-oplossing bedraagt 1,03 kg/l
- Aziz bepaalt [OH–] van 20,0 ml natronloog door middel van titratie. Aan de natronloog voegt hij een geschikte indicator toe. Na toevoeging van 14,36 ml 0,104 mol/l zoutzuur slaat de kleur van de indicator om. De vergelijking van de reactie die tijdens de titratie optreedt luidt: H+ + OH– –> H2O. Bereken [OH–]
- Het massapercentage N in een mengsel van zouten.In een mengsel van zouten met een massa van 1,428 gram bevinden zich uitsluitend NH4+ ionen als positief ion. Aan negatieve ionen bevinden zich in het mengsel ionen zonder het element stikstof.Jelmer en Robert bepalen met massapercentage N van het mengsel via titratie.Ze lossen daartoe het mengsel op in 100,00 ml water. Ze pipetteren hiervan 10,00 ml en brengen dat over in een erlenmeyer.
Ze voegen een geschikte indicator toe en titreren met natronloog waarvan [OH–] = 0,032 mol/l. Er blijkt voor de titratie 15,42 ml nodig te zijn.Tijdens de titratie vindt de volgende reactie plaats: NH4+(aq) + OH– (aq) –> NH3(aq) + H2O(l)
- Je voert een titratie uit. Je gaat onderzoeken wat de concentratie zoutzuur in een onbekende oplossing is. Hiervoor verdun je de oplossing eerst 20 keer en doe je daarvan 10,0 ml in de erlenmeyer. Vervolgens ga je dit titreren met 0,215 mol/l natronloog. Je blijkt 7,15 ml natronloog nodig te hebben. Bereken de concentratie zoutzuur in mol/l
- 20 mL KOH 0,02 mol/L wordt getitreerd met 28,2 mL HNO3. Bereken de concentratie van deze
- Men lengt 10 mL geconcentreerd H2SO4 aan tot 1 L. 20 mL van deze oplossing wordt getitreerd met NaOH 0,2 mol/L. Het equivalentiepunt wordt bereikt na toevoegen van 36,2 mL. Bereken de concentratie van het geconcentreerde H2SO4.
Spellen
Quizzen
Animaties
Titraties
- Titratie sterk zuur en sterke base
- Zuur-basetitratie (cmp)
- Titratie zwak zuur met sterke base (cmp)
- Titraties
- Zuur-basetitratie met fft als indicator (cmp)
- ChemCollective: Titratie van NaOH met KHP
Titratiecurve
- Titratie van een sterk zuur met sterke base
- Titratie van een sterke base met een sterk zuur
- Titratie van een zwak zuur met een sterke base
- Titratie van een zwakke base met een sterk zuur
- Titratie van een sterk zuur met een zwakke base
- Titratie van een sterke base met een zwak zuur
- Titraties sterke base en zwakke zuren
- Titraties (installatietool)
- Titratietool
- Titratie zuur en base (soorten zuur/base en K-waarden in te stellen)
- Titratie zuur en base (soorten en K-waarden in te stellen)
- Titratie polyprotonische zuren
Ipad apps
Titratiecurven

Waterige zuur-base-evenwichten kunnen vanuit meerdere perspectieven worden bestudeerd hoe verschillen in chemische structuur de chemische reactiviteit kunnen veranderen. Vaak neemt slechts één vorm van een molecuul deel aan een reactie en de fractie van die vorm kan aanzienlijk veranderen met kleine veranderingen in de pH.
https://itunes.apple.com/be/app/titration-1.0/id1020960305?l=nl&mt=8
https://play.google.com/store/apps/details?id=com.nof.makanoh.simulasititrasiasambasa

Voer een titratie uit zo snel en zo nauwkeurig mogelijk
https://itunes.apple.com/nl/app/utitrate/id619147829?mt=8
https://play.google.com/store/apps/details?id=com.mt.lab.ana.ti.uTitrateGame

De app analyseert de kleurveranderingen die betrokken zijn bij een titratie
https://play.google.com/store/apps/details?id=com.color.Titration_ColorCam
Android apps
Titratiecurven

Voer een titratie uit zo snel en zo nauwkeurig mogelijk
https://play.google.com/store/apps/details?id=com.mt.lab.ana.ti.uTitrateGame

De app analyseert de kleurveranderingen die betrokken zijn bij een titratie
https://play.google.com/store/apps/details?id=com.color.Titration_ColorCam
De app analyseert de kleurveranderingen die gepaard gaan met een titratie, feedback voor het detecteren van een eindpunt.
https://play.google.com/store/apps/details?id=com.color.Titration_ColorCam&gl=BE

In deze app worden de titraties van sterke en zwakke zuren (basen) gesimuleerd en worden de titratiecurven gereconstrueerd met behulp van animaties.
https://play.google.com/store/apps/details?id=com.maxbeispiel.dggoe.titration&gl=BE
U kunt het type zuur, base of zout selecteren dat fungeerde als Titrant. Niet alleen één maar maximaal negen stoffen kunnen achtereenvolgens worden toegevoegd om als titrand te gebruiken.
https://play.google.com/store/apps/details?id=com.unitary.ujang.titrateman_v3&gl=BE
Rekenen bij titraties

App bruikbaar bij berekeningen bij titraties
https://play.google.com/store/apps/details?id=org.calistry.www.titrationcalculator&gl=BE
Inspiratie op het net
Titratie
- Wikiwijs : titratie Zuurgehalte in frisdrank
- Wikiwijs : titratie maagzuurtablet
- Wikiwijs
- Wikiwijs gebruik van glaswerk
- Wikiwijs voorbeeld berekening
- Wikiwijs titratie azijnzuur in azijnoplossing
- Wikiwijs online synthese methyloranje
- wikiwijs titratiecurven online
- wikiwijs powerpoint
- wetenschap titratiecurve zwak zuur met sterke base en excel
- wetenschap titratiecurve sterk zuur met sterke base en excel
- Klascement berekenen van een titratiecurve
- klascement labo titraties
- Klascement titraties door meten van geleidbaarheid labo
- Klascement zuur-basetitratie labo
- klascement concentratie bicarbonaat via zoutzuuroplossing labo
- klascement titratie sterk zuur met sterke base labo
- klascement titratie zwak zuur met sterke base labo
- klascement titratie azijnzuur in tafelazijn labo
- klascement pH verloop van een titratie labo
- mlo chemie titraties
- internetboek titraties
- internetboek rekenen met titraties