Ipadles Bouw van het atoom
Bouw van een atoom
Een atoom bestaat uit protonen, elektronen en neutronen. De protonen en neutronen bevinden zich in de kern van het atoom de atoomkern. De elektronen zitten in de elektronenwolk op een grote afstand van de kern af. Dit wordt het atoommodel van Rutherford genoemd. Een atoom is ongeveer 0,0000000001 meter groot dat is 10 tot de macht -10. Dat is zo ontzettend klein dat een atoom met geen enkel hulpmiddel gezien kan worden.
Om een idee te hebben over de grootte van de deeltjes. Plaats bij de verschillende afmetingen een voorbeeld.
Open de app, scroll over de onderste tijdlijn en neem een printscreen van de voorstelling of vul de correcte grootte in.

Modellen voor atoombouw
Wanneer atomen met vele miljarden bij elkaar zijn worden ze zichtbaar. Er zijn ongeveer 100 verschillende soorten atomen op aarde.
Zoals besproken tijdens de lessen is er veel onderzoek verricht naar hoe een atoom eruit ziet. Er zijn een groot aantal wetenschappers die elk hun steentje hebben bijgedragen. Met volgende apps kan je achterhalen welke bijdrage iedere wetenschapper heeft geleverd.

Protonen, neutronen, elektronen
Volgens de ontdekkingen van Rutherford bestaat een atoom uit een kleine centrale positieve kern (positief door de protonen) met daarrond een wolk van negatieve ladingen, de elektronen.
Volgens het atoommodel van Bohr bestaat een elektronenwolk uit 7 concentrische schillen ronde de kern.
Het atoomnummer (Z) geeft het aantal protonen weer die in de kern aanwezig zijn. Voor een neutraal atoom komt dit overeen met het aantal elektronen rond de kern.
Wanneer we dit schematisch weergeven wordt dit steeds linksonderaan vermeld. Het element koolstof heeft 6 protonen in de kern en bijgevolg ook 6 elektronen op de schillen.
Oefening op het tekenen van elektronenconfiguratie volgens het model van Bohr:
Open de app/selecteer play/ga naar level 1/a little harder : electronic structure only/ met je vinger kan je de elektronen plaatsen op de schillen
- Afspraken voor het plaatsen van de elektronen:
- De eerst 2 elektronen worden steeds gepaard weergegeven
- Elektron 3, 4 en 5 op eenzelfde schil worden steeds ongepaard weergegeven
- Nadien worden elektron 6,7 en 8 gepaard met elektron 3, 4 en 5.
- Neem een printscreen van de verschillende elementen, je kan ook je antwoord controleren door op check te drukken

We hebben net een oefening gemaakt op de aanwezige protonen in de kern en de elektronen errond. Dat een kern van positieve deeltjes niet uit elkaar spat door onderlinge afstotingskrachten wordt verklaard door de aanwezigheid van neutrale deeltjes tussen de protonen. Deze neutrale deeltjes noemt men neutronen. In het model van Rutherford zijn de protonen en neutronen nog een theoretisch begrip.
In de eerste opdracht hebben we de diameter van een gemiddeld atoom onderzocht en vastgesteld dat deze ongeveer honderdduizend maal groter is dan de diameter van de atoomkern. Uit verder onderzoek is gebleken dat elke atoomkern nagenoeg de ganse massa van een atoom bevat. De som van het aantal protonen en neutronen in de atoomkern wordt weergegeven in het massagetal (A). Dit wordt in de schematische voorstelling linksboven geplaatst.

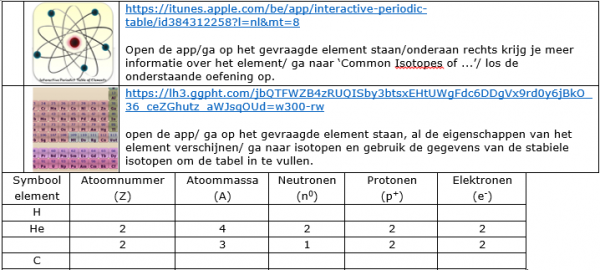
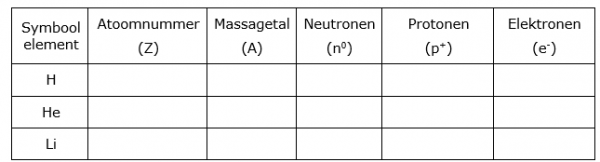
Oefening: Beschrijf de atoombouw van de gevraagde elementen:
Gebruik voor het oplossen van deze oefening de apps die beschreven zijn onder 1)
Spel: Atoomnummer
Gebruik voor dit spel de apps die beschreven zijn onder 2)
Plak hieronder een printscreen van je score
Spel: atoommassa
Gebruik voor dit spel de app die beschreven is onder 3)
Plak hieronder een printscreen van je score
Isotopen
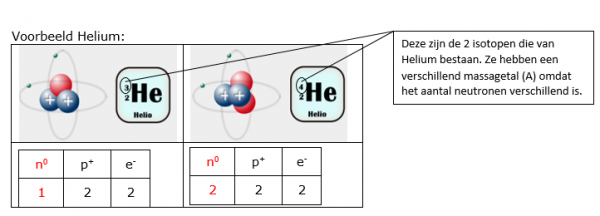
Van de meeste atoomsoorten komen in de natuur atomen voor met een verschillend aantal neutronen. Het aantal protonen en elektronen is wel hetzelfde. Dit zijn isotopen.
Omdat de eigenschappen van een atoomsoort voornamelijk bepaald wordt door het atoomnummer (Z), hebben isotopen chemisch ongeveer dezelfde eigenschappen.
Voorbeeld Helium: