H5 – Film: toelatingsexamen
Bron: Examenvragen – Toelatingsexamen arts & tandarts (toelatingsexamenartstandarts.be)
Bron: Ijkingsproeven HOME – IJkingstoets.be
- Een HNO3-oplossing reageert met 0,100 mol van een metaal waarvan het symbool voorgesteld wordt door M. Na de reactie blijft er 0,040 mol van het metaal M over en is er 0,030 mol van een oxide van stikstof gevormd.Wat kan de reactievergelijking zijn?
- <A> 3 M (s) + 8 HNO3 (aq) → 3 M(NO3)2(aq) + 2 NO(g) + 4 H2O(l)
- <B> M (s) + 4 HNO3 (aq) → M(NO3)2 (aq) + 2 NO2 (g) + 2 H2O (l)
- <C> M (s) + 2 HNO3 (aq) → MO (s) + N2O4 (g) + H2O (l)
- <D> 2 M (s) + 2 HNO3 (aq) → 2 MO (s) + N2O3 (g) + H2O (l)
2 CxH6 (g) + 7 O2 (g) –> y CO2 (g) + 6 H2O (g)
3. Wat is de waarde van de ontbrekende coëfficiënten b en c in onderstaande halfreactie?
a ClO4– + b H+ + c e- –> 1 Cl– + d H2O
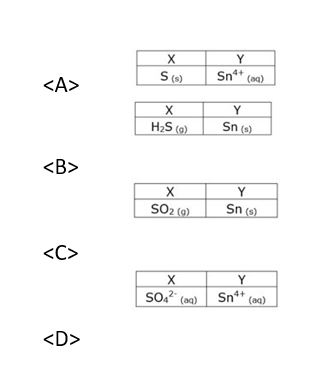
.. SO3 2- + .. Sn2+ + .. H+ –> .. X + .. Y + .. H2 O ?
5. Gegeven is volgende niet-uitgebalanceerde reactievergelijking waarin X de formule van een verbinding voorstelt:
… CS2 + … X + … KOH → … K2SO4 + … K2CO3 + … KCl + … H2O
De hoeveelheden (in mol) van de betrokken stoffen bij het begin en op het einde van de reactie worden in tabelvorm weergegeven.
Wat is de formule voorgesteld door X?







