H2 – Film: eigen oefeningen
1.Wat kan afgeleid worden uit de volgende symbolische voorstellingen van de elementen:
4.Vul voor de stoffen de volgende tabel in:
![]()
- -aantal hoofdschillen
- -totaal aantal subniveaus
- -totaal aantal magnetische niveaus
- -totaal aantal ongepaarde elektronen
- -groepsnummer in het P.S.E.
- -atoomnummer
- -s-, p-, d- of f-blokelement
- -mogelijk positief oxydatiegetal
- -mogelijk negatief oxydatiegetal
5.Vervolledig de onderstaande tabel
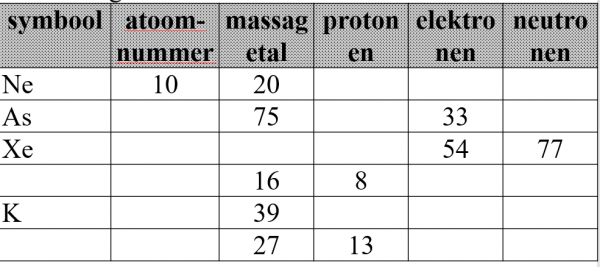
6.Hoeveel elektronen kunnen in een atoom maximaal voorkomen:
- -in de 4de hoofdschil
- -in het 4de subniveau
- -in ongepaarde toestand
- -met een ongepaarde spin voor een element uit de 2de periode in de grondtoestand
7.Geef het atoomnummer van het element waarbij als eerste een elektron voorkomt:
- -de 3de hoofdschil
- -de 4de subschil
- -het 3p-niveau
- -het 5d-niveau
- -het 5p-niveau
- -een edelgasatoom met Z> 36
8.Noem het element met het kleinst mogelijke atoomnummer met:
- -een halfvol p-subniveau
- -een vol 3 s-niveau
- -acht valentie-elektronen
- -metaalkarakter waarbij Z> 7
- -dubbel zoveel orbitalen als hoofdschillen
- -driemaal zoveel orbitalen als hoofdschillen
- -dubbel zoveel orbitalen als subniveaus
9.Hoeveel magnetische subniveaus komen in de grondtoestand maximaal voor in:
- -de tweede hoofdschil
- -een d-subniveau
- -een 15P-atoom
- -een edelgas met 54 protonen
- -een atoom van een element uit de 2 de periode
- -het derde edelgas
- -een 23V-atoom met 3 ongepaarde elektronen
- -een 8 O-atoom
- -een 37 Rb+ ion
11.Zoek op in het periodiek systeem:
- Een atoom met 3 gevulde en 3 halfgevulde p-orbitalen
- Een atoom met een volledige reeks halfgevulde 4f-orbitalen
- Een atoom waarvan 3 van de 5 3d-orbitalen volledig zijn gevuld.






