Zuurpatronen
Filmfragment
1.Onderzoeksvraag
Hoe kunnen we in oplossing bepaalde kleurpatronen vormen?
2.Voorbereiding
- Petrischaal
- Roerstaaf
- Na2CO3 oplossing 5%
- NaHSO4 oplossing 5%
- Thymol blauw
- Water
3.Uitvoeren
a.Werkwijze
- Druppel enkele druppels Na2CO3 in een petrischaal.
- Doe de petrischaal halfvol met water.
- Meng de oplossing met enkele druppels Thymol blauw.
- Roer goed.
- Druppel enkele druppels NaHSO4 in de oplossing.
- Roer goed.
- Druppel enkele druppels Na2CO3 in de oplossing.
- Roer goed en neem waar.
b.Waarneming (+ foto’s)
Na het samenvoegen kleurt de oplossing: blauw, groen en weer blauw.

4.Reflecteren
Thymol blauw verandert van kleur afhankelijk van het medium waarin het zich bevindt. Het is een pH-indicator. In een basisch medium wordt het blauw; in een zuur medium wordt het rood, in een bijna neutraal medium wordt het geel. Blauw, rood en geel worden als primaire kleuren beschouwd omdat het combineren ervan vele extra variaties kan opleveren: blauw + geel = groen, geel + rood = oranje, rood + blauw = violet. Je kunt deze combinaties ook in je Petrischaal maken! Roer de inhoud voorzichtig met een houten stok. De zuurgraad van een oplossing hangt af van de verhouding van positief geladen waterstofionen H + (protonen) tot negatief geladen hydroxide-ionen OH–. Zo vormt natriumcarbonaat, dat we als eerste aan de petrischaal toevoegden, een basisch medium.
Zijn interactie met water produceert een grote hoeveelheid hydroxide-ionen OH–: Na2CO3 + H2O → 2Na+ + HCO3– + OH–
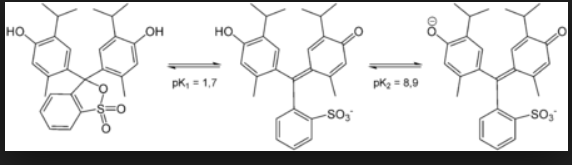
Deze overvloed aan hydroxide-ionen maakt de oplossing in de petrischaal basisch. Thymolblauw wordt blauw als het aan de oplossing wordt toegevoegd. Natriumwaterstofsulfaat, in tegenstelling tot natriumcarbonaat, lost op in water en maakt protonen H+ vrij: NaHSO4 → Na+ + H+ + SO42-
De oplossing wordt zuur zodra natriumwaterstofsulfaat aan de petrischaal wordt toegevoegd. Naarmate we reagentia op verschillende plaatsen in de petrischaal toevoegen, verandert de zuurgraad van de oplossing ongelijk. Op sommige plaatsen domineren H + -ionen, terwijl OH– heerst in een ander gebied. Hierdoor geeft de thymol blauwe oplossing een verscheidenheid aan kleuren. Wanneer gemengd, wordt de zuurgraad van het medium uniform over de oplossing, zodat de thymol blauwe kleur ook uniform wordt.
5.Onderwerpen
- pH indicator
6.Bron






