Wijnsoorten maken
1.Onderzoeksvraag
Hoe kun je verschillende wijnsoorten maken?
2.Voorbereiding
a.Begrippen als achtergrond voor experiment
- Indicator: een stof waarmee men kan aantonen dat een bepaalde andere stof aanwezig is. Dit kan gebeuren door bijvoorbeeld verkleuring.
b.Materiaal + stoffen
- 2 witte wijnglazen
- 3 rode wijn glazen
- 1 shot glas
- 1 champagne glas
- Pipetten
- Theelepel
- lucifers
- Spatels
- Natriumhydroxide oplossing (1mol/L)
- Zwavelzuur (40%)
- Ijzer(III)chloride
- Ammoniumthiocyanaat
- Fenolftaleine-oplossing
- Citroenzuur
- Heptaan
- Kaliumhexacyanoferraat (II) K4[Fe(CN)6]
- Natriumwaterstofcarbonaat
- Gedestilleerd water
c.Opstelling (foto)

d.Etiketten

3.Uitvoeren
a.Werkwijze
Glas 1 “tafelwijn, white”:
Doe in het eerste wijnglas ongeveer 1 ml Fenolftaleïne oplossing.
Glas 2 “rosé”:
Voeg ongeveer 10 druppels natriumhydroxideoplossing in het tweede wijnglas.
Glas 3 “Kabinet white”:
Doe in het derde glas een kleine spatelpunt ijzer (III) chloride en ongeveer 20 druppels zwavelzuur.
Glas 4 “champagne”:
1 theelepel natriumbicarbonaat en 1 theelepel citroenzuur worden toegevoegd aan het champagneglas.
Glas 5 “red”:
Voeg een kleine spatelpunt ammoniumthiocyanaat toe in het rode wijnglas
Glas 6 “Pinot Noir”:
Een kleine spatelpunt kaliumhexacyanoferraat (II) wordt toegevoegd aan het glas.
Glas 7 “Brandy”:
1 tot max. 2 ml heptaan voeg je toe in de shotglaasjes
Zet de zeven glazen in volgorde naast mekaar. Het eerste bekerglas vul je tot ¼ met warm water. Daarna giet je steeds de volledige inhoud van het glas over in het volgende bekerglas.
Wanneer je de inhoud van glas 6 overgiet in glas 7, steek je de bovenkant van de vloeistof van glas 7 aan met een lucifer. Neem waar.
Giet daarna gewoon de inhoud terug over in het laatste glas, glas 7. Dit glas zet u in een grote schaal of op een dienblad!
b.Waarneming (+ foto’s)
Tijdens het gieten van glas 1 (“tafelwijn, white”) in glas 2 (‘rosé’), wordt de kleurloze vloeistof rosé of roze.
Bij het gieten van glas 2 in glas 3 (“witte wijn”), wordt het mengsel lichtgeel.
In glas 4 (“champagne”) zal de vloeistof krachtig opschuimen zonder te veranderen van de kleur.
In glas 5 (‘rood’), kleurt de vloeistof rood.
In glas 6 (“Pinot Noir”) kleur de vloeistof blauw tot donkerblauw.
Bij het gieten in glas 7 (“Brandy”), zal de kleur niet veranderen, maar een geelachtige vlam wordt zichtbaar na het aansteken.

4.Reflecteren
Fenolftaleïne
Fenolftaleïne (3,3-bis (4-hydroxyfenyl) ftalide) is een wit kristallijn poeder, onoplosbaar in water, en slecht oplosbaar in alcohol of base. In het basische bereik (pH 8,4-10,0) weegt het zwaarder dan het chinoïde structuur (zie figuur 1). Dit gedeprotoneerde vorm van de indicator heeft een gedelokaliseerd pi-elektron-systeem, waarbij de Fenolftaleïenoplossing roze zal kleuren.
In zuur tot neutrale pH is fenolftaleïne voornamelijk aanwezig in de vorm van ftalide. Echter, een delocalisatie van pi-elektronen over de drie benzeenringen is niet meer mogelijk hier. Dit systeem is te klein om een kleur verschijning op een excitatie van elektronen vertonen. De kleur van de indicator van kleurloos tot roze kan door toevoeging van zuur.
Fenolftaleïne wordt veel gebruikt als zuur-base-indicator in de titratie van sterke basen. De roze kleur is nog steeds op een verdunning van 1: 1000000 herkenbaar.
Ijzer (III)thiocyanaat
Door toevoeging van een oplossing van ammoniumchloride met een ijzer (III) chloride oplossing, resulteert dit in de vorming van een bloedrood gekleurd ijzer thiocyanaat complex:
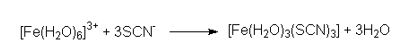
Pruisisch-blauw
Onder de complexe verbindingen van ijzer, vallen de cyano complexen ( “hexacyanoferraten”) onder de meest stabiele. De kaliumzouten worden onder “Yellow ferrocyanide” K4 [Fe (CN) 6] of “Red ferrocyanide” K3 [Fe (CN) 6] bekend. Ijzer (II) complex ([Fe (CN) 6] 4-) is thermodynamisch en kinetisch stabieler dan ijzer (III) complex ([Fe (CN) 6] 3-). Ijzer (III) complex kan vrij functioneren als oxidator:
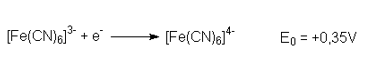
Wanneer we een oplossing van gele bloedloogzout zout met ijzer (III) chloride of een oplossing van rode bloedloogzout zout met ijzer (II) chloride samenvoegen, is het resultaat in beide gevallen bij een molaire verhouding van 1: 1 dezelfde colloid opgelost “oplosbaar Prussian Blue” :
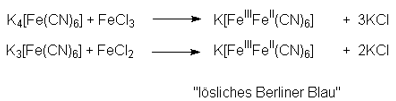
Bij het toevoegen van teveel aan ijzer (III) – of ijzer (II)-ionen [Fe (CN)6]4- of [Fe(CN)6] 3- ontstaan blauw neerslagen als “onoplosbaar Pruisisch blauw” of ” onoplosbaar Turnbull Blue ” die we onderling onderscheiden. Echter, zijn ze thans chemisch identiek:
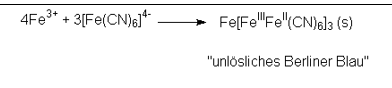
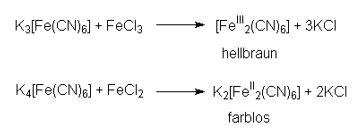
De reactie van ijzer (III) chloride met rode kaliumferrocyanide en ijzer(II)chloride met kaliumferrocyanide, is ongeacht de oorzaak kleurloze of slechts zwak gekleurde oplossingen:
Heptaan
Heptaan is een keten-achtige koolwaterstof door de stof groep van alkanen met moleculaire formule C7H16. Onder heptaan wordt gewoonlijk verstaan de onvertakte n-heptaan, die negen isomeren bevatten. N-heptaan is onoplosbaar in water en licht ontvlambaar – vlampunt -4 ° C, de ontstekingstemperatuur bij 285 ° C. Tussen een lucht volumefractie 1,1-6,7 procent, vormt het een explosief mengsel. In een oplossing met heptaan en water stijgt deze stof als gevolg van de lagere dichtheid dan water (water dichtheid: 0,997 g / cm3 bij 25 ° C; dichtheid van heptaan: 0,681 g / cm3).
Natriumwaterstofcarbonaat
Natriumbicarbonaat, ook wel bekend als Soda, is een fijn wit poeder en ontleedt boven een temperatuur van ongeveer 65 ° C in water, kooldioxide en natriumcarbonaat. Boven 300 ° C is de omzetting voltooid. Zuren worden geneutraliseerd door NaHCO3 evolutie van kooldioxide:
NaHCO3 + HCl –> NaCl + CO2 + H2O
In het experiment van natriumbicarbonaat en citroenzuur reageert dit alleen in de aanwezigheid van water, op de zojuist beschreven wijze met elkaar.
Glas 1 “tafelwijn, white”:
Fenolftaleïne is een zuur-base indicator in water (pH 7) is kleurloos.
Glas 2 “rose”: Door toevoeging van de natriumhydroxideoplossing, wordt het watermengsel alkalisch, waarbij de kleur van fenolftaleïne verandert naar roze.
Glas 3 “Kabinet white”:
Het zwavelzuur maakt de vloeistof zuurder, waardoor de indicator weer kleurloos kleurt. De toegevoegde ijzer (III)chloride veroorzaakt wel de lichte vergeling.
Glas 4 “champagne”: natriumbicarbonaat en citroenzuur reageren slechts in aanwezigheid van water, en maken vervolgens kooldioxide gas vrij – dit is vergelijkbaar met een bruistablet dat u in water toevoegt.
Glas 5 “Rood”: de Fe3 + ionen reageren met thiocyanaat een roodgekleurd ijzer (III) complex thiocyanaat.
Glas 6 “Pinot noir”: In concurrentie met thiocyanaat (SCN–) treden hexacyanoferraat (III) – ionen ([Fe(CN)6]4-) op, die reageren met de Fe3 + ionen en vormen het complex “Pruisisch blauw”.
Glas 7 “Brandy”: Door de lagere dichtheid in vergelijking met water, kan de heptaan stijgen binnen de oplossing en dus gemakkelijk ontbranden.
Reactie C7H16 + 11 O2 –> 7 CO2 + 8 H2O






