Vlamproeven met metalen draad
1.Onderzoeksvraag
Welke vlamkleuren ontstaan er bij verschillende stoffen?
2.Voorbereiding
Materiaal en stoffen:
- Materiaal:
- Gekrulde ijzerdraad in een kurk (entoog)
- Bekerglas gevuld met water
- Bunsenbrander
- Petrischaal
- Spatellepel
- Lucifers
- Stoffen:
- NaCl
- CuCl2
- Sr(NO3)2
Opstelling
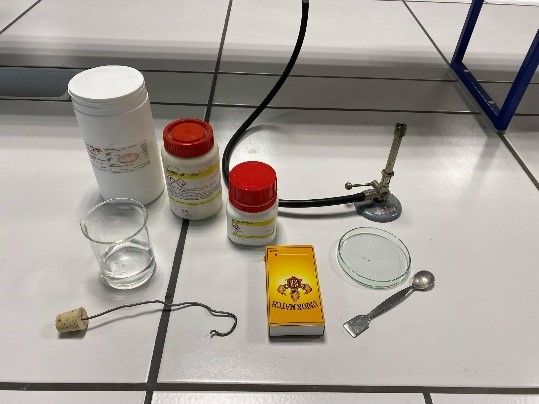
3.Uitvoeren
a.Werkwijze
- Bevestig een ijzerdraad aan een krul.
- Krul het uiteinde in de vorm van een lus.
- Neem van elk zout een schepje en leg het in een petrischaal.
- Verduister het lokaal.
- Bevochtig de lus door die even in een maatbeker met water te stoppen.
- Stop de lus van de ijzerdraad in het te onderzoeken zout. (Enkele zoutkristallen blijven aan de lus zitten.)
- Breng de zoutkristallen in de vlam van de bunsenbrander.
b.Waarneming (+ foto’s)

4.Reflecteren
Natriumchloride geeft een oranje vlam. Koperdichloride geeft een groen/blauwe vlam. Strontiumnitraat geeft een rode vlam.
Door een atoom te verhitten krijgen de elektronen meer energie. Ze gaan naar een hoger gelegen energieniveau of schil. De elektronen keren daarna terug naar de laagst mogelijke schil. Ze geven daarbij de extra energie af in de vorm van straling. De hoeveelheid afgegeven energie bepaalt de aard van de straling. Dit verklaart waarom een atoomsoort bij verhitting een welbepaalde kleur heeft.






