Hoofdstuk 8 – Experimenten
1. Geleiding

- Info:Wat is de invloed van de mens en water wanneer men verschillende metalen in serie plaatsen? Metalen hebben enigszins de neiging elektronen af te staan. Logisch: anders bestonden er geen ionen van. Maar niet alle metalen doen dat even graag. Onedele metalen doen dat eerder. Aluminium doet dat dus liever dan koper, en “duwt” daarom elektronen naar het koper, althans als er geleiding is. Op je handen zit altijd wel wat zweet dat via ionen de geleiding verzorgt. Zo lopen elektronen van Al naar Cu. Cu is de pluspool en Al is de minpool.
- Moeilijkheid: eenvoudig
- Chemische stoffen: koperen voorwerp (30 cm2) – aluminium voorwerp (30 cm2) – zinken voorwerp (30 cm2) – 1 koolstof staal – keukenzout – ammoniumchloride (salmiak)
- Thema: elektrische eigenschappen
- Tijd: 20 min
- Begrippen: geleiding metalen
1.2. Doormeetapparaat deel1 – deel2

1.3. Geleidbaarheid beïnvloeden door temperatuur

- Info:Hoe kunnen we de geleidbaarheid van ammoniumchloride beïnvloeden door temperatuurdaling? Zuiver water is niet geleidend. Indien hierin een zout zoals salmiak is opgelost gaan de vrije ionen geleiding veroorzaken.Wordt het water bevroren dan gaan de ionen niet meer vrij kunnen bewegen en vermindert de geleiding.
- Moeilijkheid: eenvoudig
- Chemische stoffen: ammoniumchloride (10g) – Zout – Ijs
- Thema: elektrische eigenschappen
- Tijd: 20 min
- Begrippen: invloed temperatuur op geleidbaarheid
1.4. Geleidbaarheid bepalen van water, zuren en hydroxiden in een blisterverpakking

- Info: Hoe verschilt de geleidbaarheid van water, zuren en basische oplossingen? We stellen vast dat zowel HCl als NaOH de elektrische stroom goed geleiden. Opgeloste zuren en basen geleiden de elektrische stroom door de aanwezigheid van ionen. (resp. door ionisatie en dissociatie). Kraantjeswater bevat ook een kleine hoeveelheid ionen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Water – HCl oplossing 1 mol/l – NaOH oplossing 0,1 mol/l
- Thema: elektrische eigenschappen
- Tijd: 20 min
- Begrippen: elektrische geleidbaarheid zuren en basen
1.5. Vloeibare Geleiders

- Info: Hoe kunnen we een lijntje actieve kool geleidend maken? Het natriumsilicaat zorgt voor een stroopachtige structuur, soms wordt het ook wel vloeibaar glas genoemd. Het gaat geen reactie aan met het water maar zorgt meer voor een indikkend effect Grafiet is een goede elektrische geleider en het vloeibare glas “lijmt” zijn deeltjes aan elkaar om een continu circuit te vormen. Elektronen beginnen van het ene deeltje grafiet naar de andere. Wanneer we het circuit sluiten, stroomt er stroom door het doorstroommetertje waardoor de lichtjes schijnen. Deze “draden” kunnen op elk oppervlak worden aangebracht in de vorm van een tekening. Maar de lijn moet ononderbroken zijn, anders sluit het circuit niet en stroomt er geen stroom doorheen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Grafiet (actieve kool) – Natriumsilicaat
- Thema: elektrische eigenschappen
- Tijd: 10 min
- Begrippen: elektrische geleidbaarheid niet-metalen
1.6. Geleidbaarheid

- Info: Welke stoffen zijn elektrisch geleidbaar? Elektrische geleiding is het transport van elektrische ladingen door geladen deeltjes. In de metalen zijn die geladen deeltjes de elektronen. Doordat metalen deze geladen deeltjes in grote hoeveelheden bevatten, zijn het erg goede geleiders.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Suiker – Cyclohexaan – Ethanol – Koper – Grafiet – Gedestilleerd water – Zout
- Thema: elektrische eigenschappen
- Tijd: 10 min
- Begrippen: elektrische geleidbaarheid zuivere stoffen
2. Oplosbaarheid
2.1. Aantonen van de oplosbaarheid van gassen

- Info:Zuurstofgas lost minder goed op in water dan koolstofdioxidegas. Dit kan je vaststellen doordat de temperatuur van het water in de erlenmeyer met CO2 hoger is dan de temperatuur van het water met O2. Hoe hoger de temperatuur, hoe beter vaste stoffen oplossen, maar hoe slechter gassen oplossen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: 2 ballonnen – azijn en bakpoeder voor de productie van koolstofdioxide
- Thema: Eigenschappen van chemische stoffen
- Tijd: 20 min
- Begrippen: oplosbaarheid van gassen
2.2. De wijntoren

- Info:Hoe kunnen we verschil in dichtheid aantonen met twee stoffen die oplosbaar zijn in elkaar? Alcoholmoleculen kunnen twee waterstofbruggen vormen, water kan 4 waterstofbruggen vormen. Hierdoor bezitten methanol; ethanol en isopropanol een kleinere cohesiekracht onderling dan met water. Bij het experiment wordt de alcoholische oplossing over een doek naar het glas overgebracht. Door capillariteit dringt de oplossing in het glas. Vermits de alcohol een kleinere dichtheid heeft, stijgt de oplossing in het glas en mengt zich met het bovenste deel.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Water (300ml) – Kleurstof (universele indicatoroplossing) – ethanol
- Thema: Eigenschappen van chemische stoffen
- Tijd: 20 min
- Begrippen: massadichtheid oplossingen
2.3. Oplosbaarheid van koolstofdioxide in water aantonen bij verschillende temperaturen
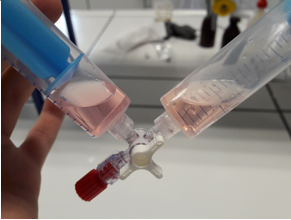
- Info: Welke reactie treedt op en wat kunnen we waarnemen wanneer we CO2 laten oplossen in water onder gewone druk en onder onderdruk in water? CO2 lost beter op in water onder gewone druk dan onder onderdruk. Bij de spuit onder onderdruk zie je belletjes ontstaan in de vloeistof zelf. Deze belletjes zijn het opgeloste gas (CO2) dat weer uit die oplossing komt.
- Moeilijkheid: eenvoudig
- Chemische stoffen: bakpoeder (NaHCO3) – azijn (CH3COOH) – universele indicator
- Thema: Eigenschappen van chemische stoffen
- Tijd: 20 min
- Begrippen: oplosbaarheid gassen – invloed temperatuur op de oplosbaarheid
2.4. Reactie van koolstofdioxide en water
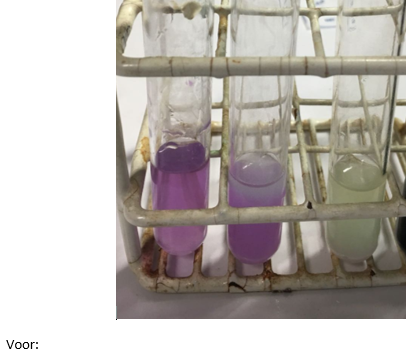
- Info: Welke veranderingen gebeuren er als je koolstofdioxide en kalkwater mengt? Hoe beïnvloedt de hoeveelheid koolstofdioxide de reactie? Controle met indicator
- Moeilijkheid: eenvoudig
- Chemische stoffen: Universeelindicator – Kalkwater – Azijn – Bakpoeder
- Thema: Eigenschappen van chemische stoffen – neutralisatiereactie
- Tijd: 20 min
- Begrippen: oplosbaarheid gassen – invloed temperatuur op de oplosbaarheid – zuur base indicator
2.5. Salz bringt mineralwasser zum sprudeln

- Info: Hoe kunnen we aantonen dat er in bruiswater dat lang openstaat nog steeds een gas aanwezig is? Het opgeloste koolstofdioxide is apolair. Het lost toch op in water omdat het ingesloten wordt. Het gehydrateerde gas wordt vrijgezet bij concurrentie van toegevoegde stoffen zoals keukenzout. De van der Waalskrachten zijn zwakker dan de iondipoolkrachten tussen zoutionen en waterdipolen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Keukenzout (5g) – Demi water (100ml) – bruiswater
- Thema: chemische reacties – anorganische stoffen – eigenschappen van stoffen
- Tijd: 20 min
- Begrippen: zouten – kristallisatie – aantonen van koolstofdioxide – oplosbaarheid

- Info: Hoe kunnen we 2 stoffen die niet reageren toch laten reageren? Breng in de proefbuis een spatel vast Na2S en een spatel vast SbCl3. Doe de waarneming Breng hierin 10 ml water door het water te spuiten op het mengsel. Doe de waarneming.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Demi water (10ml) – Natriumsulfide (5g) – Antimoonchloride (5g)
- Thema: chemische reacties – anorganische stoffen – eigenschappen van stoffen
- Tijd: 20 min
- Begrippen: zouten – oplosbaarheid
3. Polariteit
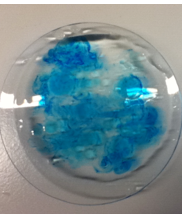
- Info: Leg onder een overhead een petrischaal die half gevuld is met water en projecteer. Los nu in 20 ml 1-heptanol wat kristalviolet op. Met een pipet wordt nu een druppel van het kristalviolet-heptanol mengsel gebracht. De druppel verdeelt zich over de waterige oplossing.
- Moeilijkheid: eenvoudig
- Chemische stoffen: heptaan-1-ol – kristalviolet
- Thema: chemische reacties – anorganische stoffen – eigenschappen van stoffen
- Tijd: 20 min
- Begrippen: osmose – diffusie – redoxreactie – microschaal – pulserende werking – oplosbaarheid
3.2. Buig het sterkst de waterstraal

- Info: Waterstraal afbuigen met geladen staven (plastiek – glas)
- Moeilijkheid: eenvoudig
- Chemische stoffen: geen
- Thema: bouw van atomen – eigenschappen van chemische stoffen
- Tijd: 5 min
- Begrippen: atoommodel van Thomson – elektrostatica – polariteit
3.3. Chemische amoebe in een petrischaal

- Info: Wat zal er gebeuren als men cyclohexanol toevoegt aan een oplossing van kaliumdichromaat en zwavelzuur?De pulserende veranderingen van grootte en vorm van de deeltjes ontstaat door de gedeeltelijke oxidatie van cyclohexanol door het kaliumdichromaat in zuur milieu tot cyclohexanon. De druppels veranderen in vorm door de verandering van oppervlaktespanning door wisselende verhouding van cyclohexanol en cyclohexanon.
- Moeilijkheid: gemiddeld
- Chemische stoffen: Kaliumdichromaat – Zwavelzuur – Cyclohexanol
- Thema: stofeigenschappen – eigenschappen van stoffen
- Tijd: 15 min
- Begrippen: osmose – diffusie – redoxreactie – microschaal – pulserende werking – polariteit
3.4. Droog onder water

- Info: Hoe kunnen we door de natuur te gebruiken, droog blijven onder water? Lycopodium is het zaad van wolfsklauw dat heel fijn is vermalen. Het is zeer sterk hydrofoob en vormt een dun waterafstotend laagje rond je vinger.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Water – Lycopodium
- Thema: stofeigenschappen – eigenschappen van stoffen
- Tijd:5 min
- Begrippen: polariteit – polaire en apolaire stoffen
3.5. Het hangende water

- Info: Hoe sterk worden waterdeeltjes onderling aangetrokken? Waarom is dit zo? Onderling heersen er krachten tussen de waterstofdeeltjes. Krachten tussen gelijkaardige deeltjes, noemen we cohesiekrachten. In dit geval wordt de onderlinge aantrekking veroorzaakt door de vorming van waterstofbruggen. Dit zijn zwakkere verbindingen tussen een H-atoom en een O-atoom van een ander molecule.Dankzij deze onderlinge krachten, vallen de waterdeeltjes niet doorheen de gaatjes van het gaas.
- Moeilijkheid: eenvoudig
- Chemische stoffen: stukje gaas – water
- Thema: stofeigenschappen – eigenschappen van stoffen
- Tijd: 15 min
- Begrippen: polariteit – polaire stoffen – waterstofbrugkrachten
3.6. Het magische zand

- Info: Hoe zorgen we ervoor dat zand droogt blijft in water? Het zand wordt gecoat met een zeer hydrofobe stof. Dit houdt in dat de waterdeeltjes zich niet kunnen vermengen met het zand omdat het zand als het ware samenklontert in het water. Door dit extreem apolair gedrag kunnen we het zand dus droog uit het water scheppen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: gekleurd zand – biocoating hout en steen of waterafstotende spray voor schoenen – water
- Thema: stofeigenschappen – eigenschappen van stoffen
- Tijd: 15 min
- Begrippen: polariteit – polaire stoffen
3.7. Het schenden van briefgeheim

- Info: Hoe kunnen we een brief lezen in een gesloten envelop? De tekst van een brief kan zichtbaar worden gemaakt als de envelop wordt bevochtigd met ethanol. Papier is polair en neemt ethanol op, daardoor wordt het papier enigszins doorzichtig. De inkt schijnt vervolgens door de envelop heen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: ethanol – potlood
- Thema: stofeigenschappen – eigenschappen van stoffen
- Tijd: 15 min
- Begrippen: polariteit – polaire stoffen – waterstofbrugkrachten
3.8. Salz bringt Mineralwasser zum Sprudeln

- Info: Hoe kunnen we aantonen dat er in bruiswater dat lang openstaat nog steeds een gas aanwezig is? Het opgeloste koolstofdioxide is apolair. Het lost toch op in water omdat het ingesloten wordt. Het gehydrateerde gas wordt vrijgezet bij concurrentie van toegevoegde stoffen zoals keukenzout. De van der Waalskrachten zijn zwakker dan de iondipoolkrachten tussen zoutionen en waterdipolen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Keukenzout (5g) – Demi water (100ml) – bruiswater
- Thema: chemische reacties – anorganische stoffen – eigenschappen van stoffen
- Tijd: 20 min
- Begrippen: zouten – kristallisatie – aantonen van koolstofdioxide – oplosbaarheid – polariteit

- Info:Door het volume en de oppervlakte te meten van een laagje oliezuur dat op water drijft, kun je een schatting maken van de lengte van een oliezuurmolecuul. Een oliezuurmolecuul is langwerpig, waarbij één kant in het water steekt.
- Moeilijkheid: gemiddeld
- Chemische stoffen:oliezuur – diëthylether
- Thema: moleculemodellen – grootte van moleculen – eigenschappen van stoffen
- Tijd: 30 min
- Begrippen:moleculen – moleculemodellen – polariteit
3.10. Troebel komt en gaat met ouzo

- Info: Hoe kan je een emulsie omzetten naar een oplossing? Alcohol is minder polair dan water waardoor de anijs opgelost kan worden in de drank. Daardoor is de oplossing alcohol (veel alcohol )-anijs zeer helder. Door toevoeging van een overmaat aan water (die een grotere polariteit heeft) kan het anijs niet meer oplossen en hierdoor wordt het uitzicht troebel.Bij toevoeging van een detergent kunnen de vetstoffen/anijs opnieuw “oplossen” dankzij de vorming van micellen rond de vetdruppels/anijs.
- Moeilijkheid: gemiddeld
- Chemische stoffen: ouzo/raki/anijs, – afwasmiddel/detergent
- Thema: moleculemodellen – grootte van moleculen – eigenschappen van stoffen – stofeigenschappen – mengsels
- Tijd: 30 min
- Begrippen:moleculen – moleculemodellen – polariteit – emulsies
3.11. Vorm de meeste kleurlagen in een vloeibaar mengsel

- Info: Maak zoveel mogelijk lagen in een erlenmeyer van allemaal oplossingen met verschillende dichtheid
- Moeilijkheid: moeilijk
- Chemische stoffen: gedemineraliseerd water – olie – honing – siroop – alcohol – Plasticine klei – zout – glycerine -kleurmiddelen
- Thema:stofeigenschappen – eigenschappen stoffen
- Tijd: 15 min
- Begrippen: dichtheidsverschillen – polariteit
3.12. Vul een pamper met het meeste water
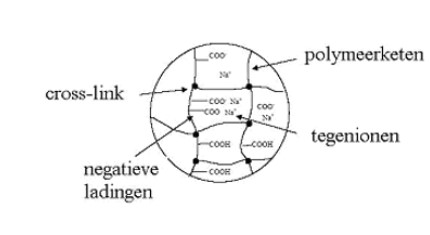
- Info: Probeer zoveel mogelijk water te binden met de gel uit 1 pamper in 10 minuten
- Moeilijkheid: eenvoudig
- Chemische stoffen: 1 pamper – water
- Thema:stofeigenschappen – eigenschappen stoffen – kuststoffen
- Tijd: 15 min
- Begrippen: polariteit – adsorptie
3.13. Kunstmatig lotuseffect op cd

- Info: Hoe kunnen we het lotuseffect nabootsen? De polycarbonaatlaag van de CD reageert met de aceton en vormt fijne kristallen die het oppervlak opruwen. Het resultaat is een ruw, super hydrofoob oppervlak in het bereik van nano /micrometer, dat werkt als een oppervlak met een lotuseffect. Aangezien er minder contactoppervlakken zijn tussen de waterdruppel en de CD, overschrijdt de cohesiekracht van het water de kleefkracht, waardoor het water meer globaal ontstaat.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Aceton – Oude CD
- Thema:stofeigenschappen – eigenschappen stoffen – nanodeeltjes
- Tijd: 15 min
- Begrippen: polariteit
3.14. Bloeiende bloemen

- Info: Hoe kunnen we papieren bloemen laten bloeien? Wanneer je het opgevouwen papier (de bloem) op water brengt zal het water naar boven stromen door het papier. Dit komt door de capillaire werking die het papier bezit. Het natte papier zal de vorm niet bewaren en de blaadjes spreiden zich uit.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Water
- Thema:stofeigenschappen – eigenschappen stoffen
- Tijd: 15 min
- Begrippen: polariteit – waterstofbruggen
3.15. Communicerende vaten

- Info: Hoe kunnen we lege glazen vullen zonder water over te gieten? D.m.v. capillariteit gaan de stukjes keukenrol, gekleurd water overbrengen van de volle bekerglazen naar de lege. Het gekleurd water uit twee aparte bekers gaat mengen en dus krijgen we een mengkleur. De uitwisseling van vloeistof gebeurt doordat we communicerende vaten verkrijgen, hierdoor dat er een evenwicht gaat zijn in het vloeistofniveau in alle bekerglazen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Keukenrol – Waterfles – kleurstoffen
- Thema:stofeigenschappen – eigenschappen stoffen
- Tijd: 15 min
- Begrippen: polariteit – waterstofbruggen
3.16. Drijvende kunst

- Info: Hoe kan je een tekening tot leven laten komen en doen bewegen? Door met whiteboardstift op een glad oppervlak te tekenen, zoals bijvoorbeeld een bord, kan je je tekening tot leven brengen. Dit door de tekening even te laten drogen en vervolgens water toe te voegen. Whiteboardstiften zijn namelijk zo gemaakt dat ze niet aan gladde oppervlakken blijven hangen, hierdoor kunnen er bij toevoeging van water, watermoleculen onder de tekening komen en deze zo los laten komen van het bord. Vervolgens is de stift niet oplosbaar in water en de densiteit is lager dan die van water. De tekening zal dus op het water blijven drijven.
- Moeilijkheid: eenvoudig
- Chemische stoffen: White boardstift – Diep bord – Water
- Thema:stofeigenschappen – eigenschappen stoffen
- Tijd: 15 min
- Begrippen: polariteit – waterstofbruggen
3.17. Kleurenregen

- Info: Hoe kunnen we een kleurrijke regen doen ontstaan met water en olie? Door gebruik te maken van polaire en apolaire eigenschappen van stoffen kan je zelf een kleurrijke regen creëren binnenshuis. De polaire voedingskleurstoffen zullen niet goed mengen met de apolaire olie, eens aangebracht op het water, zullen de kleurstoffen wel mengen met het polaire water en naar beneden vallen als regen.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Plantaardige olie – Vloeibare voedingskleurstoffen
- Thema:stofeigenschappen – eigenschappen stoffen
- Tijd: 15 min
- Begrippen: polariteit – waterstofbruggen
3.18. Motorboot
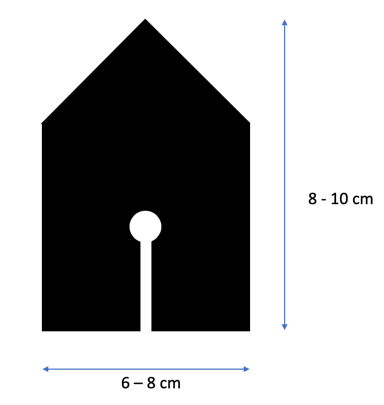
- Info: Hoe kunnen we een papieren bootje vooruit laten varen door een fysische reactie?
- Moeilijkheid: eenvoudig
- Chemische stoffen: Water – Papier – Afwasmiddel
- Thema:stofeigenschappen – eigenschappen stoffen
- Tijd: 15 min
- Begrippen: polariteit – waterstofbruggen
3.19. Stuiterende zeepbellen

- Info: Hoe kunnen we aantonen dat een bepaalde stof van wol gemaakt is? Glycerine maakt de randen van de zeepbel sterker. Wol zorgt ervoor dat er minimaal contact is tussen de zeepbel en de stof. Daarom zal de zeepbel bij niet-wollen stof barsten en bij wollen stof stuiteren.
- Moeilijkheid: eenvoudig
- Chemische stoffen: Water – Zeep – Glycerine
- Thema:stofeigenschappen – eigenschappen stoffen
- Tijd: 15 min
- Begrippen: polariteit – waterstofbruggen
3.20. Verdampingssnelheid

- Info: Op welke manier beïnvloeden intermoleculaire krachten de verdampingssnelheid van een stof?
- Moeilijkheid: gemiddeld
- Chemische stoffen: Aceton – Glycerol – Propaan-2-ol
- Thema:stofeigenschappen – eigenschappen stoffen
- Tijd: 25 min
- Begrippen: polariteit – waterstofbruggen – dipoolkrachten – dispersiekrachten






