Onderzoeksproject Verdampingssnelheid
1.Onderzoeksvraag
Op welke manier beïnvloeden intermoleculaire krachten de verdampingssnelheid van een stof?
2.Voorbereiding
Begrippen als achtergrond voor experiment
- Verdampingssnelheid
- Verbinding
- Waterstofbruggen
- Intermoleculaire krachten
Materiaal + stoffen
- 3 Temperatuursensoren
- 3 proefbuisjes
- Filtreerpapier
- Plakband
- Ipad die verbonden is met de sensoren
- Aceton
- Glycerol
- Propaan-2-ol
Opstelling

3.Uitvoeren
a. Werkwijze
- Verzamel de 3 proefbuisjes en nummer deze van 1 tot 3. In de eerste proefbuis doe je een cm aceton in, in de 2 de proefbuis een cm glycerol en in de 3de een cm propaan-2-ol.
- Verbind de thermometers met de meter en de ipad.
- Knip 3 rechthoekige strookjes van het filtreerpapier en wikkel deze rond de uiteindes van de thermometers. Maak het vast met een klein stukje plakband.
- Breng de thermometers in de 3 proefbuisjes gevuld met de stoffen.
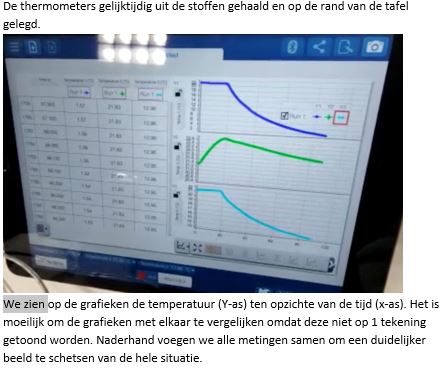
- Begin de metingen op de iPad en haal na een 10-tal seconden de thermometers gelijktijdig uit de proefbuisjes en leg deze over de rand van de tafel.
- Laat zo liggen tot de temperatuur stabiliseert.
- Noteer je waarnemingen en reflecteer.
b. Waarnemingen

4.Reflecteren
- Hoe meer en hoe groter de intermoleculaire krachten, hoe trager een stof verdampt (en hoe kleiner het gemeten temperatuurverschil zal zijn). Aceton is een keton en gaat het snelst verdampen aangezien hier de minste intermoleculaire krachten aanwezig zijn. De alcoholen glycerol en propaan-2-ol verdampen minder snel maar toch zeer verschillend van elkaar. De intermoleculaire krachten die hier aanwezig zijn, zijn: dispersiekrachten en dipoolkrachten ook waterstofbrugkrachten. De molaire massa bepaalt hier het verschil in de snelheid van de verdamping, hoe groter de molaire massa hoe sterker de intermoleculaire krachten dus hoe trager de verdamping.
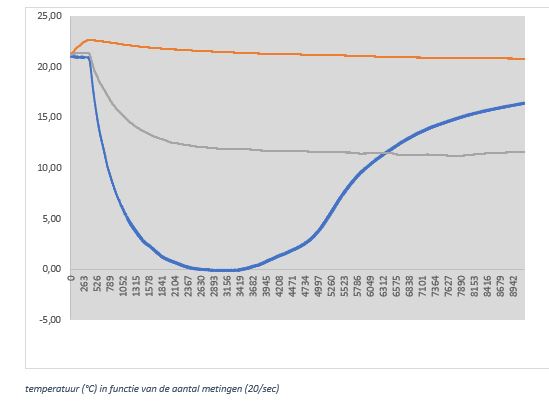
De interpretatie van de grafiek:
De glycerol zal het traagst verdampen en dus het traagst dalen in temperatuur. (rode lijn)
De propaan-2-ol zal redelijk snel beginnen te verdampen maar daarna stabiliseren. (grijze lijn)
De aceton zal zeer snel verdampen en dus zeer snel dalen in temperatuur maar hierna weer stijgen. De stijging gebeurt omdat de stof op dat moment volledig verdampt is en het papiertje terug aan het keren is naar kamertemperatuur. (blauwe lijn)






