Reacties met overgangselementen
1.Voorbereiding
a.Materiaal + stoffen
- CuSO4 0,5 mol/l
- Co(NO3)2 0,5 mol/l
- NiCl2 0,5 mol/l
- Mg(NO3)2 0,5 mol/l
- NH3 3 mol/l
- NaOH 1 mol/l
b.Opstelling (foto)
2.Uitvoeren
a.Werkwijze
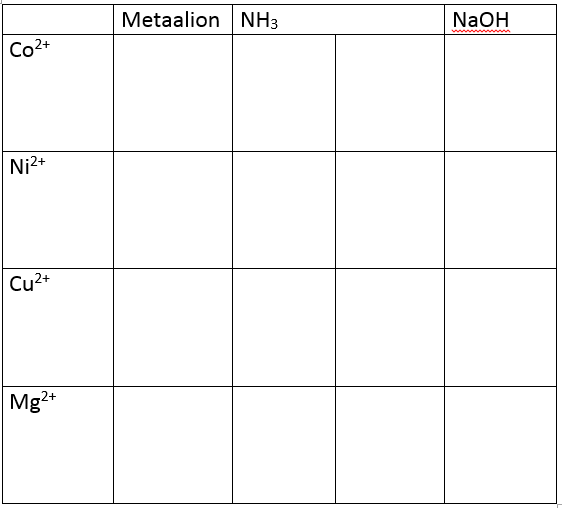
Reacties met NH3
- In de kolom met NH3 oplossing worden 4 druppels van de ionen telkens per twee aan elke zijde van de stippellijn gebracht.
- Voor kobalt. Voeg 1 druppel NH3 Voeg aan het rechter staal nog eens 3 druppels NH3 extra toe.
- Voor nikkel, voeg telkens 1 druppel NH3 Voeg na 1 minuut nog eens 5 druppels toe aan het rechter staal.
- Voor koper, voeg één druppel NH3 toe en roer. Voeg nu nog 3 druppels NH3 extra toe aan het rechter staal.
- Voor magnesium, voeg telkens 2 druppels NH3 Voeg nu nog eens 4 druppels NH3 aan het rechter staal.
Reacties met NaOH
- Breng telkens 2 druppels van de metaalionen in de vakjes in de kolom van NaOH oplossingen
- Voeg telkens 2 druppels NaOH oplossing toe.
b.Waarneming (+ foto’s)

3.Reflecteren
Voor kobalt
Toevoeging van een druppel NH3 geeft een diepgroene neerslag. Extra NH3 geeft een groen, bruine oplossing. Co2+ is stabieler dan Co3+. Toch indien Co2+ reageert met liganden zoals NH3 in het Co(NH3)62+ ontstaat een oxidatie naar Co(NH3)63+ wat een groen-bruine kleur geeft.
Voor nikkel
Toevoeging van een druppel NH3 geeft een lichtgroene neerslag van Ni(OH)2. Meer NH3 geeft het oplossen en vormen van een blauwe oplossing van het Ni(NH3)62+ complex.
Voor koper
Toevoeging van een druppel NH3 geeft een licht blauwe neerslag van Cu(OH)2. Meer NH3 geeft het diepblauwe Cu(NH3)42+
Voor magnesium
Toevoeging van NH3 geeft een witte neerslag van Mg(OH)2. Meer toevoegen geeft geen complex.
Proeven met NaOH
Alle metaalhydroxiden slaan neer met een typisch gekleurde neerslag.






