Oplosbaarheid van hydroxide
1.Onderzoeksvraag
Hoe goed lossen de verschillende hydroxiden op?
2.Voorbereiding
a.Begrippen als achtergrond voor experiment
- Hydroxide: verbinding tussen een metaalion en een hydroxide-ion: MOH
b.Materiaal + stoffen
- Fft indicator
- 5 erlenmeyers
- Ba(OH)2
- NaOH
- KOH
- Ca(OH)2
- Fe(OH)3
c.Opstelling (foto)

3.Uitvoeren
a.Werkwijze
Schud een kleine hoeveelheid vaste stof (mespunt of 1 pastille) los in een Erlenmeyer van 100ml die half gevuld is met water. Sommige hydroxiden lossen beter op dan andere. Door het troebele mengsel te filtreren, verkrijg je een heldere oplossing als filtraat. Test met fft.
We lossen elke hydroxide apart op in een erlenmeyer. Daarna filtreren we de oplossing en testen het filtraat met fft.
b.Waarneming (+ foto’s)
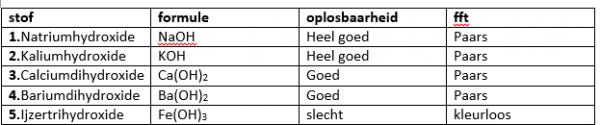

4.Reflecteren
De hydroxiden die goed oplossen, zitten ook in het filtraat. Hierdoor wordt het filtraat basisch en kleurt dit dus paars. Wanneer de hydroxide niet goed oplost, wordt de hydroxide opgevangen door het filtreerpapier en zit deze dus niet in het filtraat. Het filtraat kleurt niet en is dus ook niet basisch
5. Aanvullingen
Het filtreerpapier kan vervangen worden door koffiefilters.
Fe(OH)3 moet zelf gemaakt worden door 1M FeCl3 + 3M NaOH






