Onderzoeksproject Oplosbaarheid van anorganische stoffen
1.Onderzoeksvraag
Welke verbanden kunnen we vinden tussen de aard van deze stoffen en de oplosbaarheid in water?
We bestuderen de oplosbaarheid in water van
- HCl
- HNO3
- H3PO4
- HClO3
- NaOH
- Ca(OH)2
- CaCO3
- NaCl
- BaSO4
- KNO3
2.Voorbereiding
- De oplosbaarheid van HCl, H3PO4, HNO3 en HIO3 zoeken we op internet
- De oplosbaarheid van de andere verbindingen gaan we testen
- Een stof wordt volgens de meeste tabellen als goed oplosbaar beschouwd als een concentratie van 0.1 mol/l kan bereikt worden. Voor bijv. met een molaire massa van 101,1 g/mol, is dit 10,11 g/l. In een proefbuis met 10 ml water is dit 0.10 g. We kunnen dus werken met een spatelpunt aan vaste stof.
Benodigdheden:
- Proefbuisrek
- 5 proefbuizen 10ml
- Proefbuis kurk/plastic stop of parafilm
- Spatel
- de verschillende stoffen
3.Uitvoeren
a. Werkwijze
- Breng een spatelpunt vaste stof in een proefbuis
- Vul de proefbuis met demi water
- Dek de proefbuis af met parafilm of stop.
- Schud met de buis (max 3 min)
- Observeer oplosbaarheid
De vloeistof moet helder zijn en geen deeltjes bevatten om oplosbaarheid aan te tonen.
Als de vloeistof een witte “melkkleur” heeft is de stof niet opgelost.
b. Waarnemingen
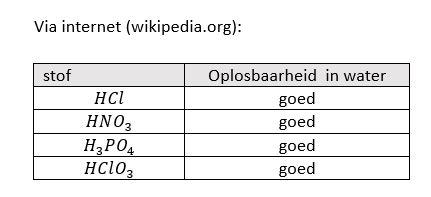


4.Reflecteren
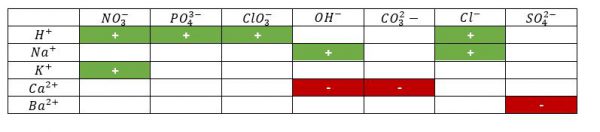
- Het is duidelijk dat alle zuren oplosbaar zijn in water.
- Zuren ioniseren in water
- De zouten en hydroxiden van de onderzochte alkalimetalen lossen op in water.
- De zouten en hydroxiden van de onderzochte aardalkalimetalen lossen niet op in water.
- Nitraatzouten van de aardalkalimetalen lossen wel op.
- Calciumhydroxide lost matig op






