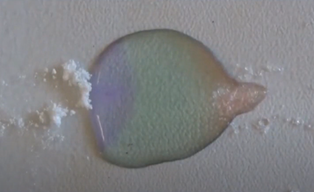
Natriumcarbonaat en citroenzuur aan beide zijden van een druppel universele indicator
1.Onderzoeksvraag
Hoe kun je een pH-gradiënt maken in een druppel?
2.Voorbereiding
a. Materiaal + stoffen
- Universele indicatoroplossing
- Geplastificeerd blad
- Citroenzuur
- Natriumcarbonaat
b. Opstelling
2.Uitvoeren
a.Werkwijze
- Maak een oplossing van 50ml universele indicator (15ml) en water (35ml).
- Voeg 2ml van de oplossing op een geplastificeerd blad.
- Aan de linkerzijde van deze grote druppel voeg je een beetje natriumcarbonaat toe, aan de rechterzijde citroenzuur. Dit mag eerst nog niet in contact komen met de oplossing van water en universele indicator.
- Breng vervolgens de 2 stoffen tegelijkertijd in contact met de oplossing.
- Er ontstaat enerzijds een kleurverandering, door de pH. Anderzijds ontstaat er CO2 wanneer de 2 stoffen met elkaar in contact komen
b. Waarneming en besluit (+ foto’s)

Aan de kant van het citroenzuur kleurt de pH-indicator zuur (rood van kleur), aan de kant van het natriumcarbonaat kleurt de pH-indicator basisch (blauw van kleur). Centraal is de pH ongeveer neutraal. Na verloop van tijd komen de stoffen in oplossing door diffusie naar elkaar toe en ontstaat een concentratiegradiënt en pH-gradiënt. Bij contact gaat uiteindelijk het natriumcarbonaat reageren met citroenzuur met vorming van waterstofcarbonaat wat ontleedt en koolzuurgas vrijzet.
Reactie:
3Na2CO3 + 2C6H8O7 –> 3CO2↑+ 3H2O +2Na3C6H5O7
Bron: Webinar “Microscale chemistry – in a little you can see a lot!” – YouTube






