Microschaalexperimenten met zuur-base indicatoren
1.Onderzoeksvraag
Hoe reageren bepaalde zuur-base indicatoren op NaOH- en HCl-oplossing? Welke invloed heeft concentratie van deze oplossingen op de kleur van de indicatoren?
2.Voorbereiding
a.Materiaal + stoffen
- Nucleonschaal, 6 bekerglazen en 6 pipetten
- NaOH opl. 0,01 mol/l, NaOH opl. 0,1 mol/l en HCl opl. 0,01 mol/l
- Universele indicator, methyloranje, thymolblauw en thymolftaleïne
b.Opstelling (foto)

c.Etiketten

3.Uitvoeren
a.Werkwijze
- Neem je nucleonschaal en neem deze over op papier om er een schema van te maken. Schrijf schematisch op wat je in welke kolom en in welke rij toevoegt.
- In je eerste kolom vul je vier vakjes gedemineraliseerd water.
- Vul je tweede kolom ook vier vakjes met gedemineraliseerd water maar voeg er hier nog enkele druppels HCl 0,01 mol/l oplossing aan toe.
- Vul je derde kolom ook vier vakjes met gedemineraliseerd water maar voeg er hier enkele druppels NaOH 0,01 mol/l oplossing aan toe.
- Vul je vierde kolom ook vier vakjes met gedemineraliseerd water maar voeg er hier enkele druppels NaOH 0,1 mol/l oplossing aan toe.
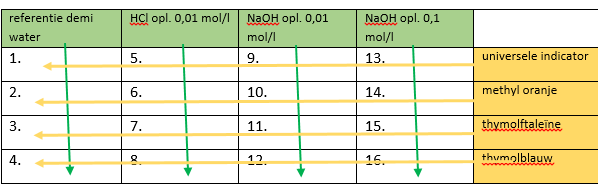
- Wanneer je nucleon schaal voorbereid is zoals hier boven staat kan je met de eigenlijke proef beginnen.
- Druppel dan enkele druppels universele indicator in de eerste vier vakjes in de eerste rij, dit doe je dus over je vorige kolommen heen.
- Druppel daarna enkele druppels methyl oranje in de eerste vier vakjes in de tweede rij.
- Druppel daarna enkele druppels thymolftaleïne in de eerste vier vakjes in de derde rij.
- Druppel daarna enkele druppels thymolblauw in de eerste vier vakjes in de vierde rij.
- Kijk dan naar de verschillende veranderende kleuren van de indicatoren.
b.Waarneming (+ foto’s)
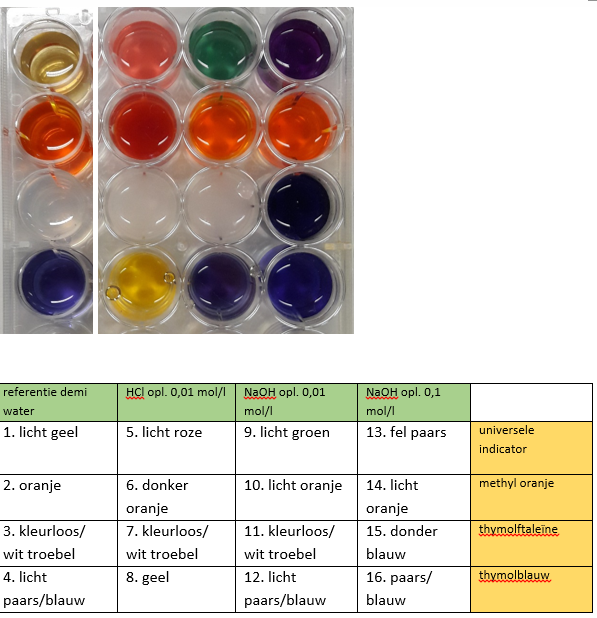
4.Reflecteren
We kunnen per indicator een kleur verandering waarnemen zoals deze staan in de tabel van de waarnemingen. De kleurverandering duidt er op dat het hier over verschillende pH waarden gaat.
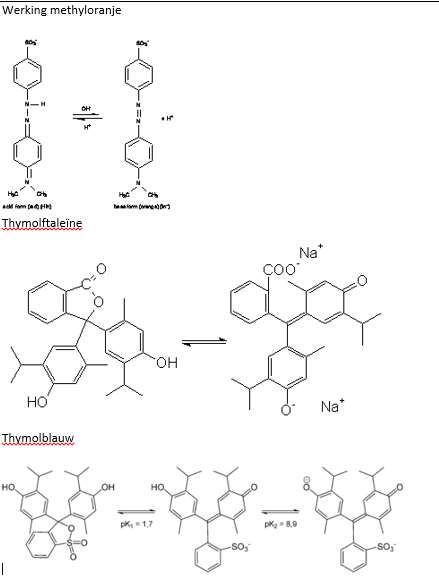
Alle indicatoren hebben een bepaald punt(een bepaalde pH waarde) waarop ze van kleur veranderen. Thymolftaleïne zijn omslaggebied ligt tussen de pH 9,3 en 10,5. Wanneer de pH van de oplossing hoger is dan pH 10,5 kleurt de indicator donker blauw, wanneer de pH van de oplossing lager is dan pH 9,3 kleurt de indicator kleurloos.
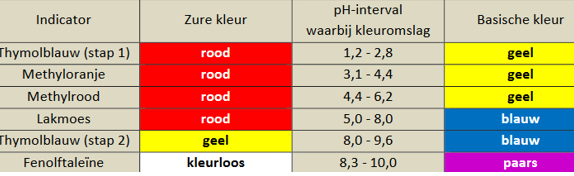
5. Aanvullingen
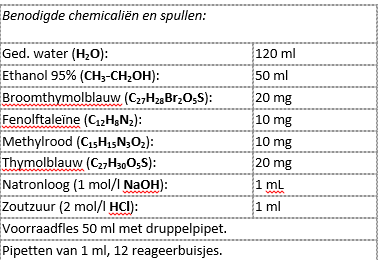

Werk met kleine hoeveelheden van de chemische stoffen en indicatoren! Met kleine hoeveelheden werken de proeven ook.
Weeg de vier indicatorstoffen af, doe ze in de fles, en voeg 50 ml ethanol toe. Gedenatureerde bioalcohol kan ook. Goed schudden om alles op te lossen, bij voorkeur een nachtje laten staan en nogmaals een paar keer schudden. Natuurlijk doe je er een etiket op.
Vervolgens kun je testoplossingen maken, bijvoorbeeld als volgt.
Neem 12 reageerbuisjes waarin je in het eerste 19 ml ged. water doet en in de overige elf 9 ml. Pipetteer 1 ml zoutzuur van 2 mol/l in de eerste erbij. Neem daartoe de droge pipet met pipetterballon en neem een ml op. Laat die in de regeerbuis erbij lopen. Zuig dan vanuit deze zelfde buis de pipet enige malen opnieuw vol en laat weer teruglopen. Schud de reageerbuis nogmaals met een dopje erop. Spoel de pipet nogmaals met de inhoud van de buis en neem precies 1 ml op die je in de tweede buis doet. Weer even opzuigen en terug laten lopen, schudden, weer spoelen en 1 ml in de derde buis doen. Dit alles herhaal je t/m de zesde buis. Pipetteer daarvan 1 ml op die je weggooit.
Dan spoel je de pipet met natronloog van 1 mol/l, en voeg je 1 ml van die loog bij buis nummer 12. Dan hetzelfde recept: schudden, spoelen, 1 ml opnemen en in buis 11 doen. Dan zo door tot buis 7, waarvan ook 1 ml wordt weggegooid. De buizen 1 t/m 12 bevatten nu oplossingen met opklimmende pH (t.w. ca. 1-6,8-13).
Bronnen






