Kerstlichtjes
1.Onderzoeksvraag
Hoe kunnen we zelf kerstlichtjes maken?
2.Voorbereiding
a.Begrippen als achtergrond voor experiment
Vlamproef: techniek gebruikt om de elementen-samenstelling van een monster vast te stellen, de kleur van de vlam is namelijk afhankelijk van de aanwezige metaalzouten.
b.Materiaal + stoffen
- 3g calciumacetaat
- 75ml ethanol
- 10g lithiumchloride
- 10g boorzuur
- Lucifer
- Maatbeker
- 2 pyrex horlogeglazen / petrischaaltjes
- Spatel
c.Opstelling (foto)
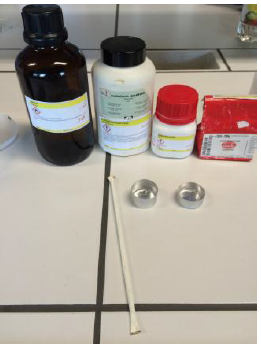
d.Etiketten


COS brochure
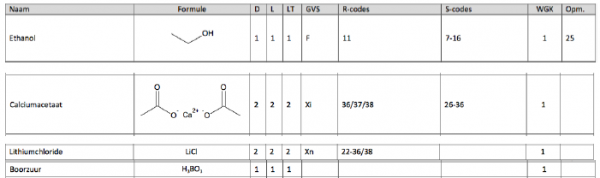
Volgens de COS-brochure mag deze proef uitgevoerd worden vanaf de 2e graad in het secundair onderwijs als:
- Demonstratieproef, uitgevoerd door de leerkracht.
- Leerlingenproef in richtingen waar chemie niet als hoofdvak beschouwd kan worden.
Leerlingenproef in richtingen waar chemie een hoofdvak is (vb: Techniek-Wetenschappen, Chemie, Biotechnische wetenschappen,…)
3.Uitvoeren
a.Werkwijze
- Doe 3g calciumacetaat in een maatbeker van 250ml.
- Voeg 10ml gedestilleerd water toe en meng met de calciumacetaat.
- Voeg 75ml ethanol toe. Er wordt onmiddellijk een gel gevormd. (niet roeren!)
- Gebruik een spatel om de gel over te brengen naar 2 pyrex petrischaaltjes.
- Strooi 10g lithiumchloride over de gel in 1 petrischaal en 10g boorzuur over de gel in de andere petrischaal.
- Steek in beide schaaltjes de gel in brand.
b.Waarneming (+ foto’s)
We mengen 3g calciumacetaat en 10ml gedestilleerd water in een maatbeker. Hierbij voegen we 75ml ethanol. We zien dat er onmiddellijk een gel wordt gevormd.

We verdelen de gel over 2 pyrex petrischaaltjes (in dit geval maakten we gebruik van de omhulsels van theelichtjes). We strooien lithiumchloride over de gel in 1 houdertje en boorzuur over de gel in het andere houdertje. Daarna steken we de gel in brand.

4.Reflecteren
Neerslagvorming bij reactie tussen ethanol en calciumacetaat: strengen Ca(OAc)2 worden gevormd (Sterno)
Bij het samenvoegen van calciumacetaat en ethanol wordt een ontvlambare gel gevormd. Wanneer je deze gel aansteekt, wordt het boorzuur en de lithiumchloride opgewarmd. Deze stoffen nemen energie op en lanceren hun elektronen naar een geëxciteerde toestand. Wanneer de elektronen hun energie vrijgeven, doen ze dit in de vorm van licht. De kleur is afhankelijk van de golflengte van het licht.
5. Aanvullingen
Je kan uiteraard ook andere metaalverbindingen gebruiken om de vlamproef uit te voeren.
In plaats van pyrex petrischaaltjes kan je ook gewoon de omhulsels van theelichtjes gebruiken.
Bronnen






