Ijzerevenwicht
1.Voorbereiding
a.Materiaal + stoffen
- FeCl3 0.2 g/100 ml
- KSCN 0.2 g/100 ml
- K4Fe(CN)6 1g/100 ml
- tanninezuur 0.2 g/100 ml
- salicylzuur 0.2 g/100 ml
- EDTA 2g/100 ml
- 6 bekers 600 ml
2.Uitvoeren
a.Werkwijze
- Breng in beker1 de Fe-oplossing.
- In de tweede beker 20 ml 0.2% salicylzuur
- In de derde beker 20 ml KSCN 0.2%
- In de vierde beker 20 ml wijnsteenzuur 0.2%
- In de vijfde beker 100 ml K4Fe(CN)6
- In de zesde beker 100 ml 2% EDTA
- Breng de inhoud van beker1 op 100 ml na in beker 2.
- Voeg nu de in houd van beker2 op 50 ml na in beker 3. Doe zo verder en hou telkens 50 ml over in de beker.
3.Reflecteren
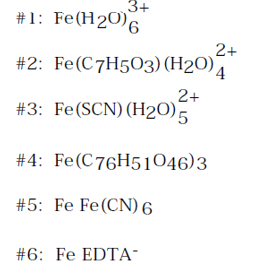
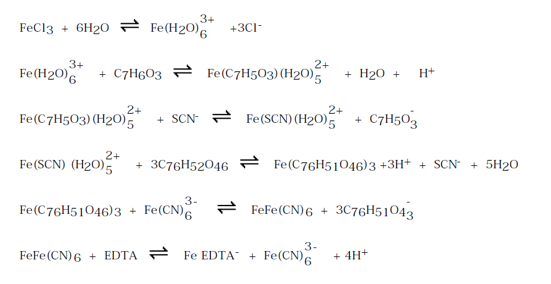
De laatste stap is niet sterk overtuigend omwille van de sterk blauwe kleur van de vorige stap.
Mogelijke oplossing is het hexacyanocomplex sterk te verdunnen voor de laatste stap wordt aangevat.
De stappen kunnen eventueel met kleinere hoeveelheden uitgevoerd worden in nuncleonschaaltjes.
-beker1: geel
-beker2: paars
-beker3: donker rood Fe(SCN)3
-beker4: blauwzwart
-beker5: blauw
-beker6: groen






