Gebeuren alle chemische reacties even snel?
1.Onderzoeksvraag
Gebeuren alle chemische reacties even snel?
2.Voorbereiding
a.Materiaal + stoffen
- 2 proefbuizen
- 2 pasteurpipetten
- Wattenprop
- Horlogeglas
- IJzeren nagel
- Staalwol
- Maatbeker
- 2 ml CuSO4-oplossing 0,1mol/l
- 2 ml NH3-oplossing 1,0 mol/l
b.Opstelling (foto)

3.Uitvoeren
a.Werkwijze
Deel 1:
- Schuur de ijzeren nagel op met staalwol.
- Maak vervolgens een wattenprop nat, en leg deze op het horlogeglas zodat het water langer behouden blijft.
- Leg dan de afgeschuurde nagel op de natte wattenprop.
Deel 2:
- Breng in een proefbuis 2 ml CuSO4. Dit doe je door eerst een kleine hoeveelheid in een maatbeker te gieten en vervolgens met de pasteurpipet 2 ml over te pipetteren in de proefbuis.
- Breng in de andere proefbuis 2 ml NH3. Dit doe je volgens dezelfde manier als met CuSO4. Spoel eerst de maatbeker even uit!
- Giet nu de 2 vloeistoffen samen en noteer je waarneming.
b.Waarneming (+ foto’s)
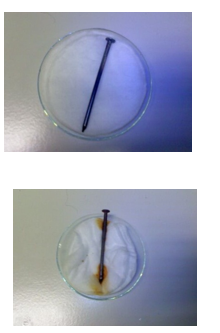

- Deel 1:
- Welke kleur heeft de droge spijker?
- Grijs.
- Welke kleur heeft de spijker op de natte wattenprop na 5 minuten?
- Nog steeds grijs.
- Deel 2:
- Welke kleur heeft de CuSO4– oplossing?
- Lichtblauw.
- Welke kleur krijgt de oplossing na toevoeging van NH3?
- Felblauw.
- Hoelang duurt het voor er kleurverandering optreedt?
- De reactie treedt onmiddellijk op.
4.Reflecteren
Vergelijk de snelheid van beide reacties met elkaar. Wat kun je vaststellen?
De tweede reactie treedt onmiddellijk op, de eerste reactie treedt traag op.
Optredende reacties:
4 Fe + 3 O2 –> 2 Fe2O3 (trage reactie)
Cu2+ + 4 NH3 –> Cu(NH3)42+ (tetramminekoper(II)ion) (snelle reactie






