De reactie van metalen met zuren
1.Voorbereiding
a.Materiaal + stoffen
- geplastificeerd papier
- pipetten
- HCl 1 mol/l
- HNO3 1 mol/l
- HNO3 5 mol/l
- H2SO4 1 mol/l
- Mg lint
- Zn korrels
- Fe poeder
- Sn korrels/poeder
- Cu draad of poeder
b.Opstelling (foto)
2.Uitvoeren
a.Werkwijze
- Maak bijhorend blad en plastificeer
- Leg wat koperpoeder of draad in de koperrij
- Leg telkens een klein stukje Mg draad in de Mg rij
- Leg telkens wat zinkgranulen in de Zn rij
- Leg telkens wat ijzer poeder in de Fe rij
- Leg telkens wat tinpoeder of –granulen in de Sn-rij
- Voeg nu in de HCl kolom telkens 2 druppels verdunde HCl
- Voeg in de H2SO4 rij telkens 2 druppels H2SO4
- Voeg in de HNO3 kolom telkens 2 druppels verdunde HNO3
- Leg in de laatste box een klein stukje koper en voeg hieraan 2 druppels geconcentreerd HNO3
b.Waarneming (+ foto’s)
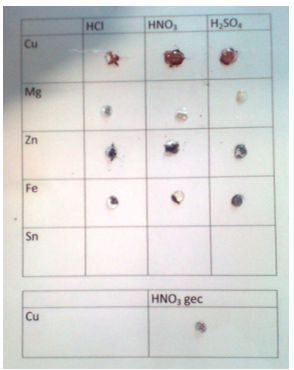
3.Reflecteren
Het Mg lint reageert vrij hevig met elk zuur. Het Fe en Zn reageren eveneens, maar minder sterk. In alle gevallen wordt H2 gas gevormd en een aantal metaalzouten. De reactie tussen Fe en HNO3 veroorzaakt ook een bruine roest van Fe2O3.
Sn en Cu reageren niet met HCl en H2SO4, enkele bellen ontstaan (te zien met vergrootglas) met HNO3.
Het Cu reageert wel met de geconcentreerde HNO3 tot een blauwe oplossing en een bruin gas NO2.






