De overgangselementen
1.Voorbereiding
a.Materiaal + stoffen
- K2CrO4 0,2 mol/l
- KMnO4 0,2 mol/l
- Co(NO3)2 0,5 mol/l
- NH3 3 mol/l
- HCl 1 mol/
- NaOH 1 mol/l
- NiCl2 0,5 mol/l
- CuSO4 0,2 mol/l
- FeSO4 0,2 mol/l
- Fe(NO3)3 0,2 mol/l
- AgNO3 0,2 mol/l
- KSCN 0,1 mol/l
- KI 0,2 mol/l
- Zetmeeloplossing
- Zn granulen
b.Opstelling (foto)
2.Uitvoeren
a.Werkwijze
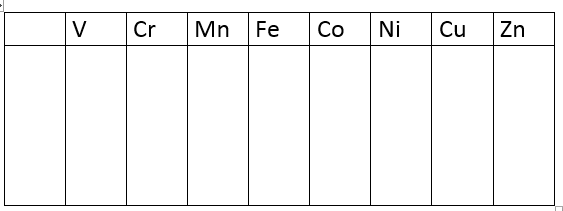
- Print bovenstaande tabel af en plastificeer het blad
- Breng telkens 2 druppels op verschillende plaatsen in het vakje van de aangeduide overgangselementen . Observeer.
- Voeg nu telkens aan 1 van de twee druppels de andere reagentia. De andere druppel dient als referentie
- Cr: Voeg een druppel AgNO3 oplossing toe
- Mn: Voeg een druppel Fe(II) oplossing toe
- Fe: Voeg een druppel KI oplossing toe. Voeg na een minuut 1 druppel zetmeeloplossing toe
- Co: Voeg 1 druppel NH3 oplossing toe
- Ni: Voeg twee druppels NaOH oplossing toe
- Cu: Voeg 1 druppel NH3 oplossing toe
- Zn: Voeg 2 druppels NaOH oplossing toe.
b.Waarneming (+ foto’s)

- Cr: Er ontstaat de rode neerslag Ag2CrO4.
- Mn: De paarse kleur van KMnO4 vermindert geleidelijk tot een bruine MnO2 en een licht roze Mn2+.
- Fe: De gele kleur ontstaat geleidelijk als Fe(II) jodide oxideert. Toevoeging van zetmeel geeft een blauwzwarte kleur door reactie van zetmeel met gevormde dijood.
- Co: Toevoeging van NH3 geeft een diepgroene neerslag. Toevoeging van meer geeft een groene of bruine oplossing.
- Ni: Toevoeging van NaOH geeft een groene neerslag van Ni(OH)2
- Cu: Toevoeging van NH3 geeft een blauwe neerslag van Cu(OH)2 en een fel blauwe kleur door Cu(NH3)42+ ionen
- Zn: Er ontstaat een witte neerslag van Zn(OH)2






