Buffermengsels
1.Onderzoeksvraag
Op welke manier kunnen we een keukenzoutoplossing onderscheiden van een bufferoplossing?
2.Voorbereiding
a. Materiaal + stoffen
- Keukenzoutoplossing (1,0 mol/l)
- Zelfgemaakte bufferoplossing met pH = 7
- Methyloranje-indicator
- HCl-oplossing (0,10 mol/l )
- fenolftalëine indicator (0,05%)
- NaOH- oplossing (0,10 mol/l)
- 4 proefbuizen
- Proefbuisrek
Bereiding van de bufferoplossing:
De bereiding van 100 ml bufferoplossing gebeurde door het samenvoegen van 61,2 ml 0,2 mol/l NaH2PO4 en 38,8 ml 0,2 mol/l Na2HPO4.
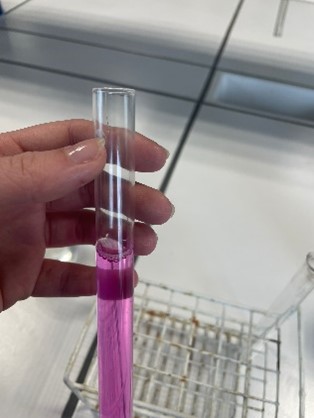
b.Opstelling (foto)

3.Uitvoeren
a.Werkwijze
- Nummer vier proefbuizen.
- Breng met een pasteurpipet 5,0 ml keukenzoutoplossing in de genummerde proefbuizen 1 en 3.
- Breng met een ander pipet 5,0 ml bufferoplossing (pH=7) in de genummerde proefbuizen 2 en 4.
- Breng twee druppels methyloranje indicator in de genummerde proefbuizen 1 en 2.

- Voeg aan de proefbuizen 1 en 2 druppel per druppel HCl-oplossing (0,10 )toe tot de kleur van de oplossing verandert.
- Schud even met de proefbuis na iedere toevoeging.
- Noteer voor iedere proefbuis hoeveel druppels je moet toevoegen om de kleurverandering te veroorzaken.
- Breng twee druppels fenolftalëine indicator in de genummerde proefbuizen 3 en 4.

- Voeg aan de proefbuizen 3 en 4 druppel per druppel NaOH-oplossing (0,10 ) toe tot de kleur van de oplossing verandert.
- Schud even met de proefbuis na iedere toevoeging.
- Noteer voor iedere proefbuis hoeveel druppels je moet toevoegen om de kleurverandering te veroorzaken.
- Vergelijk het aantal druppels zuur dat je moet toevoegen in proefbuizen 1 en 2 om een blijvende kleurverandering van methyloranje te veroorzaken.
- Vergelijk het aantal druppels base dat je moet toevoegen in proefbuizen 3 en 4 om een blijvende kleurverandering van fenolftaleïne te veroorzaken.
Omschrijf de invloed van de buffer op de pH van een oplossing.
b.Waarneming en besluit (+ foto’s)
Bij een buffer is de formule voor de pH: ![]()
Als we dit gaan invullen voor de NaH2PO4/Na2HPO4-buffer met pKz van 7.2, krijgen we: 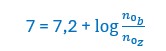
De bereiding (zie hierboven) zorgt voor de gevraagd pH van 7.
Het omslaggebied van methyloranje ligt tussen pH 3,1 en pH 4,4.
Als we de HCl-oplossing toevoegen bij de oplossing met methyloranje zien we dat het omslaggebied bij pH 4 ligt. We moeten dus van pH=7 zakken tot pH= 4. We moeten hiervoor vele druppels van de HCl-oplossing toevoegen.
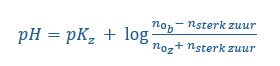
Het omslaggebied van fenolftaleIne ligt tussen pH 8,2 en pH 9,8.
Als we de NaOH-oplossing toevoegen bij de oplossing met fenolftaleïne zien we dat het omslaggebied bij pH 9-10 ligt. De pH moet dus stijgen van 7 naar 10. Om naar pH=10 te gaan moet er veel NaOH-oplossing toegevoegd worden.

Bij het keukenzout is de formule pH= -log c bij de toevoeging van de zoutzuuroplossing en pH = 14 + log c bij de toevoeging van de natriumhydroxide oplossing. Dus elke druppel die je gaat toevoegen heeft invloed op de pH.






