Verdringingsreacties metalen
1.Onderzoeksvraag
Hoe kunnen we metalen ordenen qua reactiviteit?
2.Voorbereiding
a.Begrippen als achtergrond voor experiment
- Verdringingsreeks metalen, oxidatie, reductie
b.Materiaal + stoffen
- Bord
- Pipet
- Koper(II)sulfaat 75 ml 0,1 mol/l
- Zinksulfaat 75 ml 0,1 mol/l
- Magnesiumsulfaat 75 ml 0,1 mol/l
- Loodsulfaat 75 ml 0,1 mol/l
- Magnesiumlint
- Zink folie
- Lood
- Koper
c.Bereiding oplossingen
CuSO4(aq): 0,1 mol/l . 0,1l = 0,01 mol . 159,61 g/mol = 1,596 gram
ZnSO4(aq) : 0,1 mol/l . 0,1l = 0,01 mol . 161,44 g/mol = 1,610 gram
MgSO4(aq) : 0,1 mol/l . 0,1l = 0,01 mol . 120,36 g/mol = 1,200 gram
PbSO4(aq) : 0,1 mol/l . 0,1l = 0,01 mol . 303,26 g/mol = 3,03 gram
d.Opstelling (foto)
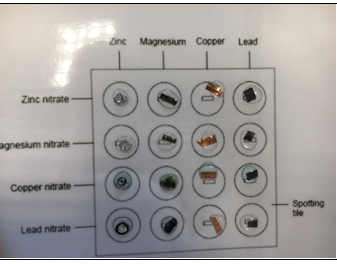
e.Etiketten
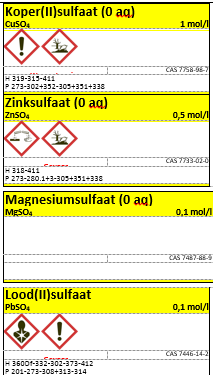
3.Uitvoeren
a.Werkwijze
- Druppel een beetje zinksulfaat oplossing in 4 cirkeltjes.
- Doe dit voor ieder zout.
- Observeer enkele minuten en bekijk de reacties
b.Waarneming (+ foto’s)
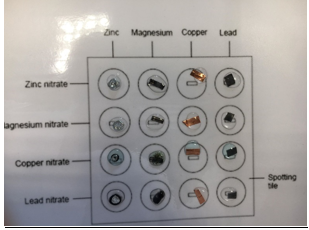
De eerste 2 vakjes van zink reageren niet. Zink regeert een beetje met kopersulfaat en het reageert fel met loodsulfaat. Magnesiumlint reageert in de eerste 2 vakjes zwak. In de laatste 2 reageert het fel en zal het uiteindelijk oplossen.
Koper reageert nergens. Lood reageert ook nergens of heel zwakjes.
4.Reflecteren
Zn + CuSO4 → Cu + ZnSO4
Zn + Pb(NO3)2 –>à Pb + Zn(NO3)2
Mg + Zn(NO3)2 –> Zn + Mg(NO3)2
Mg + CuSO4 –> Cu + MgSO4
Mg + Pb(NO3)2 –> Pb + Mg(NO3)2
Tussen zink en kopersulfaat wordt er koper en zinksulfaat gevormd. Tussen zink en loodnitraat wordt er lood en zinknitraat gevormd. Tussen magnesium en zinknitraat wordt er zink en magnesiumnitraat gevormd. Tussen magnesium en kopersulfaat wordt er koper en magnesiumsulfaat gevormd. Tussen magnesium en loodnitraat wordt er lood en magnesiumnitraat gevormd. Magnesium oxideert in het algemeen dus het makkelijkste met daarop volgend zink.






