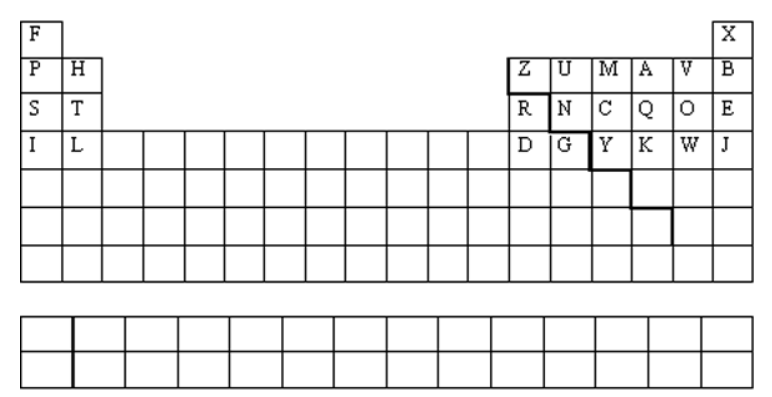
Het periodiek systeem

Printen:
Spel:
Het doel van het spel is dat de letters A tot en met Z, die op willekeurige wijze elementen
voorstellen, op de juiste wijze op een PSE worden geplaatst.
Op dertig kaartjes staan de volgende aanwijzingen:
1. D bevat 10 protonen
2. L heeft het hoogste kookpunt van de elementen in zijn groep.
3. Een atoom Z heeft 2 neutronen
4. V is kleiner dan J.
5. Van J is een aardalkalimetaal.
6. De volgende elementen horen bij elkaar in groepen: BFT- DGLZ-JNV-CMS-QXY-AEO-IPHUKWR
7. De elektronen van atoom G zijn verdeeld over 3 hoofdniveaus
8. G is een edelgas
9. Q is een sterkere oxidator dan Y
10. X is een vloeistof, terwijl Q en Y gassen zijn
11. Q is een halogeen
12. C lijkt chemisch gezien meer op S dan op M
13. De elektronegativiteit van S is groter dan die van M
14. Met W kan C water vormen
15. E heeft 5 elektronen in de buitenste schil.
16. De elektronen van O zijn verdeeld over 2 hoofdniveaus.
17. O is een gas, maar E niet
18. Atomen van E zijn lichter dan de atomen van A
19. H heeft een proton meer in de kern dan F.
20. P gaf een bevestiging van de voorstelling van de tabel van Mendelejev.
21. H kan als HO of als HO2 in de lucht zitten.
22. I is het meest voorkomend element op aarde, op één na. I komt in de natuur alleen in gebonden vorm voor.
23. T is het aardmetaal uit de 4de periode
24. F heeft de kleinste atoommassa van alle elementen in zijn groep
25. De atoomstraal van T is groter dan de atoomstraal van B
26. De EN-waarde van R is groter dan die van U.
27. U is een alkalimetaal
28. W is een gas
29. N heeft minder elektronen dan F
30. De kernlading van K is groter dan die van U.
Opl:
A:As;B:Al;C:O;D:Ne;E:P;F:B;G:Ar;H:C;I:Si;J:Ca;K:K;M:Se;N:Be;O:N;P:Ge;Q:F;R:Li;S:S;T:Ga;U:Na;V:Mg;W:
H;X:Br;Y:Cl;Z:He
Spel2:
Plaats de volgende onbekende hoofdgroepselementen op de lege periodieke tabel met behulp van de verstrekte aanwijzingen.
De onbekende elementen horen bij deze groepen, maar niet noodzakelijk in deze volgorde: ZRD PSIF JXBE LHT QKA WOV GUN YMC
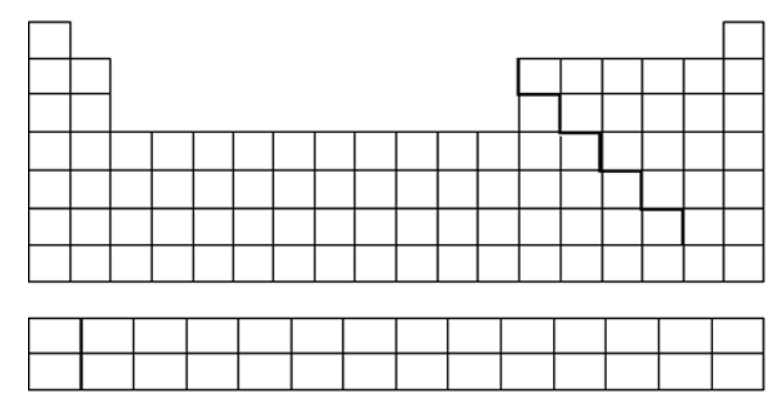
- U heeft in totaal 6 elektronen in het neutrale atoom
- I2A is de eenvoudige formule van een oxide (I heeft 1 valentie-elektron)
- P is minder dicht dan S
- S is een alkalimetaal
- E is een edelgas
- W is een vloeistof bij kamertemperatuur
- Z heeft de hoogste ionisatie-energie in zijn groep (Z heeft de minst bezette schillen in zijn groep)
- B heeft 10 protonen
- O heeft een lagere chemische reactiviteit en lagere ionisatie-energie dan V (De valentie-elektronen van O zitten in de M-schil)
- D heeft de laagste elektronenaffiniteit van zijn groep (staat voor het element G)
- C heeft 5 elektronen in het buitenste energieniveau
- F is een kleurloos gas
- X heeft een atoomnummer één hoger dan F
- Y is een niet-metaal
- O is een halogeen
- T heeft een hogere chemische reactiviteit dan die van H
- J heeft een atoomnummer dat drie keer zo groot is als dat van T
- Q heeft een atomaire massa die 2 keer die van A is
- Atomen van I zijn groter dan die van S
- M heeft een grotere atomaire straal dan die van A
- De elektronen van het atoom N zijn verdeeld over 3 belangrijke energieniveaus
- De atoomstraal van K is de grootste van de groep
Oplossing: