Waterstofbromaat
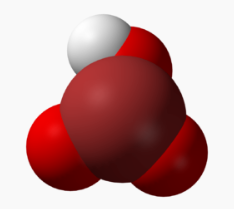
| Formule | HBrO3 |
| Familie | anorganische zuren |
| Productie |
Broomzuur is het product van een reactie van bariumbromaat en zwavelzuur.
Bariumsulfaat is onoplosbaar in water en vormt een neerslag. Het waterige broomzuur kan worden gedecanteerd waarbij het bariumsulfaat wordt verwijderd. |
| Eigenschappen |
Broomzuur bestaat alleen in een kleurloze oplossing, indien er contact wordt gemaakt met de lucht kleurt de oplossing gelig De verbinding heeft een molecuulmassa van 128,91 g / mol. De verbinding is een sterk oxidatiemiddel. Wanneer gemengd met ethanol of ether ontleedt het vormen van azijnzuur in een exotherme reactie. |
| Toepassingen |
Het broomzuur wordt gebruikt als een krachtig oxidatiemiddel in laboratoriumreacties. Het wordt gebruikt voor het produceren van chemische verbindingen zoals jodaten, chloorzuur, tetrahyonzuur en andere. Het wordt ook gebruikt voor de productie van bromaten zoals ijzer, lood, mangaan, kwikbromaat en andere. De oscillatiereactie wordt gekatalyseerd door cerium-ionen en is inherent verbonden met de chemie van broomoxozuren HBrOx. De groeiende belangstelling voor niet-lineaire chemische systemen heeft sterke prikkels gegeven om de chemie van broom te bestuderen. Broomzuur fungeert als een belangrijk tussenproduct in de Belousov-Zhabotinsky-reactie. In de reactie zijn de betrokken broomverbindingen het hypobromachtige zuur HOBr, het bromigzuur HOBrO en het broomzuur HBrO3 . Dit soort reacties zijn belangrijk voor de theoretische chemie. Ze laten zien dat chemische reacties niet moeten worden gedomineerd door het thermodynamische evenwichtsgedrag. |
| Geschiedenis |
|
| Bronnen | KLIK |






