Van elementen tot PSE
APP: http://www.teachchemistry.org/bonding
Opdracht 1: Even herhalen
Vraag 1 : Beschrijf het verschil tussen een atoom en een molecule.
Vraag 2 : Duid aan in het PSE:
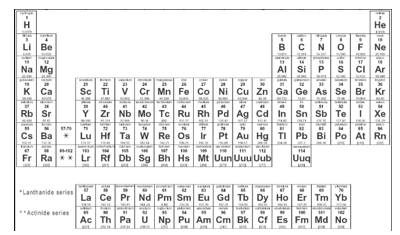
- Metalen : groen
- Niet-metalen : rood
Vraag 3 : Welke elementaire deeltjes vormen de chemische binding?
Vraag 4 : Beschrijf in je eigen woorden wat een valentie-elektron is.
Vraag 5 : Hoe kan je het aantal valentie-elektronen van een atoom bepalen met het PSE?
Vraag 6 : Teken de Lewisstructuur van de volgende atomen:
- Strontium (Sr) b. Koolstof (C)
- Zuurstof (O) d. Xenon (Xe)
Welke van bovenstaande atomen bezitten de edelgasconfiguratie?
Opdracht 2: Onderzoeksvraag

Stap 1: Kies Natrium(Na).
- Welk type element is natrium?
- Hoeveel valentie-elektronen heeft een natriumatoom?
- Vul aan.
Theoretisch kan natrium een edelgasconfiguratie bereiken door 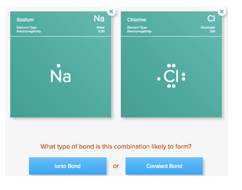
- Ofwel … elektronen op te nemen
- Ofwel … elektronen af te geven
Het Na-atoom zal eerder geneigd zijn één elektron af te geven dan zeven op te nemen. Opname zou immers zeer sterke afstotingskrachten tussen die elektronen met zich meebrengen.
Stap 2: Kies Chloor (Cl).
- Welk type element is chloor?
- Hoeveel valentie-elektronen heeft een chlooratoom?
- Vul aan.
Theoretisch kan chloor een edelgasconfiguratie bereiken door
- Ofwel … elektronen op te nemen
- Ofwel … elektronen af te geven
De opname van 1 elektron is echter veel waarschijnlijker dan de afgifte van 7 elektronen.

Stap 3: Beantwoord de vraag op jouw scherm: “What type of bond is this combination likely to form?”
- Omcirkel: Ionic of Covalent.
- Kies het aantal atomen per soort die je nodig hebt om de binding te vormen:
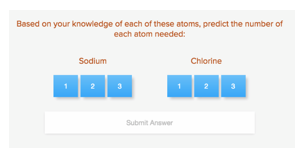
Stap 4: Kijk goed naar de animatie!
Kijk naar de verandering in het aantal valentie-elektronen van de atomen wanneer de atomen binden.
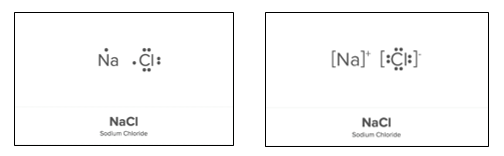
Wat betekent de positieve (+) lading?

Wat betekent de negatieve (-) lading?

Wat is de uiteindelijke lading van de molecule?
Vermeld hier de formule van de gevormde molecule.

Reset de simulatie.
Stap 5: Kies Calcium (Ca).
- Welk type element is calcium?
- Hoeveel valentie-elektronen heeft een calciumatoom?
- Vul aan en kleur het ‘meest waarschijnlijke’ bolletje.
Theoretisch kan calcium een edelgasconfiguratie bereiken door
- Ofwel … elektronen op te nemen
- Ofwel … elektronen af te geven
Schrap wat niet past: We verkrijgen een kation / anion.
Stap 6: Kies Fluor (F).
- Welk type element is fluor?
- Hoeveel valentie-elektronen heeft een fluoratoom?
- Vul aan en kleur het ‘meest waarschijnlijke’ bolletje.
Theoretisch kan calcium een edelgasconfiguratie bereiken door
- Ofwel … elektronen op te nemen
- Ofwel … elektronen af te geven
Schrap wat niet past: We verkrijgen een kation / anion.
Stap 7: Beantwoord de vraag op jouw scherm: “What type of bond is this combination likely to form?”
- Omcirkel: Ionic of Covalent.
- Kies het aantal atomen per soort die je nodig hebt om de binding te vormen:
Stap 8: Kijk goed naar de animatie!
Waarom heb je in totaal meer dan 2 atomen nodig om deze binding te maken?
Verklaar wat er gebeurde met de valentie-elektronen in elk atoom.
Wat is de totale lading van de molecule?
Vermeld hier de formule van de gevormde molecule.
Herken je een verband tussen de lading van het ion en het aantal valentie-elektronen van het atoom? Verklaar hoe je de lading kan voorspellen aan de hand van het aantal valentie-elektronen, of aan de hand van de positie van het element in het PSE.
Reset de simulatie.
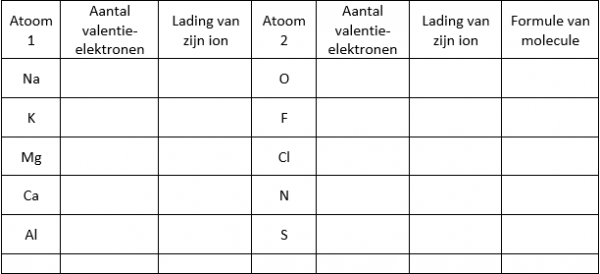
Stap 9: Gebruik je PSE om volgende tabel in te vullen. Controleer daarna jouw antwoorden met de simulatie.
Opdracht 3: Besluit
Vraag 1: Vul de tekst aan. Controleer daarna je antwoord met de bovenstaande definities.
Een binding tussen een metaal en een niet-metaal noemen we een .
Het staat zijn valentie-elektronen af aan het zodanig dat beide elektronen op de buitenste schil verkrijgen.
De ionen worden hierbij aan elkaar gebonden door hun onderlinge
aantrekkingskracht.
Een positief ion wordt gevormd door het van elektronen en noemen we een .
Een negatief ion wordt gevormd door het van elektronen en noemen we een .
Vraag 2: Begin met het tekenen van de lewisstructuren van natrium en chloor. Duid daarna aan op de tekening wat er gebeurt met de valentie-elektronen als ze een ionbinding vormen.
Vraag 3: Wat zijn de verschillen tussen ionbindingen en covalente bindingen? Verwijs in je antwoord naar de valentie-elektronen.






