Scheitrechter
Wat/Wie?
Begrip
Een scheitrechter , ook bekend als een scheidingstrechter , wordt gebruikt bij vloeistof-vloeistofextracties om de componenten van een mengsel te scheiden ( partitioneren ) in twee niet-mengbare oplosmiddelfasen met verschillende dichtheden . Typisch zal een van de fasen waterig zijn en de andere een organisch oplosmiddel zoals ether ,chloroform of ethylacetaat . Al deze oplosmiddelen vormen een duidelijke scheiding tussen de twee vloeistoffen. De meer dichte vloeistof, meestal de waterige fase, tenzij de organische fase gehalogeneerd is , zinkt en kan via een kraantje worden afgevoerd, weg van de minder dichte vloeistof, die in de scheitrechter achterblijft.
Weetjes
.De scheitrechter is gebaseerd op het concept dat het vermogen beschrijft van polaire oplosmiddelen om polaire opgeloste stoffen op te lossen en niet-polaire oplosmiddelen om niet-polaire opgeloste stoffen op te lossen. Wanneer de scheitrechter wordt geschud, migreert elke opgeloste stof naar het oplosmiddel (ook wel “fase” genoemd) waarin het beter oplosbaar is.
De oplosmiddelen vormen normaal gesproken geen verenigde oplossing samen omdat ze niet mengbaar zijn. Wanneer de trechter na het roeren stationair wordt gehouden, vormen de vloeistoffen verschillende fysieke lagen – vloeistoffen met een lagere dichtheid blijven boven vloeistoffen met een hogere dichtheid. Een mengsel van opgeloste stoffen wordt dus gescheiden in twee fysiek gescheiden oplossingen, elk verrijkt met verschillende opgeloste stoffen.
De afsluitkraan kan worden geopend nadat de twee fasen zijn gescheiden, zodat de onderste laag uit de scheidingstrechter kan ontsnappen. De toplaag kan in de scheitrechter worden vastgehouden voor verdere extracties met extra batches oplosmiddel of worden afgevoerd naar een apart vat voor andere toepassingen. Indien het gewenst is om de onderste laag in de scheitrechter te houden voor verdere extracties, worden beide lagen afzonderlijk verwijderd, waarna de voormalige onderste laag terug in de scheitrechter wordt geplaatst.
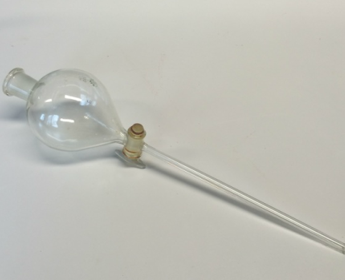
Een scheitrechter heeft de vorm van een kegel met een halfbolvormig uiteinde. Het heeft een stop bovenaan en een kraan (tap), aan de onderzijde. Scheitrechters die in laboratoria worden gebruikt, zijn meestal gemaakt van borosilicaatglas en hun kranen zijn gemaakt van glas of PTFE . Typische maten zijn tussen 30 ml en 3 L. In de industriële chemie kunnen ze veel groter zijn en voor veel grotere volumes worden centrifuges gebruikt. De schuine zijden zijn ontworpen om de identificatie van de lagen te vergemakkelijken. De door een kraan bediende uitlaat is ontworpen om de vloeistof uit de trechter te laten lopen. Bovenop de trechter zit een standaard conische voeg die past met een matglas of teflon stop.
Om een scheitrechter te gebruiken, worden de twee fasen en het in oplossing te scheiden mengsel via de bovenkant toegevoegd met de afsluitkraan aan de onderkant gesloten. De trechter wordt vervolgens gesloten en zachtjes geschud door de trechter meerdere keren om te keren; als de twee oplossingen te krachtig met elkaar worden gemengd, zullen zich emulsies vormen. De trechter wordt vervolgens omgekeerd en de kraan voorzichtig geopend om overtollige dampdruk af te laten . De scheitrechter wordt opzij gezet om een volledige scheiding van de fasen mogelijk te maken. De bovenste en onderste afsluitkraan worden dan geopend en de onderste fase wordt vrijgegeven door zwaartekracht. De bovenkant moet worden geopend terwijl de onderste fase wordt losgelaten om drukvereffening tussen de binnenkant van de trechter en de atmosfeer mogelijk te maken. Wanneer de onderste laag is verwijderd, wordt de afsluitkraan gesloten en wordt de bovenste laag door de bovenkant in een andere container gegoten.
Experiment
Materiaal + stoffen
- erlenmeyers
- scheitrechter met stop
- filter
- watten
- waterbad
- balans, horlogeglas
- glazen staaf
- lakmoespapier
- cafeïne houdende stof (koffie)
- natriumcarbonaat
- dichloormethaan
- magnesiumsulfaat
- geconc HCl
- Kaliumchloraat
- NH4OH 2 mol/l
Opstelling (foto)

Uitvoeren
Werkwijze
- Voeg 150 ml van de vloeistof (koffie) en 2 g natriumcarbonaat in een erlenmeyer. Test met lakmoespapier.
- Voeg 50 ml dichloormethaan toe en schud lichtjes gedurende 5 min. (Niet te hard of je krijgt een emulsie).
- Giet de oplossing in een scheitrechter en wacht 5 à 10 minuten tot zich twee lagen gevormd hebben. De onderste laag vang je op in een erlenmeyer.
- Bij de bovenste laag voeg je 50 ml dichloormethaan. Een paar maal de scheitrechter omkeren en de onderste fractie opvangen en bij de eerste voegen.
- Bij de dichloormethaanfractie doe je 5 mg magnesiumsulfaat als droogmiddel.
- We filtreren dit en laten het uitdampen.
- Het bekomen poeder wegen en de fractie berekenen.






