Licht en materie
http://phet.colorado.edu/en/simulation/molecules-and-light
Onderzoeksvraag:
Welke invloed hebben fotonen van een bepaald licht op verschillende moleculen?
Werkwijzen:
Zoek op in het elektromagnetisch spectrum tussen welke frequenties de gegeven lichtstralen zich bevinden. ( Vergeet de eenheden er niet bij te zetten!)
- microgolven: ……………………………………………………………………………………………………….
- infraroof: …………………………………………………………………………………………………………….
- zichtbaar licht: ……………………………………………………………………………………………………..
- ultraviolet: ……………………………………………………………………………………………………………
Groepeer de gegeven moleculen in onderstaand tabel

Maak gebruik van onderstaande symbolen.
Onderzoek wat koolstofmonoxide doet wanneer het in contact komt met de verschillende soorten licht en vul de tabel in met wat je ziet. Dit bij een minimale lichttoevoer.
Doe nu net hetzelfde, maar dan de lichttoevoer volledig aan. Bekijk ook steeds het moleculen in vertraagde versie.
Onderzoek vervolgend de volgende moleculen op dezelfde manier als je bij koolstofmonoxide hebt moeten doen.
Doe dit dan ook weer bij volle lichttoevoer en neem precies waar. (Gebruik dan ook weer de vertragende toets.)



Interpretatie:
Zet nu in onderstaande tabel welke moleculen een bepaalde beweging uitvoeren bij de soort lichtstraal.

Zet in onderstaande tabel de moleculen die geen licht absorberen

Wat valt er aan de intensiteit van de beweging van het moleculen. Kijk hiervoor van microgolven naar ultraviolet.
De moleculen gaan meer/ minder intensief bewegen naar maten men van microgolven naar ultraviolet golven gaat.
Open het extra venster (toon het magnetisch spectrum) en leg het verband tussen de frequentie en de golflengte.
………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………………
Bekijk de structuren en de bindingen van de moleculen en zet een kruisje bij hetgene wat toepasselijk is voor het moleculen
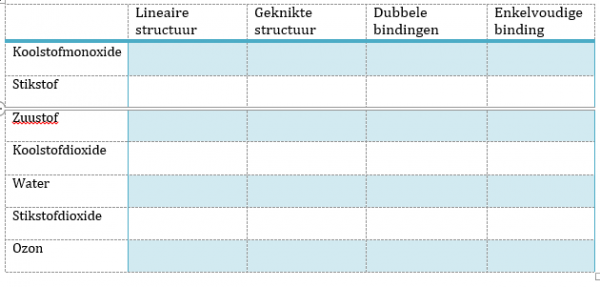
Besluit:
De soorten licht die we in deze proeven hebben gebruik komen ook voor in onze atmosfeer. Enkel zichtbaar licht kunnen wij zien met onze ogen. Zoals de ultravioletstralen kunnen enkel vlinders zien.
Wanneer we kijken naar het magnetisch spectrum kunnen we zien dat de microgolven de minste energie hebben en ook de grootste golflengte. Dit is logisch. Omdat we minder bewegingen per seconden gaan maken, wat men de frequentie noemt, is er ook minder energie die ontstaat. Dit kunnen we vergelijken met wanneer we lopen of wandelen. Wanneer we lopen hebben we op eenzelfde tijd een lange afstand afgelegd dan het wandelen, dus bij het lopen ook meer energie gebruikt.
De ultravioletstralen hebben een veel hogere energie en een kleinere golflengte. De golflengtes zijn weel korter en komen daardoor ook sneller op elkaar gevolgd wat er dan voor zorgt dat er meer energie wordt geproduceerd.
Wanneer de we verschillende moleculen dan bekijken kunnen we duidelijke verschillen zien. Alle moleculen buiten stikstofdioxiden, ozon en water zijn lineair gestructureerd. Deze lineaire structuur zorgt er voor dat de bindingen tussen de atomen zeer moeilijk gebroken kunnen worden. Ook hebben deze lineaire structuren dubbele en drievoudige bindingen die de breking van de bindingen nog moeilijker maken.
De drie andere moleculen hebben een geknikte structuur. Wanneer we dan kijken naar de specifieke bindingen zien we dat enkel water de zeer sterke waterstofbruggen kunnen vormen. Hierdoor zal deze ook bijna niet te breken zijn.
Hierdoor kunnen we zeggen dat de stikstofdioxiden en ozon moleculen zeer zwak zijn.
Wanneer we deze soorten bindingen en structuren gaan vergelijken met de soorten licht kunnen we deze dingen zeggen;
- De microgolven zijn de zwakst energetische golven, deze zorgen er enkel voor dat de moleculen die deze soorten licht absorberen zullen bewegen.
Een voorbeeld hiervan in water in een microgolf verwarmen, hierdoor gaan de waterdeeltjes sneller bewegen waardoor er dan de waterdamp ontstaat. - De infraroodgolven zijn ook nog zwak energetisch. Maar deze soorten golven zullen inwerken op de bindingen bij de stoffen die deze soort golven absorberen. De energetische waarden is hier nog te zwak om bepaalde bindingen te breken.
- Het zichtbare licht zijn al meer energetische golven. Deze golven hebben al genoeg energie om bindingen te breken, natuurlijk zal deze breking enkel mogelijk zijn om de enkelvoudige binding. Maar wanneer de aantrekkingskracht tussen de atomen te sterk is om te breken zullen de moleculen aangeslagen worden en de energie een periode bijhouden om vervolgens weer los te laten.
- Ultravioletgolven zijn de meest energetische golven. Deze zullen steeds zorgen voor breking van enkelvoudige bindingen.






