Elektrolyten en niet-elektrolyten2
Open deze link.
http://employees.oneonta.edu/viningwj/modules/CI_strong_weak_nonelectrolytes_4_05.html
Dit beeld verschijnt op de computer.
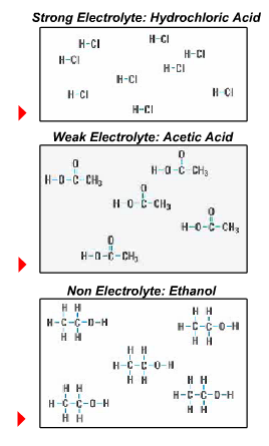
De rode driehoekjes zijn startknoppen.
Druk op de startknop om te zien wat er gebeurt en vul onderstaande vragen zorgvuldig in. Wees correct.
Eerst een kleine herhaling :
Een sterk elektrolyt is een chemische verbinding die in een oplossing of gesmolten toestand geheel in ionen splitst. Om zo elektrische stroom te geleiden.
Een zwak elektrolyt is een chemische verbinding die in een oplossing of gesmolten toestand gedeeltelijk in ionen splitst. Om zo elektrische stroom te geleiden.
Een niet elektrolyt is een chemische verbinding die niet splitst in ionen in een oplossing of in gesmolten toestand. En dus ook geen elektrische stroom geleidt.
1. H-Cl :
a. Wat neem je waar wanneer je op de startknop drukt?
b. Welk soort elektrolyt is dit en waarom denk je dit?
De HCl moleculen splitsten op in H+ en Cl–ionen
Dit is een sterk elektrolyt want alle atomen splitsen in ionen. .
2. CH3COOH :
a. Wat neem je waar wanneer je op de startknop drukt?
b. Welk soort elektrolyt is dit en waarom denk je dit?
Enkele CH3COOH moleculen splitsten op in H+ en CH3COO–ionen
Dit is een zwak elektrolyt want niet alle atomen splitsen in ionen. .
3. CH3CH2OH:
a. Wat neem je waar wanneer je op de startknop drukt?
b. Welk soort elektrolyt is dit en waarom denk je dit?
Enkele CH3CH2OH moleculen splitsten niet op in ionen . Dit is geen elektrolyt want geen atomen splitsen in ionen.






