Daniëllcel voor een lampje
1.Onderzoeksvraag
Hoe kan je een lampje laten branden zonder een batterij te gebruiken?
2. Materiaal + stoffen

- Koper(II)sulfaat oplossing (0 aq)
- Zinksulfaatoplossing (7 aq)
- Koper en zink elektroden
- Kaliumchloride
- Water
- Lepel
- Petrischaaltje
- Krokodillen klemmen
- Plastieke proefbuisjes/maatbekers
- Proefbuisrek
- LED/voltmeter
- Spuitjes
- Rechthoekig stuk stof
3.Uitvoeren
a.Werkwijze
- Knip twee reepjes uit een rechthoekig stuk stof.
- Maak een kaliumchloride-oplossing en dompel de reepjes stof hier in onder. 5 gram KCl + 100ml water.
- Plaats koper- en zinkelektroden in een maatbeker en plaats ze zo dat de metalen elkaar afwisselen (zink/koper/zink/koper).
- Verbind de elektroden met de krokodillenklemmen zodat de elektroden aan weerszijden een vrije klem hebben.
- Verbind de maatbekers met de stukjes stof die je ondergedompeld hebt in KCl-oplossing.
- Giet koper(II)sulfaatoplossing in de maatbekers met de koperelektroden en zinksulfaatoplossing in de flesjes met de zinkelektroden.
- Verbind de vrije uiteinden van de klemmen met een LED-lampje.
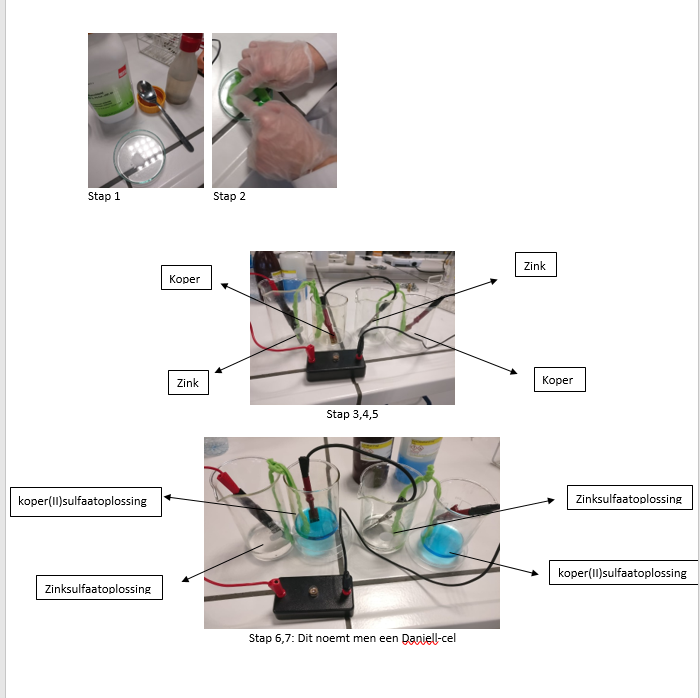
b.Waarneming (+ foto’s)

4.Reflecteren
Je kan een lampje laten branden door een Daniell-cell te maken. De Daniell-cell bestaat uit anoden (= de zink elektroden) en kathoden (= de koperen elektroden). Zink geeft makkelijk elektronen af, waarbij Zn2+-ionen worden gevormd die in de oplossing vrijkomen
(Zn – 2e → Zn²⁺). De vrijgekomen elektronen verplaatsen zich van de zink elektroden (anode) naar de koperen elektroden (kathode) (Cu²⁺ + 2e → Cu⁰). Doordat de elektronen door de draden van zink naar koper bewegen, vormen ze een elektrische stroom waardoor het lampje normaal zou moeten branden. In dit geval had het lampje meer Volt nodig om te branden.
5. Aanvullingen

