Constante van Avogadro
Inleiding
Een hoeveelheid kun je uitdrukken met een massa. Er bestaan hiervoor in het dagelijks leven nog andere manieren. Zo worden 12 eieren uitgedrukt als een dozijn eieren, 2 appelen als een paar en 1 gros nagels als 144 nagels.
Binnen de chemie drukken we de hoeveelheid stof uit in mol. Amedeo Avogadro (1776-1856) berekende voor het eerst het aantal deeltjes aanwezig in één mol van om het even welke stof. Hij definieerde daaruit de constante van Avogadro.
De constante van Avogadro = NA = 6,02 x 1023
In één mol van om het even welke stof zitten 6,02 x 1023 deeltjes.
Deel 1
Ga nu naar http://repo.unnes.ac.id/freeware/kimia/swf_1/solid_at.swf.
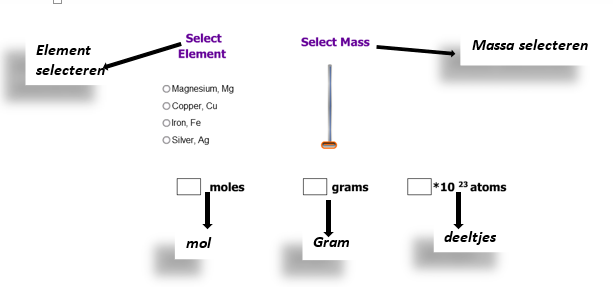
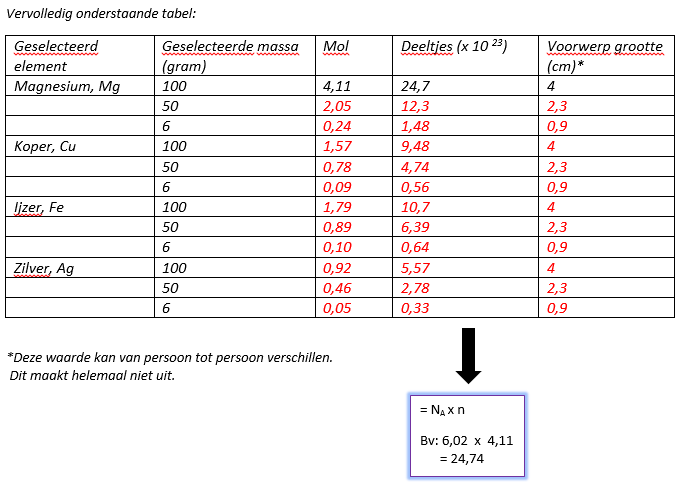
Besluit
Hoe groter de massa van een stof, hoe groter/ kleiner de mol waarde.
Hoe groter de massa van een stof, hoe meer/minder deeltjes.
Hoe groter de massa van een stof, hoe kleiner/ groter het voorwerp.






