ChemCollective: standaardisatie van een NaOH-oplossing
Ga naar deze link. Dan zie je dit verschijnen.
Als je drukt op ‘Standardization of NaOH’ opent er een venster met de instructies voor de proef.
In dit probleem zult u de concentratie van een oplossing van natriumhydroxide (NaOH) nauwkeurig bepalen met een 0.500 mol/l kaliumwaterstofftalaat (KHP) standaardoplossing. Zuur-base-indicator fenoftaleïne wordt toegevoegd in zijn (kleurloze) vorm aan een nauwkeurig volumemonster van KHP. De base NaOH wordt langzaam aan het monster KHP toegevoegd. Zodra alle KHP met de base heeft gereageerd, zal de eerste overmaat aan NaOH ervoor zorgen dat de indicator in de basisvorm (roze) wordt omgezet. De exacte concentratie van de NaOH-oplossing kan vervolgens worden berekend.
Experimentele procedure:
Haal de KHP, 1 mol/l NaOH-oplossing en de fenolftaleïne uit de opslagkamer (= solutions). Noteer het volume van KHP, dat u kunt vinden in het venster Solution Info.
Haal een wegwerppipet en een buret van 50 ml op.
Gebruik een wegwerppipet om een kleine hoeveelheid (-0,3 ml) indicator aan de KHP-oplossing toe te voegen.
Vul de buret met NaOH-oplossing.
Titreer kleine hoeveelheden (- 0,5 ml of minder) NaOH van de buret in de KHP tot een lichte kleurverandering optreedt. Noteer het gebruikte volume NaOH, dat u kunt vinden in het venster Solution Info.
Als je niet weet hoe je iets moet doen, kijk dan gerust op deze website.
Onderzoeksvraag
Hoe vinden we de concentratie van NaOH?
Voorbereiden
Definities:
Standaardisatie is het proces van het bepalen van de exacte concentratie (molariteit) van een oplossing.
Fenolftaleïne: fenolftaleïne is een zuur-base indicator, die kleurloos is in een zuur milieu en paars in een basisch milieu.
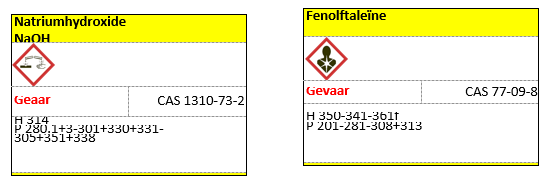
Materiaal/ stoffen:
| · NaOH· KHP· Fenolftaleïne | Bekerglas Buret 50ml |
Werkwijze:
- Plaats de KHP-oplossing, NaOH- oplossing en fenolftaleïne op de werktafel
- Doe 0,3ml fenolftaleïne in de KHP- oplossing
- Pak een buret van 50ml uit de stockroom
- Vul de buret met 45ml NaOH- oplossing
- Titreer kleine hoeveelheden (ongeveer 0,5ml) NaOH in de KHP-oplossing totdat je een kleurverandering opvalt.
- Noteer het gebruikte volume NaOH-oplossing
- Kijk naar de pH-waarde in de zijkolom.
- Voer de proef nu nog eens uit, maar titreer nog kleinere hoeveelheden (ongeveer 0,1).
Waarnemingen:
Vanaf welke pH waarde merk je een verschil op bij grote hoeveelheden en bij kleine hoeveelheden?
Bij grote hoeveelheden is de pH-waarde 11,76
Bij kleine hoeveelheden is de pH-waarde 7,78
Reflecteren:
| Titratie 1 (l) | Titratie 2 (l) | |
| Volume KHP | 0,025 | 0,025 |
| Volume NaOH gebruikt | 0,0138 | 0,0135 |
Reactievergelijking: KHP + NaOH → H2O + NaKP
We werken natuurlijk met de meest correcte titratie.
Hoeveel mol KHP zit er in de oplossing?
Tip: het aantal mol KHP is gelijk aan het aantal mol NaOH






