Atoombinding
APP: http://www.echalk.co.uk/Science/chemistry/bonding/bonding.html
Onderzoeksvraag:
Hoe kunnen twee dezelfde niet-metalen een binding vormen?
De binding tussen 2 O-atomen (niet-metalen) in O2.
Instructie:
Kijk aandachtig naar de simulatie. Probeer, na het bekijken van de simulatie, een antwoord te formuleren op volgende vraag: wat gebeurt er met de zuurstofatomen?
Waarneming:
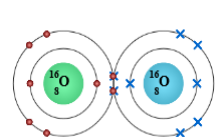
De zuurstofatomen gaan een binding vormen.

Elke atoom wil de edelgasconfiguratie bereiken, maar elk Cl-atoom heeft 6 valentie-elektronen en dus 2 te kort om een edelgasconfiguratie te verkrijgen. Zij kunnen niet van elkaar een elektron opnemen, dus zal elk O-atoom die ongepaarde elektronen
gemeenschappelijk stellen, er ontstaat twee gemeenschappelijke elektronenparen in de molecule (dubbele binding). (Duid deze aan in het blauw)

De ∆ EN tussen de bindingspartner is 0. Dat wil zeggen dat bij de atoombinding of covalente binding tussen dezelfde niet-metalen ∆EN = 0.
De EN-waarde geeft aan hoe sterk een element de neiging heeft om gebonden elektronenpaar zich toe te trekken.






