Waterstofchloraat
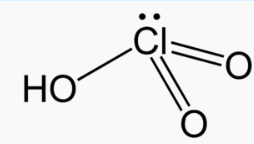
| Formule | HClO3 |
| Familie | anorganische zuren |
| Productie |
Het kan worden bereid door de reactie van zwavelzuur met bariumchloraat , waarbij het onoplosbare bariumsulfaat door neerslag wordt verwijderd:
Een andere methode is het verwarmen van hypochloorzuur , waarbij chloorzuur en waterstofchloride worden geproduceerd :
|
| Eigenschappen | |
| Toepassingen |
Een in de handel verkrijgbaar mengsel van 40% chloorzuur met rokend (38%) zoutzuur wordt Euchlorin genoemd . De combinatie van sterk zure en oxiderende eigenschappen kan helpen anders onoplosbare mineralen af te breken en organische stoffen te vernietigen. Het oxidatie-effect begint niet alleen bij het chloorzuur zelf, maar ook bij dichloor en chloordioxide, die tijdens de reactie met HCl worden gevormd: Meestal worden chloorzure zouten gebruikt ; bijvoorbeeld:
|
| Bronnen | KLIK |







