pHet zuur-base oplossingen
APP: https://phet.colorado.edu/sims/html/acid-base-solutions/latest/acid-base-solutions_nl.html
Klik op ‘mijn oplossing’.
Je ziet een beker met een oplossing. Van deze oplossing kan je op 2 manieren de pH – waarde meten; met een pH ‘meter’ en met een pH – strookje. Je kan ook de geleidbaarheid van de oplossing weergeven door de batterij met de positieve en de negatieve kant en de lamp.
Om deze allemaal toe te passen klik je simpel links onderaan bij ‘hulpmiddelen’ op hetgeen je wilt gebruiken. Dit wordt boven de beker zichtbaar:
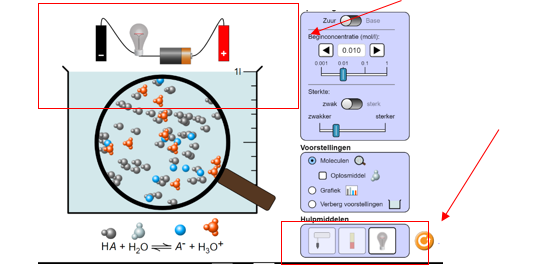
Als je daarna wil toepassen wat je hebt geselecteerd bij ‘hulpmiddelen’, klik je met je linker muisknop op je hulpmiddel dat nu boven de beker staat en sleep je het in het water.
Hierna kan je de gegevens duidelijk aflezen.
Je kan aan de rechterkant in de tabel ook de beginconcentratie aanpassen door het balkje te verschuiven en de sterkte aanpassen door de balk hieronder op zwak of op sterk te verschuiven. Bij ‘voorstellingen’ kan je op ‘Grafiek’ klikken. Dan krijg je een overzichtelijke weergave van de concentraties in je oplossing.
Oefeningen:
Geleidbaarheid:
Wat merk je op als je een sterk en een zwak zuur vergelijkt i.v.m. de geleidbaarheid in H2O-oplossing:
…………………………………………………………………………………………………………………………………………………………….
Wat merk je op als je een sterke en een zwakke base vergelijkt i.v.m. geleidbaarheid H2O-oplossing:
…………………………………………………………………………………………………………………………………………………………….
pH-waardes:
Wat gebeurt er met de pH – waarde van een zuur als je de concentratie verhoogt?
Hoe komt dit?
Wat gebeurt er met de pH – waarde van een base als je de concentratie verhoogt?
Hoe komt dit?
Wat is het evenwicht van een zuur bij een concentratie van 0,010 mol/l? (gebruik de grafiekfunctie)
Wat is het evenwicht van een zuur bij een concentratie van 0,1 mol/l? (gebruik de grafiekfunctie)
Vergelijk de 2 resultaten met elkaar:
Vergelijk een sterke base en zwakke base met elkaar, wat merk je op? Bekijk dit ook voor een zwak en een sterk zuur!
Leerdoelen: leerlingen zullen kunnen:
- Moleculaire voorstellingen kunnen interpreteren of geven voor zuur en base oplossingen.
- Geef of gebruik representaties van de relatieve hoeveelheden deeltjes in zuur- of baseoplossingen om de sterkte en / of concentratie te schatten.
- Gebruik algemene hulpmiddelen (pH-meter, geleidbaarheid, pH-papier) van zuur- of baseoplossingen om de sterkte en / of concentratie te schatten
Prelab:
- Water moleculen niet zichtbaar. Iedere beker bevat hetzelfde volume van de oplossing;
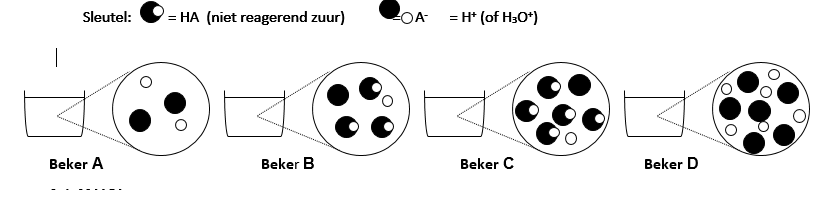
Wat kan het label op beker C zijn?
A. 0.01 mol/l HC2H3O2 B. 0.1 mol/l HC2H3O2 C. 0.3 mol/l HC2H3O2 D. 0.01 mol/l HCl E. 0.3 mol/l HCl
Welke beker zal de laagste pH hebben? A B C D
Leg je redenering uit voor beide vragen:Je hebt twee bekers. Eén beker bevat 100 ml NaOH (een sterke base); de andere bevat 100 ml waterige Na3PO4 (een zwakke base). U test de pH van elke oplossing. Welke van de volgende uitspraken is waar?
- Het Na3PO4 heeft een hogere pH omdat het meer natriumionen heeft dan NaOH.
- Het is mogelijk dat de oplossingen in elke beker dezelfde pH hebben.
- Als de pH van de NaOH-oplossing 12,00 is, moet de pH van de Na3PO4-oplossing groter zijn dan 12,00.
- Als de pH van de NaOH-oplossing 12,00 is, moet de pH van de Na3PO4-oplossing minder zijn dan 12,00.
Verklaar je redenering.
Lab: Visualisering van de zuursterkte, concentratie en pH
Verken de simulatie met uw groep en bespreek deze vragen. Gebruik de moleculaire weergave, pH, geleidbaarheid en staafdiagrammen.
- Wat gebeurt er met een zuur met het molecuul in een wateroplossing?
- Wat is er anders aan wat er gebeurt met een zwak zuurmolecuul en wat gebeurt er met een sterk zuurmolecuul?
- Hoe verschillen de representaties van een zwakke zure reactie van een sterke reactie?
- Als u de concentratie van een zuur verhoogt, welke veranderingen in beide soorten zuren?
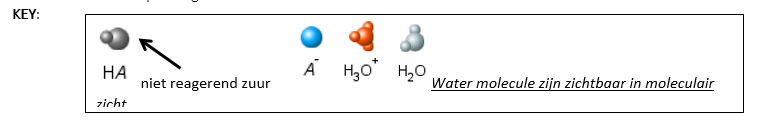
Deze afbeeldingen (moleculair beeld van oplossing / grafiek / pH / geleidbaarheid) geven een sterke zuuroplossing weer:
- Hoe verandert de Sleutel voor een zwak zuur?
- Hoe zouden de afbeeldingen veranderen voor een zwak zure oplossing met dezelfde concentratie? Teken de afbeeldingen en beschrijf ze in woorden.
- Teken de beelden voor een zwak zuur en een sterk zure oplossing van de grotere concentratie? Maak notities die je kunnen helpen herinneren.
- Schrijf de chemische reacties voor een zwak zuur en een sterk zuur.
- Is er een soort representatie die voor jou de beste zou kunnen zijn om informatie over zwakke en sterke zuren te onthouden? Maak notities die u kunnen helpen herinneren hoe u de twee typen kunt vergelijken / contrasteren.
Herhaal de delen A en B voor base oplossingen.






