pH-schaal
Inleiding:
Wat we hier hebben is een applet om het begrip pH-schaal te demonstreren. De pH-verdeling van 0 tot 14. Wanneer de pH van een stof/oplossing kleiner dan 7 is, is dit een zure pH-waarde. Omgekeerd voor een basische pH-waarde. Een pH-waarde van precies 7 noemen we een neutrale pH-waarde.
Een voorbeeld van een stof met een neutrale pH-waarde is water. We gaan met de applet onderzoeken wat het eigenlijk wilt zeggen wanneer een stof nu een zure of basische pH-waarde heeft.
Bekijk eerst eens de verschillende stoffen met hun pH-waarde die we in de maatbeker kunnen doen door linksboven op het pijltje te drukken.
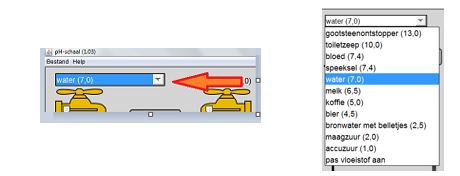
Selecteer dan water (7,0). Bekijk het diagram aan de rechter kant. Laat al het water dan weglopen door het kraantje links onder open te zetten.
Vul de maatbeker dan met accuzuur (1,0). Bekijk het diagram aan de rechterkant. Laat de maatbeker opnieuw leeglopen en vul het deze keer met toiletzeep (10,0). Bekijk opnieuw het diagram aan de rechterkant. Wat is het verschil tussen de 3 histogrammen (water-accuzuur-toiletzeep)?
Bij water zijn het aantal H3O+ en OH– deeltjes gelijk. Bij accuzuur zijn er meer H3O+ deeltjes en bij toiletzeep meer OH– deeltjes
Bekijk ook het histogram van toiletzeep maar klik eerst op ‘Aantal molen (mol)’. Laat deze keer de beker maar half leeg lopen.
Bekijk het diagram aan de rechterkant en vergelijk deze met het diagram toen de beker nog vol was. Wat merk je op? Het aantal H3O+ en OH– deeltjes zakken allebei evenveel.
Laat de beker opnieuw leeglopen en vul deze voor de helft met gootsteenontstopper (13,0). Vul de beker dan helemaal met water door het rechtse kraantje te gebruiken.
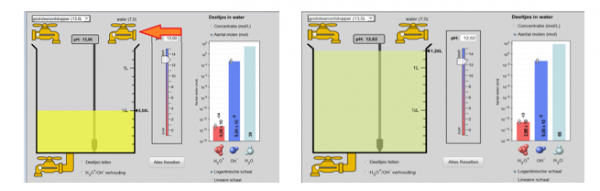
Wat valt je op aan de kleur van de vloeistof in de beker? De kleur van de vloeistof wordt minder geel.
Wat is er met de pH gebeurd? De pH-waarde is gezakt van 13,00 naar 12,62
Is er ook iets veranderd aan het histogram? Wat dan? Het aantal H3O+ deeltjes is gestegen, het aantal OH– deeltjes blijft gelijk.
Vink het vakje ‘H3O+ / OH– verhouding aan en kijk wat er gebeurd in de beker.

Wat valt je op? Er zijn veel meer OH– deeltjes dan H3O+ deeltjes.
Doe hetzelfde voor maagzuur (2,0). Wat valt je hier op? Er zijn veel meer H3O+ deeltjes dan OH– deeltjes.
Wat is het verband tussen het aantal H3O+ en OH– deeltjes en de pH van de vloeistoffen?Hoe meer H3O+ deeltjes er aanwezig zijn, hoe lager de pH-waarde.
Hoe meer OH- deeltjes er aanwezig zijn, hoe hoger de pH-waarde.
Kies nu zelf een bepaalde pH op de meter in het midden en voorspel op voorhand welke deeltjes er meer aanwezig zullen zijn (H3O+ of OH–).
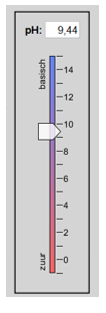
Gekozen pH-waarde:






