Fosforzuur
| Formule | H3PO4 triwaterstoffosfaat |
| Familie | anorganisch zuur |
| Productie | Nat proces
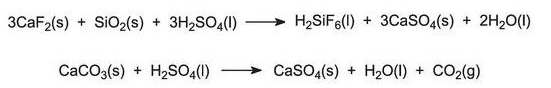
Fosforzuur wordt geproduceerd uit fluorapatiet, bekend als fosfaatgesteente, 3Ca3(PO4) 2.CaF2, door toevoeging van geconcentreerd (93%) zwavelzuur. De gevormde reactieproducten zijn fosforzuur, calciumsulfaat (gips) en onoplosbare onzuiverheden. Water wordt toegevoegd en hierdoor wordt het gips verwijderd door filtratie samen met andere onoplosbare materialen (bijvoorbeeld silica). Het fluoride wordt in een verdere fase door verdamping verwijderd. Hoewel de reactie plaatsvindt in fasen waarbij calciumdiwaterstof betrokken is, kan de algemene reactie worden voorgesteld als:
Het product uit het ‘nat proces’ is onzuiver en kan zonder verdere zuivering voor de vervaardiging van meststoffen gebruikt worden Als alternatief kan het verder verdampt tot ongeveer 70% P2O5, een oplossing die superfosforzuur genoemd wordt, dat direct gebruikt wordt als een vloeibare vruchtversterker. Om industriële fosfaten te maken wordt het zuur gezuiverd door middel van extractie waarin het zuur licht oplosbaar is en geconcentreerd wordt tot 60% P2O5. Dit zuur kan verder worden gezuiverd met behulp van oplosmiddelen om het uit zware metalen te onttrekken en te verdampen. (b) thermisch proces De grondstoffen voor dit proces zijn fosfor en lucht: In eerste instantie wordt fosfor in de oven gespoten en in lucht verbrand bij ongeveer 1800-3000 K. Als alternatief kan het fosfor in gedroogde lucht verbranden. Het fosforpentoxide wordt gecondenseerd als een wit poeder en afzonderlijk gehydrateerd tot fosforzuur.
|
| Eigenschappen | Fosforzuur is een heldere, kleurloze, geurloze vloeistof met een siroopachtige consistentie. KLIK |
| Toepassingen | Fosforzuur wordt gebruikt als verzurende middel om cola’s hun smakelijke smaak te geven. Door het gebruik van fosforzuur is cola zuurder dan citroensap of azijn! De grote hoeveelheid suiker maskeert de zuurgraad. KLIK Fosforzuur komt voor als E-nummer: E338 Fosforzuur wordt vaak gebruikt voor roestverwijdering. KLIK Fosforhoudende stoffen komen natuurlijk voor (0,1% -0,5%) in voedingsmiddelen zoals melk, vlees, pluimvee, vis, noten en eidooiers. Fosforzuur wordt gebruikt in tandheelkunde en orthodontie als etsoplossing, om de oppervlakken van de tanden te reinigen en te ruwen om nadien vullingen te plaatsen. Dit zuur wordt ook gebruikt in vele tandwitters om plaque te elimineren. KLIK |
| Geschiedenis | Fosforzuur werd onafhankelijk ontdekt als een bestanddeel van botas in 1770 door twee Zweedse chemici, Johann Gottlieb Gahn (1745-1818) KLIK
en Karl Wilhelm Scheele (1742-1786). KLIK |
| Bronnen | KLIK – KLIK – KLIK |